题目内容
13.铁触媒是重要的催化剂,CO易与铁触媒作用导致其失去催化活性:Fe+5CO=Fe(CO)5;除去CO的化学反应方程式为:[Cu(NH3)2]OOCCH3+CO+NH3=[Cu(NH3)3(CO)]OOCCH3.请回答下列问题:
(1)C、N、O的电离能由大到小的顺序为N>O>C,基态Fe原子的价电子排布式为3d64s2.
(2)Fe(CO)5又名羰基铁,常温下为黄色油状液体,则Fe(CO)5的晶体类型是分子晶体,
Fe(CO)5在空气中燃烧后剩余的固体呈红棕色,相应的化学方程式为4Fe(CO)5+13O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3+20CO2.
(3)gd合物[Cu(NH3)2]OOCCH3中碳原子的杂化类型是sp3、sp2,配体中提供孤对电子的原子是N.
(4)用[Cu(NH3)2]OOCCH3除去CO的反应中,肯定有bd形成.
a.离子键 b.配位键 c.非极性键 d.δ键
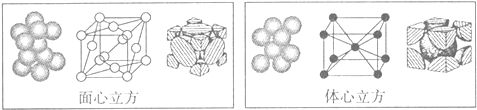
(5)单质铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示,面心立方晶胞和体心立方晶胞中实际含有的铁原子个数之比为2:1,面心立方堆积与体心立方堆积的两种铁晶体的密度之比为4$\sqrt{2}$:3$\sqrt{3}$(写出已化简的比例式即可).
分析 (1)同一周期元素,ⅤA第一电离能大于ⅥA族;Fe原子3d、4s能级电子为其价电子;
(2)熔沸点较低的晶体为分子晶体;Fe(CO)5在空气中燃烧后剩余的固体呈红棕色,为氧化铁,同时生成C的稳定氧化物二氧化碳;
(3)该配合物中C原子价层电子对个数是4和3且不含孤电子对,根据价层电子对互斥理论确定C原子杂化方式;该配体中Cu原子提供空轨道、N原子提供孤电子对;
(4)用[Cu(NH3)2]OOCCH3除去CO的反应中,肯定有配位键和δ键生成;
(5)利用均摊法计算晶胞中Fe原子个数;根据密度公式ρ=$\frac{m}{V}$计算.
解答 解:(1)N的电离能大于O,这三种元素第一电离能大小顺序是N>O>C;Fe原子3d、4s能级电子为其价电子,基态Fe原子的价电子排布式为3d64s2,
故答案为:N>O>C;3d64s2;
(2)熔沸点较低的晶体为分子晶体,Fe(CO)5又名羰基铁,常温下为黄色油状液体,其熔沸点较低,为分子晶体;Fe(CO)5在空气中燃烧后剩余的固体呈红棕色,为氧化铁,同时生成C的稳定氧化物二氧化碳,
反应方程式为4Fe(CO)5+13O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3+20CO2,
故答案为:分子晶体;4Fe(CO)5+13O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3+20CO2;
(3)该配合物中C原子价层电子对个数是4和3且不含孤电子对,根据价层电子对互斥理论确定C原子杂化方式为sp3、sp2,该配体中Cu原子提供空轨道、N原子提供孤电子对,
故答案为:sp3、sp2;N;
(4)用[Cu(NH3)2]OOCCH3除去CO的反应中,肯定有Cu原子和N、C原子之间的配位键且也是δ键生成,
故选bd;
(5)利用均摊法计算晶胞中Fe原子个数,面心立方晶胞中Fe原子个数=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4、体心立方晶胞中Fe原子个数=1+8×$\frac{1}{8}$=2,所以二者Fe原子个数之比=4:2=2:1;
设Fe原子半径为rcm,面心立方晶胞半径=2$\sqrt{2}$rcm,其体积=(2$\sqrt{2}$rcm)3,
体心立方晶胞半径=$\frac{4\sqrt{3}}{3}$rcm,体积=($\frac{4\sqrt{3}}{3}$rcm)3,
其密度之比=$\frac{\frac{4M}{{N}_{A}}}{(2\sqrt{2}r)^{3}}$:$\frac{\frac{2M}{{N}_{A}}}{(\frac{4\sqrt{3}}{3})^{3}}$=4$\sqrt{2}$:3$\sqrt{3}$,
故答案为:2:1;4$\sqrt{2}$:3$\sqrt{3}$.
点评 本题考查晶胞计算,为高频考点,侧重考查学生分析计算及空间想象能力,涉及晶胞计算、原子杂化方式判断、元素周期律等知识点,难点是晶胞计算,注意Fe晶胞面心立方和体心立方区别,关键会正确计算两种晶胞体积,题目难度中等.

 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案I CaCO3 (s)?CO2 (g)+CaO(s)△H=+178kJ/mol
ⅡSO2(g)+CaO(s)?CaSO3(s)△H=-402kJ/mol
Ⅲ2CaS03(S)+02 (g)+4H2O(I)?2(CaS04•2H2O](S)△H=-234.2kJ/mol
(1)试写出由石灰石、二氧化硫、氧气和水反应生成生石膏的热化学方程式2SO2(g)+2CaS03(s)+02(g)+4H2O(l)=2[CaS04•2H2O](s)△H=-681.8kJ/mol.
(2)反应Ⅱ为烟气除硫的关健,取相同用量的反应物在3种不网的容器中进行该反应,A容器保持恒温恒压,B容器保持恒温恒容,C容器保持恒容絶热,且初始时3个容器的容积和温度均相同,下列说法正确的是ad.
a.3个容器中SO2的平衡转化率的大小顺序为 aA>aB>aC.
b.当A容器内气体的平均摩尔质量不变时,说明谈反应处于化学平衡状态
c.A、B两个容器达到平衡所用的时间:tA>tB
d.当C容器内平衡常数不变时,说明该反应处于化学平衡状态
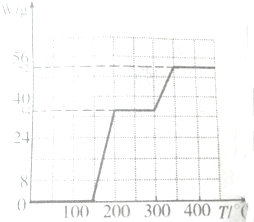
(3)依据上述反应Ⅱ来除硫,将一定量的烟气压缩到一个20L的容器中,测得不同温度下,容器内SO2的质量(mg)如下表:
| 时间/min SO3/mg 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | 120 |
| T1 | 2100 | 1052 | 540 | 199 | 8.7 | 0.06 | 0.06 |
| T2 | 2100 | 869 | 242 | x | x | x | x |
②若其它条件都相同T1< T2,《填“>”、“<”或“=”下同);x>0.06.
③在T2温度下,若平衡后将容器的容器压缩为10L,则新平衡时SO2的浓度平衡时SO2的浓度=(填“>”、“C”或“=”)理由是该反应的平衡常数表达式为K=$\frac{1}{c(S{O}_{2})}$,温度不变,K不变,所以浓度相等.
| 污染指数 | 首要污染物 | 空气质量级别 | 空气质量状况 |
| 55 | SO2 | II | 良 |
(1)用如图所示装置进行实验.
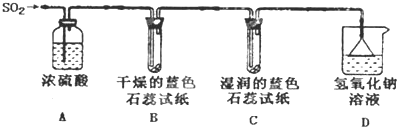
①A装置的作用是干燥二氧化硫.
②实验过程中,B装置内石蕊试纸的颜色没有发生变化,C装置内湿润的蓝色石蕊试纸变成红色,说明SO2与水反应生成一种酸,其化学反应方程式是SO2+H2O=H2SO3.
③D装置的作用是吸收S02,防止污染空气,D中发生反应的化学方程式是S02+2NaOH=Na2S03+H20.
(2)往盛有水的烧杯中通入SO2气体,测得所得溶液的pH<7(填“>”“=”或“<”),然后每隔1h测定其pH,发现pH逐渐变小(填“变大”或“变小”),直至恒定,原因是2H2SO3+O2=4H++SO42-(写出反应的离子方程式).
(3)SO2形成酸雨的另一途径为:SO2与空气中的O2在飘尘的作用下反应生成SO3,SO3溶于降水生成H2SO4,则在此过程中的飘尘是作为催化剂(填“催化剂”或“氧化剂”).
(4)SO2与空气中的氧气、水反应生成硫酸而形成酸雨.该市可能易出现酸雨.
(5)汽车排放的尾气,硝酸、化肥等工业生产排出的废气中都含有氮的氧化物,氮的氧化物溶于水最终转化为硝酸,是造成酸雨的另一主要原因.
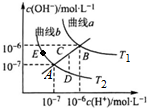
| A. | 图中温度T2>T1 | |
| B. | 曲线a、b均代表纯水的电离情况 | |
| C. | 图中五点的Kw的关系:B>C>A>D=E | |
| D. | 若处在B点时,将pH=2的硫酸溶液与pH=12的KOH溶液等体积混合后,溶液呈碱性 |
| A. | M的气态氢化物与其最高价氧化物的水化物之间能相互反应 | |
| B. | N单质能将K从其钠盐的水溶液中置换出来 | |
| C. | N的氢化物沸点高于其它同族元素氢化物的沸点 | |
| D. | P、Q、K对应的最高价氧化物的水化物相互之间可能发生反应 |
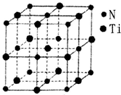 金属钛(Ti)被誉为21世纪金属,其单质和化合物具有广泛的应用价值.请回答下列问题:
金属钛(Ti)被誉为21世纪金属,其单质和化合物具有广泛的应用价值.请回答下列问题:(1)Ti的基态原子价电子排布式为3d24s2.
(2)纳米TiO2常用作下述反应的催化剂.
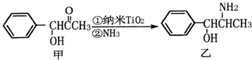
化合物甲的分子中采取sp2方式杂化的碳原子有7个,化合物乙中采取sp3方式杂化的原子对应的元素的电负性由大到小的顺序为O>N>C.
(3)含Ti3+的配合物的化学式为[TiCl(H2O)5]Cl2•H2O,其配离子中含有的化学键类型是共价键、配位键,1mol该配合物中含有的σ键数目是18NA.
(4)通过X-射线探知KCl、MgO、CaO、TiN的晶体与NaCl的晶体结构相似.且知三种离子晶体的晶格能数据如表:
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ•mol-1 | 786 | 715 | 3401 |
(5)某种氮化钛晶体的晶胞如图所示,该晶体中与N原子距离相等且最近的N原子有12个:Ti原子的配位数为6;此配位原子构成的空间构型为正八面体;该晶胞中N、Ti原子之间的最近距离为a nm.则该氮化钛晶体的密度为$\frac{4×62}{{N}_{A}×(2a×1{0}^{-7})^{3}}$g•cm-3、NA为阿伏加德罗常数的值,只列计算式).
 2H2(g)+O2(g)ΔH1=571.6kJ/mol
2H2(g)+O2(g)ΔH1=571.6kJ/mol