题目内容
8.加强空气质量检测,客观分析空气中污染物的来源及性质,将有助于制定有针对性的治理措施.表是某城市某日的空气质量报告:| 污染指数 | 首要污染物 | 空气质量级别 | 空气质量状况 |
| 55 | SO2 | II | 良 |
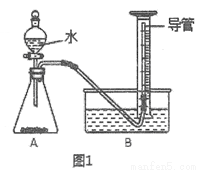
(1)用如图所示装置进行实验.
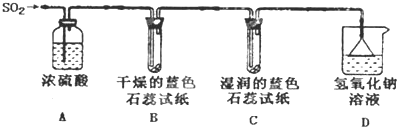
①A装置的作用是干燥二氧化硫.
②实验过程中,B装置内石蕊试纸的颜色没有发生变化,C装置内湿润的蓝色石蕊试纸变成红色,说明SO2与水反应生成一种酸,其化学反应方程式是SO2+H2O=H2SO3.
③D装置的作用是吸收S02,防止污染空气,D中发生反应的化学方程式是S02+2NaOH=Na2S03+H20.
(2)往盛有水的烧杯中通入SO2气体,测得所得溶液的pH<7(填“>”“=”或“<”),然后每隔1h测定其pH,发现pH逐渐变小(填“变大”或“变小”),直至恒定,原因是2H2SO3+O2=4H++SO42-(写出反应的离子方程式).
(3)SO2形成酸雨的另一途径为:SO2与空气中的O2在飘尘的作用下反应生成SO3,SO3溶于降水生成H2SO4,则在此过程中的飘尘是作为催化剂(填“催化剂”或“氧化剂”).
(4)SO2与空气中的氧气、水反应生成硫酸而形成酸雨.该市可能易出现酸雨.
(5)汽车排放的尾气,硝酸、化肥等工业生产排出的废气中都含有氮的氧化物,氮的氧化物溶于水最终转化为硝酸,是造成酸雨的另一主要原因.
分析 (1)①根据浓硫酸具有吸水性分析;
②二氧化硫为酸性氧化物,能够与水反应生成亚硫酸,亚硫酸电离生成氢离子,据此解答;
③根据二氧化硫的性质以及污染空气进行解答;
(2)二氧化硫与水反应生成弱酸亚硫酸,亚硫酸不稳定容易被氧气氧化生成硫酸;
(3)SO2与空气中的O2在飘尘的作用下反应生成SO3,SO3溶于降水生成H2SO4,飘尘起催化作用;
(5)二氧化氮溶于水,生成硝酸和一氧化氮,按一定比例混合一氧化氮氧气和水,或二氧化氮和氧气和水可几乎完全转化为硝酸.
解答 解:(1)①二氧化硫与浓硫酸不反应,浓硫酸有吸水性,可以吸收二氧化硫中的水蒸气,所以浓硫酸的作用为:干燥二氧化硫气体,
故答案为:干燥二氧化硫;
②二氧化硫为酸性氧化物,能够与水反应生成亚硫酸,方程式:SO2+H2O=H2SO3,亚硫酸电离生成氢离子,溶液显酸性,遇到石蕊显红色;
故答案为:红色;SO2+H2O=H2SO3;
③二氧化硫任意排放会造成酸雨,为了防止污染空气,用氢氧化钠溶液吸收;反应的化学方程式是S02+2NaOH=Na2S03+H20,
故答案为:吸收多余SO2气体,避免污染空气;S02+2NaOH=Na2S03+H20;
(2)二氧化硫与水反应生成弱酸亚硫酸,溶液显酸性,所以pH小于7,亚硫酸不稳定容易被氧气氧化生成硫酸,方程式:2H2SO3+O2=2H2SO4,离子方程式:2H2SO3+O2=4H++SO42-;硫酸为强酸,完全电离,溶液氢离子浓度增大,酸性增强,pH减小;
故答案为:<;变小;2H2SO3+O2=4H++SO42-;
(3)S02与空气中的02在飘尘的作用下反应生成S03,而飘尘的质量和性质在反应前后不发生变化,说明此过程中飘尘作催化剂,
故答案为:催化剂;
(5)氮的氧化物在空气中:2NO+O2=2NO2,3NO2+H2O=2HNO3+NO,4NO2+O2+2H2O═4HNO3,4NO+3O2+2H2O═4HNO3,所以氮的氧化物溶于水最终转化为硝酸,
故答案为:硝酸.
点评 本题主要考查了酸雨的形成,侧重考查了二氧化硫的性质,注意二氧化硫对空气的污染和二氧化硫的吸收的反应原理,题目难度中等.

 某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂.请填写下列空白:
某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂.请填写下列空白:(1)用标准的盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视锥形瓶中溶液颜色变化,直到因加入一滴盐酸后,溶液由黄色变为橙色,并半分钟内不复原为止.
(2)下列操作中可能使所测NaOH溶液的浓度数值偏低的是D(填字母序号).
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
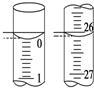
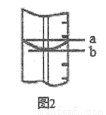
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示,则所用盐酸溶液的体积为26.10mL.
(4)某学生根据3次实验分别记录有关数据如表:
| 滴定次数 | 待测NaOH溶液的体积/mL | 0.100 0 mol•L-1盐酸的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
 二甲醚(CH3OCH3)是一种重要的清洁燃料,也可替代氟利昂作做冷剂等,对臭氧层无破坏作用.工业上以水煤气(CO、H2)为原料生产二甲醚CH3OCH3的新工艺主要发生三个反应:
二甲醚(CH3OCH3)是一种重要的清洁燃料,也可替代氟利昂作做冷剂等,对臭氧层无破坏作用.工业上以水煤气(CO、H2)为原料生产二甲醚CH3OCH3的新工艺主要发生三个反应:2H2(g)+CO(g)?CH3OH(g)△H=-90.0kJ.mol-1 ①
2CH3OH(g)?CH3OCH(g)+H2O (g)△H=-24.5kJ.mol-1②
CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41.1kJ.mol-1③
回答下列问题:
(1)新工艺的总反应3H2+3CO?CH3OCH3+CO2的热化学方程式为3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)△H=-245.6kJ/mol.
(2)已知一些共价键的键能如下:
| 化学键 | H-H | C-H | C-O | O-H |
| 键能(kJ.mol-1 | 436 | 414 | 326 | 464 |
(3)在250℃恒容密闭容器中,下列事实可以说明反应③已达平衡的是(填选项字母)BC.
A.容器内气体密度保持不变
B.CO与CO2的物质的量之比保持不变
C.H2O与CO2的生成速率之比为1:1
D.该反应的平衡常数保持不变
(4)某温度下,将2mol CO和6mol H2充入2L的密闭容器中,充分反应10min后,达到平衡时测得c(CO)=0.2mol/L,计算此温度下的平衡常数K=2.042.
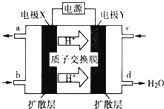
(5)绿色电源“二甲醚-氧气燃料电池”的工作原理如图所示.
①氧气应从C处通入,电极Y为正极,发生的电极反应式为O2+4e-+4H+═2H2O;
②二甲醚(CH3)2O应从b处加入,电极X上发生的电极反应式为(CH3)2O-12e-+3H2O=2CO2+12H+;
③电池在放电过程中,电极X周围溶液的pH减小 (填“增大”“减小”或“不变”).

 .
.
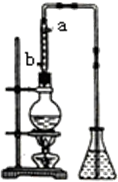 市售乙醛通常为40%左右的乙醛溶液.久置的乙醛溶液会产生分层现象,上层为无色油状液体,下层为水溶液.据测定,上层物质为乙醛的加合物(C2H4O)n,它的沸点比水的沸点高,分子中无醛基.乙醛在溶液中易被氧化,为从变质的乙醛溶液中提取乙醛(仍得到溶液),可利用如下反应原理:(C2H4O)n$\stackrel{H+}{→}$n(C2H4O).
市售乙醛通常为40%左右的乙醛溶液.久置的乙醛溶液会产生分层现象,上层为无色油状液体,下层为水溶液.据测定,上层物质为乙醛的加合物(C2H4O)n,它的沸点比水的沸点高,分子中无醛基.乙醛在溶液中易被氧化,为从变质的乙醛溶液中提取乙醛(仍得到溶液),可利用如下反应原理:(C2H4O)n$\stackrel{H+}{→}$n(C2H4O).