题目内容
3.已知一些银盐的颜色和Ksp(20℃)如下,测定水体中氯化物的含量,常用标准硝酸银溶液进行滴定.| 化学式 | AgCl | AgBr | AgI | Ag2S | Ag2CrO4 |
| 颜色 | 白色 | 浅黄色 | 黄色 | 黑色 | 红色 |
| Ksp | 1.8×10-10 | 5.0×10-13 | 8.3×10-17 | 2.0×10-48 | 1.8×10-10 |
| A. | KBr | B. | KI | C. | K2S | D. | K2CrO4 |
分析 滴定实验是利用沉淀变色指示反应沉淀完全,在氯化银刚好沉淀完成,再滴加硝酸银溶液,与指示剂作用生成不同现象来进行判断;测定水体中氯化物的含量,必须使氯离子完全生成白色沉淀,指示沉淀反应完全的试剂溶解性一定小于氯化银,所以本题应在Ag+和Cl-生成AgCl沉淀后,再生成不同颜色沉淀指示沉淀终点.则指示剂的溶解度应比AgCl大来分析判断.
解答 解:指示剂的作用是指示出氯离子恰好沉淀完全,即让氯离子先沉淀,沉淀完全后,再滴入硝酸银溶液会生成一种颜色不同的沉淀来指示沉淀终点.
A.氯化银、溴化银、碘化银的组成都是1:1,依据Ksp可以直接比较溶解性大小为氯化银>溴化银>碘化银;随Ksp的减小,应先出现碘化银沉淀、再出现溴化银,最后才沉淀氯化银;所以不符合滴定实验的目的和作用,不能测定氯化物的含量,故A错误;
B.依据A分析可知碘化银优先于氯化银析出,不能测定氯化物的含量,故B错误;
C.硫化银的Ksp很小,Ksp=[Ag+]2[S2-]=2.0×10-48,计算得到需要的银离子浓度[S2-]=$\root{3}{\frac{2.0×1{0}^{-48}}{4}}$;Ksp(AgCl)=[Ag+][Cl-]=1.8×10-10,[Cl-]=$\sqrt{1.8×1{0}^{-10}}$,通过计算得出硫化银也比氯化银先沉淀,故C错误;
D.铬酸银的阳、阴离子个数比为2:1,可以计算相同浓度的银离子沉淀氯离子、铬酸根离子需要的浓度,依据Ksp计算得到,Ksp(AgCl)=[Ag+][Cl-]=1.8×10-10,[Cl-]=$\sqrt{1.8×1{0}^{-10}}$,Ksp(Ag2CrO4)=[Ag+]2[CrO42-]=1.8×10-10,[CrO42-]=$\root{3}{\frac{1.8×1{0}^{-10}}{4}}$;所以同浓度的银离子需要的氯离子浓度小于铬酸根离子浓度,说明铬酸银溶解度大于氯化银,加入K2CrO4,做指示剂可以正确的测定氯化物的含量,故D正确;
故选D.
点评 本题考查了沉淀溶解平衡的计算判断,题目难度中等,明确在Ag+和Cl-生成AgCl沉淀后,再生成不同颜色沉淀指示沉淀终点是解答关键.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 反应物总能量高于生成物的总能量的反应为放热反应 | |
| B. | 化学键的断裂和形成是化学反应中能量变化的主要原因 | |
| C. | 只有氧化还原反应中的化学能才有可能转化为电能---形成原电池 | |
| D. | 需要加热才能发生的反应都是吸热反应 |
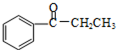 +H2N-NH2$→_{△}^{NaOH/(HOCH_{2}CH_{2})_{2}O}$
+H2N-NH2$→_{△}^{NaOH/(HOCH_{2}CH_{2})_{2}O}$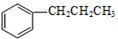 +X(g)+Y(l)
+X(g)+Y(l)其中,X和Y不污染环境,下列说法中不正确的是( )
| A. | 肼作还原剂 | B. | X是N2 | ||
| C. | Y是H2O | D. | 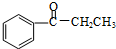 在酸性条件下水解为苯甲酸和乙醇 在酸性条件下水解为苯甲酸和乙醇 |
| A. | 原混合物中CuO与Fe2O3物质的量的比为1:2 | |
| B. | 原混合物中CuO与Fe2O3的质量比为2:1 | |
| C. | 吸收CO2后的溶液中一定有Ba(HCO3)2 | |
| D. | 反应中生成的CO2体积为1.792L |
| A. | 若铁粉有剩余,则不溶物中一定有铜 | |
| B. | 若铁粉有剩余,则溶液中的金属阳离子只有Fe2+ | |
| C. | 若铁粉无剩余,且溶液中有Cu2+,则溶液中一定无Fe3+ | |
| D. | 若铁粉无剩余,且溶液中无Cu2+,则溶液中一定有Fe2+,一定无Fe3+ |
A.A B.B C.C D.D
| a | b | ||||||||||||||||
| d | e | f | |||||||||||||||
| c | g | h | |||||||||||||||
| A | B | C | D | ||||||||||||||
甲、乙两元素相比较,金属性较强的是镁(填名称),可以验证该结论的实验是BC.
A.将在空气中放置很久的这两种元素的块状单质分别放入热水中
B.将这两元素的单质粉末分别和同浓度的盐酸反应
C.将这两元素的单质粉末分别和热水作用,并滴入酚酞
D.比较这两种元素的气态氢化物的稳定性
(3)上表中所列某些元素间能形成等电子的A、B、C、D、E五种微粒,A与C组成元素相同,B、E、D组成元素相同,它们间能发生如下反应:A+B=C+D,E+B=2D,则写出E的电子式:
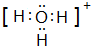
(4)“神舟六号”载人飞船舱内有一种化合物来吸收航天员呼出的CO2,你认为该物质是由上表中c、f(填字母)元素组成的,写出该反应的化学方程式2Na2O2+2CO2═2Na2CO3+CO2.
| A. | 石油分馏、煤的干馏均是物理变化 | |
| B. | 铅蓄电池、锂电池、碱性锌锰干电池都属于二次电池 | |
| C. | 资源的“3R”即减少消耗(Reduce)、增加重复使用(Reuse)、重复再生(Recycle)有利于实现“低碳生活” | |
| D. | PM2.5是指氮、硫的氧化物溶于水形成的酸性液体造成的空气污染 |
| A. | NaOH | B. | H2SO4 | C. | Na2CO3 | D. | Na2SO4 |