题目内容
9.pH=a的某电解质溶液中,插入两只惰性电极,通直流电一段时间后,溶液的pH<a,则该电解质可能是( )| A. | NaOH | B. | H2SO4 | C. | Na2CO3 | D. | Na2SO4 |
分析 pH=a的某电解质溶液中,插入两只惰性电极,通直流电一段时间后,溶液的pH<a,说明溶液酸性增强,溶液中的溶质可能是含氧酸、H之后的不活泼非金属的含氧酸盐等,据此分析解答.
解答 解:A.电解NaOH溶液时,阳极上生成氧气、阴极上生成氢气,所以相当于生成水,导致溶液中c(NaOH)增大,溶液的pH增大,不符合题意,故A错误;
B.电解稀硫酸时,阳极上生成氧气、阴极上生成氢气,所以相当于生成水,导致溶液中c(H2SO4)增大,溶液的pH减小,符合题意,故B正确;
C.电解碳酸钠溶液时,阳极上生成氧气、阴极上生成氢气,所以相当于生成水,导致溶液中c(Na2CO3)增大,溶液的碱性增强,故C错误;
D.电解硫酸钠溶液时,阳极上生成氧气、阴极上生成氢气,所以相当于生成水,导致溶液中c(Na2SO4)增大,但硫酸钠溶液呈中性,所以溶液的pH不变,故D错误;
故选B.
点评 本题考查电解原理,为高频考点,明确离子放电顺序是解本题关键,注意:电解这几种溶液时都相当于电解水,溶质的物质的量不变但溶剂的物质的量减小导致溶液浓度增大,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
3.已知一些银盐的颜色和Ksp(20℃)如下,测定水体中氯化物的含量,常用标准硝酸银溶液进行滴定.
滴定时,你认为该滴定适宜选用的指示剂是下列中的 ( )
| 化学式 | AgCl | AgBr | AgI | Ag2S | Ag2CrO4 |
| 颜色 | 白色 | 浅黄色 | 黄色 | 黑色 | 红色 |
| Ksp | 1.8×10-10 | 5.0×10-13 | 8.3×10-17 | 2.0×10-48 | 1.8×10-10 |
| A. | KBr | B. | KI | C. | K2S | D. | K2CrO4 |
17.下列元素非金属性最强的是( )
| A. | Cl | B. | F | C. | N | D. | O |
14.氢氧化镁用于制药工业,还是重要的绿色阻燃剂.
Ⅰ.治疗胃酸过多药物Stmoache的有效成分为Mg(OH)2.
(1)该药物治疗胃酸(主要成分为盐酸)过多症时反应的离子式方程式为Mg(OH)2+2H+=Mg2++2H2O;
Ⅱ.已知:
H2O(g)=H2(g)+$\frac{1}{2}$O2(g)△H1=+242kJ•mol-1
Mg(s)+2H2O(g)=Mg(OH)2(s)+H2(g)△H2=-441kJ•mol-1
Mg(s)+$\frac{1}{2}$O2(g)=MgO(s)△H3=-602kJ•mol-1
(2)氢氧化镁分解的热化学方程式为Mg(OH)2(s)=MgO(s)+H2O(g);△H=81KJ/mol;
Ⅲ.某工厂用六水合氯化镁和粗石灰制取的氢氧化镁含有少量氢氧化铁杂质,通过如下流程进行提纯精制.获得阻燃剂氢氧化镁.
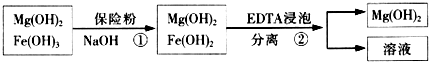
(3)步骤①中加入保险粉(Na2S2O4)的作用:将氢氧化铁还原为氢氧化亚铁.
(4)已知EDTA只能与溶液中的Fe2+反应生成易溶于水的物质,不与Mg(OH)2反应.虽然Fe(OH)2难溶于水,但步骤②中随着EDTA的加入,最终能够将Fe(OH)2除去并获得纯度高的Mg(OH)2.请从沉淀溶解平衡的角度加以解释Fe(OH)2悬浊液中存在如下平衡:Fe(OH)2(s)=Fe2+(aq)+2OH-(aq)当不断滴入EDTA时,EDTA将结合Fe 2+促使平衡向右移动而使Fe(OH)2不断溶解;
Ⅳ.为研究不同分离提纯条件下所制得阻燃剂的纯度从而确定最佳提纯条件,某研究小组各取等质量的下列4组条件下制得的阻燃剂进行含铁量的测定,结果如下:
(5)若不考虑其它条件,根据上表数据,制取高纯度阻燃剂最佳条件是C(填字母).
①40℃②60℃③EDTA质量为0.05g④EDTA质量为0.10g ⑤保险粉质量为0.05g ⑥保险粉质量为0.10g
A.①③⑤B.②④⑥C.①④⑥D.②③⑤
Ⅰ.治疗胃酸过多药物Stmoache的有效成分为Mg(OH)2.
(1)该药物治疗胃酸(主要成分为盐酸)过多症时反应的离子式方程式为Mg(OH)2+2H+=Mg2++2H2O;
Ⅱ.已知:
H2O(g)=H2(g)+$\frac{1}{2}$O2(g)△H1=+242kJ•mol-1
Mg(s)+2H2O(g)=Mg(OH)2(s)+H2(g)△H2=-441kJ•mol-1
Mg(s)+$\frac{1}{2}$O2(g)=MgO(s)△H3=-602kJ•mol-1
(2)氢氧化镁分解的热化学方程式为Mg(OH)2(s)=MgO(s)+H2O(g);△H=81KJ/mol;
Ⅲ.某工厂用六水合氯化镁和粗石灰制取的氢氧化镁含有少量氢氧化铁杂质,通过如下流程进行提纯精制.获得阻燃剂氢氧化镁.
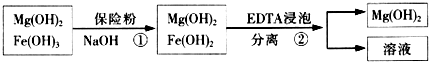
(3)步骤①中加入保险粉(Na2S2O4)的作用:将氢氧化铁还原为氢氧化亚铁.
(4)已知EDTA只能与溶液中的Fe2+反应生成易溶于水的物质,不与Mg(OH)2反应.虽然Fe(OH)2难溶于水,但步骤②中随着EDTA的加入,最终能够将Fe(OH)2除去并获得纯度高的Mg(OH)2.请从沉淀溶解平衡的角度加以解释Fe(OH)2悬浊液中存在如下平衡:Fe(OH)2(s)=Fe2+(aq)+2OH-(aq)当不断滴入EDTA时,EDTA将结合Fe 2+促使平衡向右移动而使Fe(OH)2不断溶解;
Ⅳ.为研究不同分离提纯条件下所制得阻燃剂的纯度从而确定最佳提纯条件,某研究小组各取等质量的下列4组条件下制得的阻燃剂进行含铁量的测定,结果如下:
| 精制阻燃剂的条件 | 阻燃剂铁含量 | |||
| 序号 | 提纯体系温度/℃ | 加入EDTA质量/g | 加入保险粉质量/g | W(Fe)/(10-4g) |
| 1 | 40 | 0.05 | 0.05 | 7.63 |
| 2 | 40 | 0.05 | 0.10 | 6.83 |
| 3 | 60 | 0.05 | 0.10 | 6.83 |
| 4 | 60 | 0.10 | 0.10 | 6.51 |
①40℃②60℃③EDTA质量为0.05g④EDTA质量为0.10g ⑤保险粉质量为0.05g ⑥保险粉质量为0.10g
A.①③⑤B.②④⑥C.①④⑥D.②③⑤
 ,
,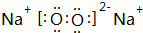 ,用电子式表示C2B的形成过程
,用电子式表示C2B的形成过程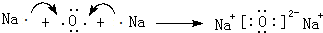
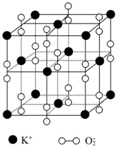 如图所示是钾、氧两元素形成的一种晶体的一个晶胞(晶体中最小的重复单元).晶体中氧的化合价可看作是部分为0价,部分为-2价.
如图所示是钾、氧两元素形成的一种晶体的一个晶胞(晶体中最小的重复单元).晶体中氧的化合价可看作是部分为0价,部分为-2价.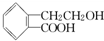 ,它可通过不同化学反应分别制得B、C和D三种物质.
,它可通过不同化学反应分别制得B、C和D三种物质.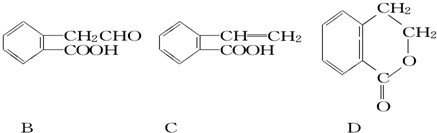
 .
.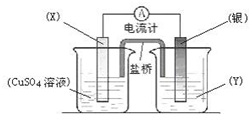 依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.
依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示. (写结构简式).
(写结构简式).