题目内容
13.已知A、B、C、D、E是短周期中的五种非金属元素,它们的原子序数依次增大.A元素原子形成的离子核外电子数为零,C、D在元素周期表中处于相邻的位置,B原子的最外层电子数是内层电子数的2倍.E元素与D元素同主族;E的单质为黄色固体,易溶于二硫化碳.(1)请写出元素符号:BC DO.
(2)画出E的阴离子的结构示意图
 .
.(3)用电子式表示钠与D形成原子个数为2:1的化合物的形成过程:
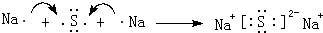 .
.
分析 A、B、C、D、E是短周期中的5种非金属元素,它们的原子序数依次增大.A元素原子形成的离子核外电子数为零,则A为H元素;B原子的最外层电子数是内层电子数的2倍,原子只能有2个电子层,最外层电子数为4,故B为碳元素;E的单质为黄色晶体,易溶于二硫化碳,则E为S元素;E元素与D元素同主族,则D为O元素;C、D在元素周期表中处于相邻的位置,且D的原子序数大,则C为N元素,据此解答.
解答 解:A、B、C、D、E是短周期中的5种非金属元素,它们的原子序数依次增大.A元素原子形成的离子核外电子数为零,则A为H元素;B原子的最外层电子数是内层电子数的2倍,原子只能有2个电子层,最外层电子数为4,故B为碳元素;E的单质为黄色晶体,易溶于二硫化碳,则E为S元素;E元素与D元素同主族,则D为O元素;C、D在元素周期表中处于相邻的位置,且D的原子序数大,则C为N元素.
(1)由上述分析可知,B为C元素、D为O元素,故答案为:C;O;
(2)E的阴离子为S2-,离子结构示意图: ,故答案为:
,故答案为: ;
;
(3)钠与D形成原子个数为2:1的化合物为Na2S,用电子式表示形成过程: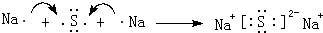 ,
,
故答案为: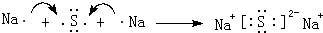 .
.
点评 本题考查结构性质位置关系应用,难度不大,推断元素为解题关键,有利于基础知识的巩固,掌握用电子式表示物质或化学键形成.

练习册系列答案
相关题目
3.相同温度相同物质的量浓度的六种溶液:①NaHCO3 ②CH3COONa ③NaOH ④Ba(OH)2 ⑤NaHSO4按pH值由大到小的顺序是( )
| A. | ⑤②①④③ | B. | ⑤①②③④ | C. | ④③②①⑤ | D. | ④③①②⑤ |
4.1 mol某链烃最多能和2 mol氯化氢发生加成反应,生成氯代烷1 mol,该氯代烷能和6 mol氯气发生取代反应,生成只含碳元素和氯元素的氯代烃,该烃可能是( )
| A. | 丙烯 | B. | 丙炔 | C. | 1-丁炔 | D. | 1,3-丁二烯 |
1.下列有关化学用语或说法正确的是( )
| A. | 氯离子的结构示意图: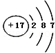 | |
| B. | 18g18O2中含有2mol氧原子 | |
| C. | Ca2+和Ca是同种元素,且性质相似 | |
| D. | NaHCO3的电离方程式:NaHCO3=Na++HCO3- |
8.有机物 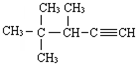 的系统名称为( )
的系统名称为( )
 的系统名称为( )
的系统名称为( )| A. | 2,2,3一三甲基一1-戊炔 | B. | 3,4,4一三甲基一l一戊炔 | ||
| C. | 3,4,4一三甲基-2一戊炔 | D. | 2,2,3一三甲基一4一戊炔 |
18.断肠草(Gelsemium)为中国古代九大毒药之一,据记载能“见血封喉”,现代查明它是葫蔓藤科植物葫蔓藤,其中的毒素很多,下列是分离出来的四种毒素的结构式,下列推断错误的是( )
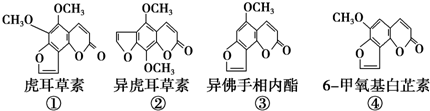

| A. | ①与②、③与④分别互为同分异构体 | |
| B. | 等物质的量的②、④分别在足量氧气中完全燃烧,前者消耗氧气比后者多 | |
| C. | ①、②、③、④均能与氢氧化钠溶液反应 | |
| D. | ①、④互为同系物 |
5.下列气体中,既能用浓硫酸也能用固体NaOH干燥的是( )
| A. | N2 | B. | SO2 | C. | NH3 | D. | Cl2 |
2.把铁和铜的混合物放入稀硝酸中,反应后过滤,滤出的固体物质投入盐酸中无气体放出,则滤液中一定含有的是( )
| A. | Fe(NO3)2 | B. | Cu(NO3)2 | C. | Fe(NO3)3 | D. | HNO3 |
3.下列物质既能与稀硫酸反应,又有跟氢氧化钠溶液反应的是( )
①NaHCO3 ②Na2CO3 ③Al2O3 ④Al(OH)3 ⑤Al.
①NaHCO3 ②Na2CO3 ③Al2O3 ④Al(OH)3 ⑤Al.
| A. | ③④ | B. | ②④⑤ | C. | ①③④⑤ | D. | 全部 |