题目内容
1.下列有关化学用语或说法正确的是( )| A. | 氯离子的结构示意图: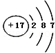 | |
| B. | 18g18O2中含有2mol氧原子 | |
| C. | Ca2+和Ca是同种元素,且性质相似 | |
| D. | NaHCO3的电离方程式:NaHCO3=Na++HCO3- |
分析 A.氯离子的最外层达到8电子稳定结构;
B.该氧原子的摩尔质量为18g/mol,根据n=$\frac{m}{M}$计算氧原子的物质的量‘
C.钙离子性质稳定,钙原子具有较强还原性;
D.碳酸氢钠电离出钠离子和碳酸氢根离子.
解答 解:A. 为氯原子结构示意图,氯离子最外层达到8电子稳定结构,故A错误;
为氯原子结构示意图,氯离子最外层达到8电子稳定结构,故A错误;
B.18g18O2中含有氧原子的物质的量为:$\frac{18g}{18g/mol}$=1mol,故B错误;
C.Ca2+和Ca是同种元素,但是其结构不相同,钙离子性质稳定,钙原子具有较强还原性,故C错误;
D.碳酸氢钠为强电解质,其电离方程式为:NaHCO3=Na++HCO3-,故D正确;
故选D.
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及离子结构示意图、电离方程式、物质的量计算等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
11.下列反应的离子方程式正确的是( )
| A. | 石英与烧碱溶液共热:SiO2+2OH-$\frac{\underline{\;\;△\;\;}}{\;}$SiO32-+H2O | |
| B. | 在氯化铝溶液中滴加过量的氨水:Al3++4OH-=[Al(OH)4]- | |
| C. | 在氢氧化钠溶液中通入过量的CO2:2OH-+CO2=CO32-+H2O | |
| D. | 稀硫酸与氢氧化钡溶液反应H++SO42-+Ba2++OH-=BaSO4↓+H2O |
9.分析下列各项结构的规律,按此规律排布第8项的分子式应为( )
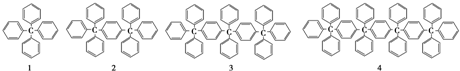

| A. | C158H118 | B. | C158H116 | C. | C160H116 | D. | C160H118 |
16.下列各项表述正确的是( )
| A. | 水分子的结构式是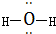 | |
| B. | NaCl的电子式为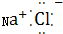 | |
| C. | 23Na37Cl中质子数和中子数之比是7:8 | |
| D. | 三氟化氮的电子式为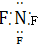 |
6.短周期元素A、B、C在元素周期表中所处的位置如表所示.A、B、C三种元素原子的质子数之和为32,D元素原子的最外层电子数为次外层电子数的2倍.则下列说法正确的是( )
| A | C | |
| B |
| A. | A、B、C三元素的气态氢化物溶于水均显酸性 | |
| B. | A、B两种元素的气态氢化物均能与它们的最高价氧化物对应的水化物发生反应,且反应类型相同 | |
| C. | C在周期表中的位置为第二周期第ⅦA族,最高价为+7价 | |
| D. | B02是酸性氧化物,AO2不是酸性氧化物 |
10.设想你采集了某星球上十种元素单质的样品,为了确定这些元素的相对位置以便系统地进行研究,你设计了一些实验并得到下列结果:
按照元素性质的周期性递变规律,试确定以上十种元素的相对位置,将其余五种元素填入下表:
| 单质 | A | B | C | D | E | F | G | H | I | J |
| 熔点(℃ | -150 | 550 | 160 | 210 | -50 | 370 | 450 | 300 | 260 | 250 |
| 与水反应 | ∨ | ∨ | ∨ | ∨ | ||||||
| 与酸反应 | ∨ | ∨ | ∨ | ∨ | ∨ | ∨ | ||||
| 与氧气反应 | ∨ | ∨ | ∨ | ∨ | ∨ | ∨ | ∨ | ∨ | ||
| 不发生化学反应 | ∨ | ∨ | ||||||||
| 相对于A元素的原子质量 | 1.0 | 8.0 | 15.6 | 17.1 | 23.8 | 31.8 | 20.0 | 29.6 | 3.9 | 18.0 |
| A | ||||||||||
| I | B | |||||||||
| J | ||||||||||
| H | ||||||||||
11.对图两种化合物的结构或性质描述错误的是( )
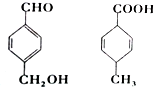

| A. | 均可以发生加成和取代反应 | |
| B. | 均能使酸性高锰酸钾溶液褪色 | |
| C. | 互为同分异构体 | |
| D. | 既能用红外光谱区分,也可以用核磁共振氢谱区分 |
 .
.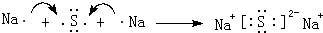 .
.