��Ŀ����
13����X��Y��Z 3��Ԫ�أ�X���л��������бغ���Ԫ�أ�Y�ǵؿ��ﺬ������Ԫ�أ�Z��������С��Ԫ�أ�X�� Z��ϵ���Ļ�����A�п�ȼ�ԣ�X��Y��Z����Ԫ�ؽ�ϵĻ�����B������ʵ���Ҽ��ȵ�ȼ�ϣ�B�����Ը��������Һ��������C����1��д��X��Y��Z��Ԫ�ط��ţ�XC��YO��ZH��
��2��д��A��B��C�Ľṹ��ʽ��ACH4��BC2H5OH��CCH3COOH��
��3����ͭ�������Ҽ���������B��������Ӧ�ķ���ʽ��2C2H5OH+O2$��_{��}^{Cu}$2CH3CHO+2H2O��
��B��C��Ũ���������������������·�Ӧ���ɵ��л��������Ϊ����������
���� X���л��������бغ���Ԫ�أ���XΪCԪ�أ�Y�ǵؿ��ﺬ������Ԫ�أ���YΪOԪ�أ�Z��������С��Ԫ�أ���ZΪHԪ�أ�X��Z��ϵ���Ļ�����A�п�ȼ�ԣ�AΪCH4��X��Y��Z����Ԫ�ؽ�ϵĻ�����B������ʵ���Ҽ��ȵ�ȼ�ϣ���֪BΪC2H5OH��B�����Ը��������Һ��������C��CΪCH3COOH���Դ������
��� �⣺X���л��������бغ���Ԫ�أ���XΪCԪ�أ�Y�ǵؿ��ﺬ������Ԫ�أ���YΪOԪ�أ�Z��������С��Ԫ�أ���ZΪHԪ�أ�X��Z��ϵ���Ļ�����A�п�ȼ�ԣ�AΪCH4��X��Y��Z����Ԫ�ؽ�ϵĻ�����B������ʵ���Ҽ��ȵ�ȼ�ϣ���֪BΪC2H5OH��B�����Ը��������Һ��������C��CΪCH3COOH��
��1��������������֪��X��Y��Z�ֱ�ΪC��O��H���ʴ�Ϊ��C��O��H��
��2��������������֪��A��B��C�ֱ�ΪCH4��C2H5OH��CH3COOH���ʴ�Ϊ��CH4��C2H5OH��CH3COOH��
��3����ͭ�������Ҽ���������B��������Ӧ�ķ���ʽΪ2C2H5OH+O2$��_{��}^{Cu}$2CH3CHO+2H2O���ʴ�Ϊ��2C2H5OH+O2$��_{��}^{Cu}$2CH3CHO+2H2O��
��B��C��Ũ���������������������·�Ӧ���ɵ��л��������Ϊ�����������ʴ�Ϊ������������
���� ���⿼���л�����ƶϣ�Ϊ��Ƶ���㣬���ճ������л��P���ʡ��ת��Ϊ���Ĺؼ������ط������ƶ������Ŀ��飬ע���л���Ĺ����������ʣ���Ŀ�ѶȲ���

 Ӧ�����������Ĵ���ѧ������ϵ�д�
Ӧ�����������Ĵ���ѧ������ϵ�д�| A�� | ����ͼױ��ж����м����ױ����Ա�����KMnO4��Һ�����ɱ����ᣬ�����鲻�ܱ���������˵�������Բ���������Ӱ�� | |
| B�� | ����Ũ���ᡢŨ����������100-110��������ɶ������������ױ���1000ʱ���������������ױ���˵�������Լ�������Ӱ�� | |
| C�� | �������֣��״���ˮ��Һ���ǻ�����������������걾 | |
| D�� | ��ȥ���л���������ױ��ɼ�������������KMnO4��Һ��Ȼ���Һ���� |
| ���� | Fe��OH��2 | Cu��OH��2 | Fe��OH��3 |
| Ksp/25�� | 8.0��10-16 | 2.2��10-20 | 4.0��10-38 |
| ��ȫ����ʱ��pH��Χ | ��9.6 | ��6.4 | ��3.4 |
| A�� | ��û����Һ����μ���NaOH��Һ�����ȿ������ɫ���� | |
| B�� | ����Һ��[SO42-]����[Cu2+]+[Fe2+]+[Fe3+]����5��4����[SO42-]��ʾSO42-���ʵ���Ũ�� �� | |
| C�� | �����Һ�м���������ˮ��������pH��3.4���ˣ��ɻ�ô�����CuSO4��Һ | |
| D�� | ��pH=4����Һ��Fe3+���ܴ������� |
��һ��N2O5��һ�������������������ʺ��Ʊ��ܵ����ǵĹ�ע��
һ���¶��£��ں����ܱ�������N2O5�ɷ������з�Ӧ��2N2O5��g��?4NO2��g��+O2��g����H��0
��1����Ӧ�ﵽƽ�������ͨ��һ������������N2O5��ת���ʽ����������������С�����䡱����
��2���±�Ϊ��Ӧ��T1�¶��µIJ���ʵ�����ݣ�
| t/s | 0 | 500 | 1000 |
| c��N2O5/mol/L�� | 5.00 | 3.50 | 2.50 |
��3����T2�¶��£���Ӧ1000sʱ���N2O5��Ũ��Ϊ3.00mol/L����T2��T1�����������������=������
��������ҵ�����ؾ�ʯ����Ҫ�ɷ�ΪBaSO4���Ʊ�BaCl2
��1��BaSO4��̼�ڸ����·�Ӧ����һ����̼���������÷�Ӧ��ÿ1mol̼����CO��Ҫ����142.8kJ���������˷�Ӧ���Ȼ�ѧ����ʽΪBaSO4��s��+4C��s���T4CO��g��+BaS��s����H=+571.2kJ/mol��
��2����BaCl2��Һ�м���AgNO3��KBr�������ֳ�������ʱ��$\frac{c��B{r}^{-}��}{c��C{l}^{-}��}$=2.7��10-3����Ksp��AgBr��=5.4��10-13��Ksp��AgCl��=2.0��10-10��
��3����NaOH��Һ����H2S�������ɵ����ʵ�����Na2S��NaHS������Һ�и�����Ũ���ɴ�С��˳��Ϊc��Na+����c��HS-����c��S2-����c��OH-����c��H+����
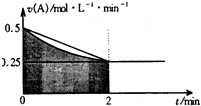 ij��Һ�з�����Ӧ��A�T2B+C��A�ķ�Ӧ����v��A����ʱ��t��ͼ����ͼ��ʾ������Һ�����Ϊ2L������ʼʱֻ����A���ʣ�����˵��������ǣ�������
ij��Һ�з�����Ӧ��A�T2B+C��A�ķ�Ӧ����v��A����ʱ��t��ͼ����ͼ��ʾ������Һ�����Ϊ2L������ʼʱֻ����A���ʣ�����˵��������ǣ�������| A�� | ͼ����Ӱ���ֵ������ʾ0-2min��A�����ʵ���Ũ�ȵļ�Сֵ | |
| B�� | ��Ӧ��ʼ��ǰ2min��A��ƽ����Ӧ����С��0.375mol•L-1•min-1 | |
| C�� | ��2minʱ��A�����ʵ�����Сֵ����0.5mol��1mol֮�� | |
| D�� | ��2minʱ��c��B������1mol•L-1 ��1.5mol•L-1 ֮�� |
| t�� | 700 | 800 | 850 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
��1���÷�ӦΪ���ȷ�Ӧ������ȡ����ȡ�����
��2�����жϸ÷�Ӧ�Ƿ�ﵽ��ѧƽ��״̬��������BC����ѡ�۷֣���
A��������ѹǿ���� B����������� c��CO������
C��������H2��=���棨H2O�� D��c��CO2��=c��CO��
��3��850��ʱ������һ�ݻ��ɱ���ܱ�������ͬʱ����1.0molCO��3.0molH2O��1.0molCO2��xmolH2����
�ٵ�x=5.0ʱ������ƽ�����淴Ӧ�������Ӧ�������淴Ӧ������ǡ��ƽ�⡱��������У�
����Ҫʹ������Ӧ��ʼʱ������Ӧ������У���xӦ�����������0��x��3��
��4����850��ʱ������x=5.0mol��x=6.0mol���������ʵ�Ͷ�ϲ��䣬��������Ӧ�ﵽƽ����H2����������ֱ�Ϊa%��b%����a�� b �����������������=������
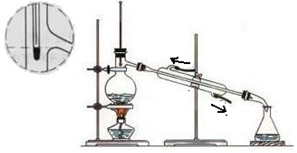
| A�� | ����ˮ�Ľ����ڷ�����ȷ | B�� | Ӧѡ��20 mL��������ƿ | ||
| C�� | �¶ȼ�Һ��Ӧ���ڻ��Һ�� | D�� | ��ƿ���ռ������Ǽױ� |
 ��Z��ԭ�ӽṹʾ��ͼΪ
��Z��ԭ�ӽṹʾ��ͼΪ ��
��