题目内容
8.下列叙述正确的是( )| A. | 浓硫酸具有强氧化性,稀硫酸无氧化性 | |
| B. | 浓硫酸在常温下可迅速与铜片反应放出二氧化硫气体 | |
| C. | 浓硫酸在常温下能够使铁、铝形成氧化膜而钝化 | |
| D. | 浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体 |
分析 A.稀硫酸具有弱氧化性;
B.常温下,浓硫酸与铜不反应;
C.常温下,浓硫酸具有强氧化性能使Fe、Al钝化;
D.浓硫酸具有吸水性,是一种干燥剂,不能干燥碱性气体和还原性气体.
解答 解:A.稀硫酸具有氧化性,可被还原生成氢气,故A错误;
B.常温下,浓硫酸与铜不反应,在加热条件下Cu与浓硫酸反应生成二氧化硫,故B错误;
C.常温下,浓硫酸具有强氧化性能使Fe、Al钝化,在金属的表面形成致密的氧化膜,故C正确;
D.浓硫酸具有吸水性,是一种干燥剂,不能干燥碱性气体和还原性气体,所以不能够干燥氨气等气体,故D错误.
故选C.
点评 本题综合考查浓硫酸的性质,侧重基础知识的理解和运用的考查,注意把握浓硫酸的特点以及与稀硫酸的区别,难度不大.

练习册系列答案
相关题目
18.五颜六色的颜色变化增添了化学的魅力,下列有关反应的颜色叙述正确的是( )
①新制氯水久置后→浅黄绿色消失;②淀粉溶液遇单质碘→蓝色;
③溴化银见光分解→银白色;④Na2CO3溶液中滴加酚酞→红色;
⑤鸡蛋白溶液遇浓硝酸→黄色;⑥碘化银的悬浊液中加入硫化钠晶体,振荡后变黑.
①新制氯水久置后→浅黄绿色消失;②淀粉溶液遇单质碘→蓝色;
③溴化银见光分解→银白色;④Na2CO3溶液中滴加酚酞→红色;
⑤鸡蛋白溶液遇浓硝酸→黄色;⑥碘化银的悬浊液中加入硫化钠晶体,振荡后变黑.
| A. | ①②③④⑤ | B. | ②③④⑤⑥ | C. | ①②④⑤⑥ | D. | ①③④⑤⑥ |
19.要除去碳酸钠固体中的碳酸氢钠,最好的方法是( )
| A. | 加热 | B. | 加入氢氧化钠 | C. | 加入氯化钙 | D. | 通入CO2 |
16.有关化学用语表达正确的是( )
| A. | 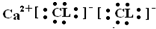 | |
| B. | C1-的结构示意图: | |
| C. | ${\;}_{46}^{102}$Pd和${\;}_{46}^{103}$Pd互为同位素 | |
| D. | 过氧化氢电子式: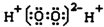 |
13.一定温度下,某一密闭恒容的容器内有可逆反应:A(g)+3B(g)?2C(g).该反应进行到一定限度后达到了化学平衡,该化学平衡的标志是( )
| A. | C物质的生成速率和A的生成速率相等 | |
| B. | 容器内气体的压强不再随时间而改变 | |
| C. | 单位时间内生成a mol物质A,同时生成3a mol物质B | |
| D. | A、B、C三种物质的分子数之比为1:3:2 |
20.在容积为672mL的烧瓶里充满NO、NO2(气体所处环境均在标准状况下)的混合气体,将其倒立在水槽里,去塞后再通入280mL氧气,恰好完全反应,且水充满烧瓶(气体体积都已折合为标准状况),下列有关叙述中正确的是( )
| A. | 总反应为NO+NO2+O2+H2O═2HNO3 | |
| B. | 总反应为2NO+10NO2+4O2+6H2O═12HNO3 | |
| C. | 生成硝酸的物质的量浓度接近0.03 mol/L | |
| D. | 生成硝酸的物质的量浓度约为0.045 mol/L |
17.如图是氢氧燃料电池构造示意图.关于该电池的说法不正确的是( )


| A. | a极是负极 | B. | 供电时的总反应为2H2+O2═2H2O | ||
| C. | 电子由b通过灯泡流向a | D. | 氢氧燃料电池是环保电池 |