题目内容
17.如图是氢氧燃料电池构造示意图.关于该电池的说法不正确的是( )
| A. | a极是负极 | B. | 供电时的总反应为2H2+O2═2H2O | ||
| C. | 电子由b通过灯泡流向a | D. | 氢氧燃料电池是环保电池 |
分析 氢氧燃料电池中,通入氢气的一极为电源的负极,发生氧化反应,电极反应式为H2-2e-=2H+,通入氧气的一极为原电池的正极,电极反应式为O2+4H++4e-=2H2O,原电池工作时,电子由负极经外电路流向正极.
解答 解:A、氢氧燃料电池中,H2在负极a上被氧化,O2在正极b上被还原,a极是负极,故A正确;
B、氢氧燃料电池中,H2在负极a上被氧化,O2在正极b上被还原,总反应是燃料燃烧的方程式,即:2H2+O2═2H2O,故B正确;
C、原电池工作时,电子由负极经外电路流向正极,即由a通过灯泡流向b,故C错误;
D、氢氧燃料电池的总反应为:2H2+O2=2H2O,属于环保电池,故D正确.
故选C.
点评 本题考查原电池的工作原理,题目难度不大,注意把握电极方程式的书写,特别是电解质溶液的酸碱性.

练习册系列答案
相关题目
8.下列叙述正确的是( )
| A. | 浓硫酸具有强氧化性,稀硫酸无氧化性 | |
| B. | 浓硫酸在常温下可迅速与铜片反应放出二氧化硫气体 | |
| C. | 浓硫酸在常温下能够使铁、铝形成氧化膜而钝化 | |
| D. | 浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体 |
12.下列说法中正确的是( )
| A. | 离子键就是阴、阳离子间的静电引力 | |
| B. | 所有金属元素与所有非金属元素间都能形成离子键 | |
| C. | 钠原子与氯原子结合形成离子键 | |
| D. | 在离子化合物CaCl2中,两个氯离子间也存在离子键 |
2.下列叙述中能肯定说明金属A比金属B的活泼性强的是( )
| A. | A原子最外层电子数比B原子的最外层电子数少 | |
| B. | 由金属A和金属B构成的原电池,电子由A流向B | |
| C. | 1molA从酸中置换生成的H2比1mol B从酸中置换生成的H2多 | |
| D. | 常温时,A能从酸中置换出氢,而B不能 |
9.氢化铵(NH4H)与氯化铵的结构相似,又知NH4H与水反应有氢气放出,下列叙述不正确的是( )
| A. | NH4H是离子化合物,含有离子键和共价键 | |
| B. | NH4H与水反应时,NH4H是还原剂 | |
| C. | 每反应1molNH4H,转移2mol电子 | |
| D. | NH4H投入少量的水中,有两种气体产生 |
6.下列叙述不正确的是( )
| A. | 在干旱地区植树造林时,可利用高吸水性树脂抗旱保水 | |
| B. | 硅酸钠的水溶液俗称水玻璃,是制备硅胶的原料 | |
| C. | SiO2的导电能力强,可用于制造太阳能电池板 | |
| D. | 服用阿司匹林若出现水杨酸反应,应立即停药并静脉滴注NaHCO3溶液. |
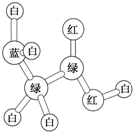 某期刊封面上的一个分子球棍模型图如图所示,图中“棍”代表单键、双键或三键,不同颜色的球代表不同元素的原子.该模型图可代表一种( )
某期刊封面上的一个分子球棍模型图如图所示,图中“棍”代表单键、双键或三键,不同颜色的球代表不同元素的原子.该模型图可代表一种( ) 化学上常用燃烧法确定有机物组成,这种方法是在电炉加热时用纯氧气氧化管内样品,根据产物的质量确定有机物的组成,图中所列装置是用燃烧法确定有机物分子式常用的装置.
化学上常用燃烧法确定有机物组成,这种方法是在电炉加热时用纯氧气氧化管内样品,根据产物的质量确定有机物的组成,图中所列装置是用燃烧法确定有机物分子式常用的装置.