题目内容
3.请你根据化学反应2AgNO3+Cu=2Ag+Cu(NO3) 2设计成原电池,画出原电池的装置图,并在图上标出正、负极材料、电解质溶液名称,电子流动的方向.写出正负电极反应式.负极Cu-2e-=Cu2+
正极Ag++e-=Ag.
分析 根据方程式,原电池中失电子的物质作负极,根据反应方程式知,Cu作负极,电解质溶液中含有得电子的Ag+,可用硝酸银溶液作电解质溶液,正极可用C,据此设计实验装置图.
解答 解:原电池中失电子的物质作负极,根据反应方程式知,Cu作负极,电解质溶液中含有得电子的Ag+,可用硝酸银溶液作电解质溶液,正极可用C,电子流动方向为负极到正极;则装置图为 ;在负极上铜失电子生成铜离子,发生氧化反应,电极反应式为Cu-2e-=Cu2+;在正极上银离子得电子生成银单质,电极反应式为Ag++e-=Ag;
;在负极上铜失电子生成铜离子,发生氧化反应,电极反应式为Cu-2e-=Cu2+;在正极上银离子得电子生成银单质,电极反应式为Ag++e-=Ag;
故答案为: ;Cu-2e-=Cu2+;Ag++e-=Ag.
;Cu-2e-=Cu2+;Ag++e-=Ag.
点评 本题考查了原电池工作原理、原电池装置图的设计,题目难度不大,注意掌握原电池工作原理,能够根据反应原理画出正确的原电池装置图.

练习册系列答案
相关题目
13.(1)二甲苯苯环上的一溴代物有六种同分异构体,这些一溴代物与生成它的对应二甲苯的熔点分别为:
熔点为234℃分子的结构简式为
(2)完全燃烧下列烃①丙烷(C3H8)、②丁烯(C4H8)、③乙烯(C2H4)、④己烷(C6H14),等物质的量的上述四种烃,耗氧量最小的为③(填写序号);等质量时,则耗氧量最大的为①(填写序号).
(3)0.2mol某烃A在氧气中完全燃烧后,生成CO2和H2O各1.2mol.试回答:
①若烃A不能使溴水褪色,但在一定条件下能与氯气发生取代反应,其一氯取代物只有一种,则烃A的结构简式为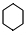 .
.
②若烃A能使溴水褪色,在催化剂作用下,与H2加成反应后生成2,2-二甲基丁烷,则烃A的名称是3,3-二甲基-1-丁烯.
(4)组成符合CnH2n-2的某种烃,分子结构中没有支链或侧链.它完全燃烧时所消耗O2的体积是同状况下该烃蒸气体积的8.5倍,由此分析回答:
①若该烃为链状二烯烃,并且与等物质的量的Br2加成后只能得到单一产物,则该烃的结构简式为CH2═CH-CH2-CH2-CH═CH2
②若该烃只能与等物质的量的Br2发生加成反应,则其结构简式为 (填任一种).
(填任一种).
| 一溴代二甲苯 | 234℃ | 206℃ | 213.8℃ | 204℃ | 214.5℃ | 205 |
| 对应的二甲苯 | -13℃ | -54℃ | -27℃ | -54℃ | -27℃ | -54℃ |

(2)完全燃烧下列烃①丙烷(C3H8)、②丁烯(C4H8)、③乙烯(C2H4)、④己烷(C6H14),等物质的量的上述四种烃,耗氧量最小的为③(填写序号);等质量时,则耗氧量最大的为①(填写序号).
(3)0.2mol某烃A在氧气中完全燃烧后,生成CO2和H2O各1.2mol.试回答:
①若烃A不能使溴水褪色,但在一定条件下能与氯气发生取代反应,其一氯取代物只有一种,则烃A的结构简式为
 .
.②若烃A能使溴水褪色,在催化剂作用下,与H2加成反应后生成2,2-二甲基丁烷,则烃A的名称是3,3-二甲基-1-丁烯.
(4)组成符合CnH2n-2的某种烃,分子结构中没有支链或侧链.它完全燃烧时所消耗O2的体积是同状况下该烃蒸气体积的8.5倍,由此分析回答:
①若该烃为链状二烯烃,并且与等物质的量的Br2加成后只能得到单一产物,则该烃的结构简式为CH2═CH-CH2-CH2-CH═CH2
②若该烃只能与等物质的量的Br2发生加成反应,则其结构简式为
 (填任一种).
(填任一种).
14.NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 标准状况下,11.2 L的戊烷所含的分子数为0.5NA | |
| B. | 30 g乙烷所含共用电子对数目为6NA | |
| C. | 标准状况下,11.2 L二氯甲烷所含分子数为0.5NA | |
| D. | 现有C2H4、C3H6、C4H8的混合气体共14 g,其原子数为3NA |
11.对于反应A(g)+3B(g)?2C(s)+D(g),用下列各数据表示不同条件下的反应速度,其中反应进行得最快的是( )
| A. | v(A)=0.01mol•L-1s-1 | B. | v(B)=0.02mol•L-1s-1 | ||
| C. | v(C)=1.50mol•L-1min-1 | D. | v(D)=0.50mol•L-1min-1 |
18.把1体积CH4和4体积Cl2组成的混合气体充入大试管中,将此试管倒立在盛有饱和食盐水的水槽里,放在光亮处,试推测可观察到的现象是( )
①黄绿色逐渐消失
②试管壁上有小油珠出现
③水位在试管内上升到一定高度
④水位在试管内上升至充满试管
⑤水槽内有少量晶体析出.
①黄绿色逐渐消失
②试管壁上有小油珠出现
③水位在试管内上升到一定高度
④水位在试管内上升至充满试管
⑤水槽内有少量晶体析出.
| A. | ①③ | B. | ①②③ | C. | ①②③⑤ | D. | ①②④⑤ |
8.下列叙述正确的是( )
| A. | 浓硫酸具有强氧化性,稀硫酸无氧化性 | |
| B. | 浓硫酸在常温下可迅速与铜片反应放出二氧化硫气体 | |
| C. | 浓硫酸在常温下能够使铁、铝形成氧化膜而钝化 | |
| D. | 浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体 |
12.下列说法中正确的是( )
| A. | 离子键就是阴、阳离子间的静电引力 | |
| B. | 所有金属元素与所有非金属元素间都能形成离子键 | |
| C. | 钠原子与氯原子结合形成离子键 | |
| D. | 在离子化合物CaCl2中,两个氯离子间也存在离子键 |
