题目内容
18.五颜六色的颜色变化增添了化学的魅力,下列有关反应的颜色叙述正确的是( )①新制氯水久置后→浅黄绿色消失;②淀粉溶液遇单质碘→蓝色;
③溴化银见光分解→银白色;④Na2CO3溶液中滴加酚酞→红色;
⑤鸡蛋白溶液遇浓硝酸→黄色;⑥碘化银的悬浊液中加入硫化钠晶体,振荡后变黑.
| A. | ①②③④⑤ | B. | ②③④⑤⑥ | C. | ①②④⑤⑥ | D. | ①③④⑤⑥ |
分析 ①新制氯水含有次氯酸,不稳定;
②淀粉遇碘变蓝色;
③溴化银见光分解生成银;
④Na2CO3水解呈碱性;
⑤鸡蛋白与浓硝酸发生颜色反应;
⑥碘化银的溶解度比硫化银大.
解答 解:①新制氯水含有次氯酸,不稳定,见光易分解,故正确;
②淀粉遇碘变蓝色,故正确;
③溴化银见光分解生成银,银粉为黑色,故错误;
④Na2CO3水解呈碱性,滴加酚酞变红色,故正确;
⑤鸡蛋白与浓硝酸发生颜色反应,蛋白质变色黄色,故正确;
⑥碘化银的溶解度比硫化银大,碘化银可转化为硫化银,故正确.
故选C.
点评 本题多角度考查元素化合物知识,为高频考点,侧重于学生的双基知识的考查,有利于培养学生良好的科学素养,提高学习的积极性,难度不大.

练习册系列答案
 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案
相关题目
7.下列说法正确的是( )
| A. | 铝、铁、铜相比较,铜元素在自然界中的含量最低、铁元素含量最高 | |
| B. | Al2O3、MgO可用作高温材料,二氧化硅是生产光纤制品的基本原料 | |
| C. | 工业上采用电解熔融态Al2O3、MgO的方法冶炼Al、Mg | |
| D. | 用纯碱制玻璃、用铁矿石炼铁、用氨制碳酸铵都会产生温室气体 |
9.常温下,用0.1000mol•L-1NaOH溶液滴定20.00mL 0.1000mol•L-1CH3 COOH溶液所得滴定曲线如图.下列说法正确的是( )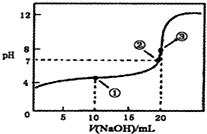

| A. | ①处水的电离程度大于②处水的电离程度 | |
| B. | ②处加入的NaOH溶液恰好将CH3COOH中和 | |
| C. | ③处所示溶液:c(N+)<c(CH3COO-) | |
| D. | 滴定过程中可能出现:c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-) |
6.1mol某烃能与2mol HCl完全加成,其产物最多能被8mol Cl2完全取代,则原烃可为( )
| A. | 乙炔 | B. | 1-丁炔 | C. | 1-丙炔 | D. | 环丁烯 |
13.(1)二甲苯苯环上的一溴代物有六种同分异构体,这些一溴代物与生成它的对应二甲苯的熔点分别为:
熔点为234℃分子的结构简式为
(2)完全燃烧下列烃①丙烷(C3H8)、②丁烯(C4H8)、③乙烯(C2H4)、④己烷(C6H14),等物质的量的上述四种烃,耗氧量最小的为③(填写序号);等质量时,则耗氧量最大的为①(填写序号).
(3)0.2mol某烃A在氧气中完全燃烧后,生成CO2和H2O各1.2mol.试回答:
①若烃A不能使溴水褪色,但在一定条件下能与氯气发生取代反应,其一氯取代物只有一种,则烃A的结构简式为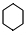 .
.
②若烃A能使溴水褪色,在催化剂作用下,与H2加成反应后生成2,2-二甲基丁烷,则烃A的名称是3,3-二甲基-1-丁烯.
(4)组成符合CnH2n-2的某种烃,分子结构中没有支链或侧链.它完全燃烧时所消耗O2的体积是同状况下该烃蒸气体积的8.5倍,由此分析回答:
①若该烃为链状二烯烃,并且与等物质的量的Br2加成后只能得到单一产物,则该烃的结构简式为CH2═CH-CH2-CH2-CH═CH2
②若该烃只能与等物质的量的Br2发生加成反应,则其结构简式为 (填任一种).
(填任一种).
| 一溴代二甲苯 | 234℃ | 206℃ | 213.8℃ | 204℃ | 214.5℃ | 205 |
| 对应的二甲苯 | -13℃ | -54℃ | -27℃ | -54℃ | -27℃ | -54℃ |

(2)完全燃烧下列烃①丙烷(C3H8)、②丁烯(C4H8)、③乙烯(C2H4)、④己烷(C6H14),等物质的量的上述四种烃,耗氧量最小的为③(填写序号);等质量时,则耗氧量最大的为①(填写序号).
(3)0.2mol某烃A在氧气中完全燃烧后,生成CO2和H2O各1.2mol.试回答:
①若烃A不能使溴水褪色,但在一定条件下能与氯气发生取代反应,其一氯取代物只有一种,则烃A的结构简式为
 .
.②若烃A能使溴水褪色,在催化剂作用下,与H2加成反应后生成2,2-二甲基丁烷,则烃A的名称是3,3-二甲基-1-丁烯.
(4)组成符合CnH2n-2的某种烃,分子结构中没有支链或侧链.它完全燃烧时所消耗O2的体积是同状况下该烃蒸气体积的8.5倍,由此分析回答:
①若该烃为链状二烯烃,并且与等物质的量的Br2加成后只能得到单一产物,则该烃的结构简式为CH2═CH-CH2-CH2-CH═CH2
②若该烃只能与等物质的量的Br2发生加成反应,则其结构简式为
 (填任一种).
(填任一种).
3.下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 含大量Fe3+的溶液中:Na+、Mg2+、SO42-、SCN- | |
| B. | 使甲基橙呈红色的溶液:NO3-、Ba2+、AlO2-、Cl- | |
| C. | 与铝反应产生大量氢气的溶液:Na+、K+、CO32-、NO3- | |
| D. | pH=12的溶液:CO32-、Cl-、K+、F- |
10.下列有关试验的做法不正确的是( )
| A. | 检验NH4+时,往试样中加入NaOH溶液,微热,用湿润的蓝色石蕊试纸检验逸出的气体 | |
| B. | 用加热分解的方法区分碳酸钠和碳酸氢钠两种固体 | |
| C. | 配置0.1000 mol•L-1氢氧化钠溶液时,将液体转移到容量瓶中需用玻璃棒引流 | |
| D. | 分液时,分液漏斗的上层液体应由上口倒出 |
8.下列叙述正确的是( )
| A. | 浓硫酸具有强氧化性,稀硫酸无氧化性 | |
| B. | 浓硫酸在常温下可迅速与铜片反应放出二氧化硫气体 | |
| C. | 浓硫酸在常温下能够使铁、铝形成氧化膜而钝化 | |
| D. | 浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体 |
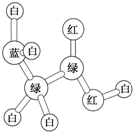 某期刊封面上的一个分子球棍模型图如图所示,图中“棍”代表单键、双键或三键,不同颜色的球代表不同元素的原子.该模型图可代表一种( )
某期刊封面上的一个分子球棍模型图如图所示,图中“棍”代表单键、双键或三键,不同颜色的球代表不同元素的原子.该模型图可代表一种( )