题目内容
14.用${\;}_{Z}^{A}$X表示原子:(1)阳离子AXn+中共有x个电子,则该阳离子中含有的中子数目为A-x-n.
(2)A2-原子核内有x个中子,其质量数为m,则n g A2-所含电子的物质的量为$\frac{n}{m}$(m-x+2)mol.
分析 (1)在阳离子中,核电荷数=质子数=核外电子数+所带电荷数,中子数=质量数-质子数,据此分析;
(2)元素A的质量数为m,A2-离子的原子核内有x个中子,则A的质子数为m-x,所以A2-中核外电子数为m-x+2,计算出n克A2-离子的物质的量,则可计算电子个数.
解答 解:(1)根据在阳离子中:核电荷数=质子数=核外电子数+所带电荷数,即核电荷数=质子数=x+n,又根据中子数=质量数-质子数=A-(x+n),
故答案为:A-x-n;
(2)元素A的质量数为m,A2-离子的原子核内有x个中子,则A的质子数为m-x,所以A2-中核外电子数为:m-x+2,
n(A2-)=$\frac{n}{m}$mol,则n克A2-离子中包含电子个数是$\frac{n}{m}$mol×(m-x+2)×NA/mol=$\frac{n}{m}$(m-x+2)mol;
故答案为:$\frac{n}{m}$(m-x+2).
点评 本题考查了原子符号的含义、原子(或离子)中微粒之间的关系、物质的量的有关计算,明确原子(或离子)中微粒之间的关系是解本题关键,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
20.根据乙烯和乙酸的结构与性质,推测CH2═CH-COOH能发生的反应有( )
①加成反应 ②取代反应 ③氧化反应.
①加成反应 ②取代反应 ③氧化反应.
| A. | ①② | B. | ②③ | C. | ①③ | D. | ①②③ |
2.下列情况会破坏共价键的是( )
| A. | 氯化钠加热融化 | B. | 氢氧化钠溶于水 | ||
| C. | 氯化氢气体溶于水 | D. | 酒精溶于水 |
3.在一定的温度下,向CH3COOH溶液里加水稀释,下列组数据变大的是
①c(H+)的物质的量浓度 ②c(OH-)的物质的量浓度 ③$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$ ④水的浓度⑤c(H+)•c(OH-)( )
①c(H+)的物质的量浓度 ②c(OH-)的物质的量浓度 ③$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$ ④水的浓度⑤c(H+)•c(OH-)( )
| A. | ①④ | B. | ②③ | C. | ③④ | D. | ②⑤ |
4.甲、乙、丙都是短周期元素,其中甲、乙两元素原子的最外层电子数分别是次外层电子数的2倍和3倍,丙元素原子K层和M层电子数之积与L层的电子数相同.则下列判断正确的是( )
| A. | 乙元素的族序数比甲元素的族序数小 | |
| B. | 甲、丙元素最高价氧化物对应水化物的酸性强弱顺序为:甲<丙 | |
| C. | 原子半径由大到小的顺序为:丙>甲>乙 | |
| D. | 含乙元素的化合物数目比含甲或丙元素的化合物数目多 |
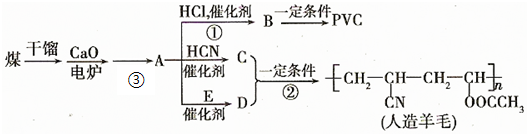
 ,CCH2═CHCN.
,CCH2═CHCN.