题目内容
SO2、NO是大气污染物.吸收SO2 和NO,获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素):

(1)装置Ⅰ中生成HSO3-的离子方程式为 .
(2)含硫各微粒(H2SO3、HSO3-和SO32-)存在于SO2与NaOH溶液反应后的溶液中,它们的物质的量分数X(i)与溶液pH 的关系如图1所示.

①下列说法正确的是 (填字母序号).
a.pH=8时,溶液中c(HSO3-)<c(SO32-)
b.pH=7时,溶液中c(Na+)=c(HSO3-)+c(SO32-)
c.为获得尽可能纯的NaHSO3,可将溶液的pH控制在4~5左右
②向pH=5的NaHSO3溶液中滴加一定浓度的CaCl2溶液,溶液中出现浑浊,pH降为2,用化学平衡移动原理解释溶液pH降低的原因: .
(3)装置Ⅱ中,酸性条件下,NO被Ce4+氧化的产物主要是NO3-、NO2-,写出生成NO3-的离子方程式 .
(4)装置Ⅲ的作用之一是再生Ce4+,其原理如图2所示.
①生成Ce4+的电极反应式为 .
②生成Ce4+从电解槽的 (填字母序号)口流出.
(5)已知进入装置Ⅳ的溶液中,NO2-的浓度为a g?L-1,要使1m3该溶液中的NO2-完全转化为NH4NO3,需至少向装置Ⅳ中通入标准状况下的O2 L.(用含a代数式表示,计算结果保留整数)

(1)装置Ⅰ中生成HSO3-的离子方程式为
(2)含硫各微粒(H2SO3、HSO3-和SO32-)存在于SO2与NaOH溶液反应后的溶液中,它们的物质的量分数X(i)与溶液pH 的关系如图1所示.

①下列说法正确的是
a.pH=8时,溶液中c(HSO3-)<c(SO32-)
b.pH=7时,溶液中c(Na+)=c(HSO3-)+c(SO32-)
c.为获得尽可能纯的NaHSO3,可将溶液的pH控制在4~5左右
②向pH=5的NaHSO3溶液中滴加一定浓度的CaCl2溶液,溶液中出现浑浊,pH降为2,用化学平衡移动原理解释溶液pH降低的原因:
(3)装置Ⅱ中,酸性条件下,NO被Ce4+氧化的产物主要是NO3-、NO2-,写出生成NO3-的离子方程式
(4)装置Ⅲ的作用之一是再生Ce4+,其原理如图2所示.
①生成Ce4+的电极反应式为
②生成Ce4+从电解槽的
(5)已知进入装置Ⅳ的溶液中,NO2-的浓度为a g?L-1,要使1m3该溶液中的NO2-完全转化为NH4NO3,需至少向装置Ⅳ中通入标准状况下的O2
考点:物质分离和提纯的方法和基本操作综合应用,原电池和电解池的工作原理,离子浓度大小的比较
专题:实验设计题,基本概念与基本理论
分析:(1)二氧化硫是酸性氧化物,能和强碱之间发生反应;
(2)①当溶液的pH=8时,根据图示得到溶液是亚硫酸钠和亚硫酸氢钠的混合物,根据离子浓度大小比较的方法来回答;
②NaHSO3溶液中HSO3-的电离大于水解,溶液显示酸性,根据平衡移动原理来回答;
(3)在酸性环境下,NO和Ce4+之间会发生氧化还原反应;
(4)在电解池中,阳极上发失去电子的氧化反应,阴极上发生得电子的还原反应;
(5)根据氧化还原反应中电子守恒来计算.
(2)①当溶液的pH=8时,根据图示得到溶液是亚硫酸钠和亚硫酸氢钠的混合物,根据离子浓度大小比较的方法来回答;
②NaHSO3溶液中HSO3-的电离大于水解,溶液显示酸性,根据平衡移动原理来回答;
(3)在酸性环境下,NO和Ce4+之间会发生氧化还原反应;
(4)在电解池中,阳极上发失去电子的氧化反应,阴极上发生得电子的还原反应;
(5)根据氧化还原反应中电子守恒来计算.
解答:
解:(1)二氧化硫是酸性氧化物,能和强碱氢氧化钠之间发生反应:SO2+OH-=HSO3-,NO和氢氧化钠之间不会反应,故答案为:SO2+OH-=HSO3-;
(2)①a、当溶液的pH=8时,根据图示得到溶液是亚硫酸钠和亚硫酸氢钠的混合物,离子浓度大小顺序是:c(Na+)>c(SO32-)>c(HSO3-)>c(OH-)>c(H+),c(SO32-)>c(HSO3-),故a正确;
b.pH=7时,溶液呈中性,c(H+)=c(OH-),溶液中存在电荷守恒:c(H+)+c(Na+)=c(HSO3-)+2c(SO32-)+c(OH-),故溶液中c(Na+)=c(HSO3-)+2c(SO32-),故b错误;
c.图象可知,为获得尽可能纯的NaHSO3,可将溶液的pH控制在4~5左右.故c正确;
故答案为:ac;
②NaHSO3溶液中HSO3-的电离大于水解,HSO3-?SO32-+H+,溶液显示酸性,加入CaCl2溶液后,Ca2++SO32-=CaSO3↓使电离平衡右移,
故答案为:HSO3-在溶液中存在电离平衡:HSO3-?SO32-+H+,加CaCl2溶液后,Ca2++SO32-=CaSO3↓使电离平衡右移,c(H+)增大;
(3)在酸性环境下,NO和Ce4+之间会发生氧化还原反应:NO+H2O+Ce4+=Ce3++NO2-+2H+,故答案为:NO+H2O+Ce4+=Ce3++NO2-+2H+;
(4)①电解池的阴极发生得电子的还原反应,电极反应式为:2HSO3-+4H++4e-=S2O32-+3H2O,阳极电极反应为:Ce3+-e-═Ce4+,故答案为:Ce3+-e-═Ce4+;
②在电解池中,阳极上是Ce3+失电子成为Ce4+的过程,所以生成Ce4+从电解槽的阳极上极a极流出,故答案为:a;
(5)NO2-的浓度为a g?L-1,要使1m3该溶液中的NO2-完全转化为NH4NO3,则失去电子数目是:
,设消耗标况下氧气的体积是V,则失电子数目是:
,根据电子守恒:
=
,解得V=243a,故答案为:243a.
(2)①a、当溶液的pH=8时,根据图示得到溶液是亚硫酸钠和亚硫酸氢钠的混合物,离子浓度大小顺序是:c(Na+)>c(SO32-)>c(HSO3-)>c(OH-)>c(H+),c(SO32-)>c(HSO3-),故a正确;
b.pH=7时,溶液呈中性,c(H+)=c(OH-),溶液中存在电荷守恒:c(H+)+c(Na+)=c(HSO3-)+2c(SO32-)+c(OH-),故溶液中c(Na+)=c(HSO3-)+2c(SO32-),故b错误;
c.图象可知,为获得尽可能纯的NaHSO3,可将溶液的pH控制在4~5左右.故c正确;
故答案为:ac;
②NaHSO3溶液中HSO3-的电离大于水解,HSO3-?SO32-+H+,溶液显示酸性,加入CaCl2溶液后,Ca2++SO32-=CaSO3↓使电离平衡右移,
故答案为:HSO3-在溶液中存在电离平衡:HSO3-?SO32-+H+,加CaCl2溶液后,Ca2++SO32-=CaSO3↓使电离平衡右移,c(H+)增大;
(3)在酸性环境下,NO和Ce4+之间会发生氧化还原反应:NO+H2O+Ce4+=Ce3++NO2-+2H+,故答案为:NO+H2O+Ce4+=Ce3++NO2-+2H+;
(4)①电解池的阴极发生得电子的还原反应,电极反应式为:2HSO3-+4H++4e-=S2O32-+3H2O,阳极电极反应为:Ce3+-e-═Ce4+,故答案为:Ce3+-e-═Ce4+;
②在电解池中,阳极上是Ce3+失电子成为Ce4+的过程,所以生成Ce4+从电解槽的阳极上极a极流出,故答案为:a;
(5)NO2-的浓度为a g?L-1,要使1m3该溶液中的NO2-完全转化为NH4NO3,则失去电子数目是:
| 1000a |
| 46 |
| V |
| 22.4 |
| 1000a |
| 46 |
| V |
| 22.4 |
点评:本题综合考查学生含氮元素、含硫元素物质的性质知识,注意知识的梳理和归纳是关键,难度中等.

练习册系列答案
 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案
相关题目
不具有放射性的同位素称之为稳定同位素,稳定同位素分析法近20年来在植物生理学、生态学和环境科学研究中获得广泛应用,如在陆地生态系统研究中,2H、13C、15N、18O、34S等常用作环境分析指示物,下列有关说法正确的是( )
| A、34S原子核内中子数为16 |
| B、1H216O和1H218O的相对分子质量相差2 |
| C、13C和15N原子的原子序数相差2 |
| D、2H+结合OH-的能力比1H+的更强 |
将15g金属混合物粉末投入足量稀H2SO4中,充分反应后得到11.2L H2(在标准状况下),此金属混合物可能组成是( )
| A、Zn、Ag |
| B、Cu、Fe |
| C、Al、Fe |
| D、Mg、Al |


 某学生利用如图装置探究氯气与氨气之间的反应.其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置.
某学生利用如图装置探究氯气与氨气之间的反应.其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置.

 (I)如图是某学校林老师制备NH3并进行性质实验时的改进装置.按图1把仪器安装好,称取2g固体氯化铵装入试管底部,再称取2g氢氧化钠覆盖在氯化铵上方;立即用带有滴管的塞子塞紧(滴管预先吸入约2mL浓氨水);烧杯内盛滴有酚酞试液的水:把浓氨水滴入试管里,可立即观察到试管内发生剧烈反应,有大量气泡.
(I)如图是某学校林老师制备NH3并进行性质实验时的改进装置.按图1把仪器安装好,称取2g固体氯化铵装入试管底部,再称取2g氢氧化钠覆盖在氯化铵上方;立即用带有滴管的塞子塞紧(滴管预先吸入约2mL浓氨水);烧杯内盛滴有酚酞试液的水:把浓氨水滴入试管里,可立即观察到试管内发生剧烈反应,有大量气泡.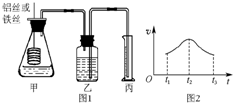 某研究小组拟用定量的方法测量Al和Fe分别与酸反应的快慢,设计了如下图1所示的装置.
某研究小组拟用定量的方法测量Al和Fe分别与酸反应的快慢,设计了如下图1所示的装置.