题目内容
9.下列各组物质中,所含分子数不相同的是( )| A. | 10g H2 和10g O2 | B. | 5.6L N2(标准状况)和11g CO2 | ||
| C. | 9g H2O 和0.5mol Br2D | D. | 224mLH2 (标准状况)和0.01mol N2 |
分析 根据N=nNA可知,若所含分子数不相同,说明二者的物质的量不相等,先根据n=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$=$\frac{V}{{V}_{m}}$分别计算出其物质的量,然后进行判断即可.
解答 解:A.氢气和氧气的摩尔质量不同,根据n=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$可知,质量相等时二者的分子数一定不相等,故A正确;
B.5.6L N2(标准状况)的物质的量为:$\frac{5.6L}{22.4L/mol}$=0.25mol,11g CO2的物质的量为:$\frac{11g}{44g/mol}$=0.25mol,二者物质的量相等,则含有的分子数相等,故B错误;
C.9g H2O的物质的量为:$\frac{9g}{18g/mol}$=0.5mol,与0.5mol Br2的物质的量相等,则二者含有的分子数相等,故C错误;
D.224mLH2 (标准状况)的物质的量为:$\frac{0.224L}{22.4L/mol}$=0.01mol,与0.01mol N2的物质的量相等,二者含有分子数相等,故D错误;
故选A.
点评 本题考查了物质的量的计算,题目难度中等,明确物质的量与摩尔质量、气体摩尔体积、阿伏伽德罗常数之间的关系为解答关键,试题培养了学生的化学计算能力.

练习册系列答案
 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案
相关题目
19.在同温同压下,A容器中的氧气和B容器中的氨所含的原子个数相同时,则A、B两容器中气体体积之比为( )
| A. | 1:2 | B. | 2:1 | C. | 2:3 | D. | 3:2 |
20.能正确表示下列化学反应的离子方程式是( )
| A. | 澄清的石灰水与稀盐酸反应 Ca(OH)2+2H+=Ca2++2H2O | |
| B. | 向硝酸银溶液中加盐酸:Ag++C1-═AgCl↓ | |
| C. | 铜片插入硝酸银溶液中 Cu+Ag+=Cu2++Ag | |
| D. | 氢氧化钡溶液与硫酸的反应 OH-+H+=H2O |
17.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 标准状态下,33.6L三氧化硫中含有硫原子的数目为1.5 NA | |
| B. | 12g石墨烯(单层石墨)中含有六元环的个数为0.5 NA | |
| C. | 50mL18.4mol•L-1浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46 NA | |
| D. | 标准状况下,6.72 L NO2与水充分反应转移的电子数目为0.1 NA |
4.下列离子方程式中书写正确的是( )
| A. | 氧化亚铁与稀盐酸反应:FeO+2H+═Fe3++H2O | |
| B. | 硫酸滴在铜片上:Cu+2H+=Cu2++H2↑ | |
| C. | 硫酸溶液和氢氧化钡溶液反应:Ba2++SO42-═BaSO4 | |
| D. | 硝酸银溶液与氯化钠溶液反应:Ag++Cl-═AgCl↓ |
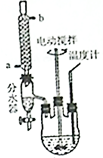 某学习小组以乙二酸(分子式:H2C2O4,结构简式:HOOC-COOH,二元弱酸,俗称草酸)和乙醇为原料制备乙二酸二乙酯,实验步骤如下:
某学习小组以乙二酸(分子式:H2C2O4,结构简式:HOOC-COOH,二元弱酸,俗称草酸)和乙醇为原料制备乙二酸二乙酯,实验步骤如下: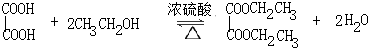 .
.