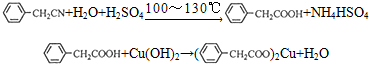题目内容
2. 某学习小组以乙二酸(分子式:H2C2O4,结构简式:HOOC-COOH,二元弱酸,俗称草酸)和乙醇为原料制备乙二酸二乙酯,实验步骤如下:
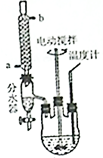
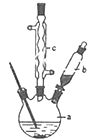
某学习小组以乙二酸(分子式:H2C2O4,结构简式:HOOC-COOH,二元弱酸,俗称草酸)和乙醇为原料制备乙二酸二乙酯,实验步骤如下:步骤一、在如图所示装置中,加入无水乙醇81g,无水草酸45g,苯200mL,浓硫酸10mL,搅拌下加热68-70℃回流共沸脱水.
步骤二、待水基本蒸完后,分离出乙醇和苯.
步骤三、所得混合液冷却后依次用水、饱和碳酸氢钠溶液洗涤,再用无水硫酸钠干燥.
步骤四、常压蒸馏,收集182-184℃的馏分,得草酸二乙醇58.4g.
根据以上实验操作,回答下列问题:
(1)草酸是一种还原性酸,能使酸性高锰酸钾溶液褪色,试写出其反应的离子方程式:5H2C2O4+2MnO4-+6H+=2Mn2++10CO2↑+8H2O.
(2)步骤一中加入苯的作用是做溶剂,浓硫酸的作用是催化剂和吸水剂,发生反应的化学方程式是
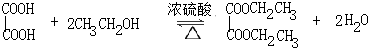 .
.(3)步骤三中用饱和碳酸氢钠溶液洗涤的目的是除去草酸、硫酸等酸性物质.
(4)本实验中,草酸二乙醇的产率为80%.
分析 (1)草酸具有还原性能够被酸性的高锰酸钾氧化生成二氧化碳,高锰酸根离子被还原为二价锰离子;
(2)苯为有机溶剂,依据相似相溶原理可知苯可以溶解有机物;乙二酸与乙醇在浓硫酸最催化剂吸水剂条件下发生酯化反应生成草酸二乙酯和水;
(3)步骤3用饱和碳酸氢钠溶液,可以吸收草酸、硫酸等酸性物质;
(4)依据方程式计算解答.
解答 解:(1)草酸与酸性的高锰酸钾发生氧化还原反应,生成锰离子、二氧化碳、水,该离子反应为5H2C2O4+2MnO4-+6H+=2Mn2++10CO2↑+8H2O,
故答案为:5H2C2O4+2MnO4-+6H+=2Mn2++10CO2↑+8H2O;
(2)草酸、乙醇为有机物易溶于苯,可以用苯做溶剂增大乙醇与草酸接触面积,乙二酸与乙醇在浓硫酸最催化剂吸水剂条件下发生酯化反应生成草酸二乙酯和水,方程式: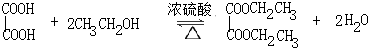 ;
;
故答案为:做溶剂;催化剂、吸水剂;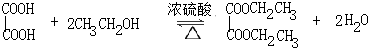 ;
;
(3)步骤3用饱和碳酸氢钠溶液,可以吸收草酸、硫酸等酸性物质;
故答案为:除去草酸、硫酸等酸性物质;
(4)根据反应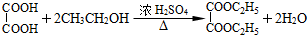
90 146
45g 73g
则本实验中,草酸二乙酯的产率为:$\frac{58.4g}{73g}$×100%=80%,
故答案为:80%.
点评 本题考查有机物的制备实验,为高频考点,把握制备实验原理、有机物的结构与性质、实验中混合物分离提纯等为解答的关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
相关题目
11.已知:2CO(g)+O2(g)=2CO2(g)△H=-566kJ•mol-1
2Na2O2(s)+2CO2(g)=2Na2CO3(s)+O2(g)△H=-452kJ•mol-1
根据以上热化学方程式判断,下列说法正确的是( )
2Na2O2(s)+2CO2(g)=2Na2CO3(s)+O2(g)△H=-452kJ•mol-1
根据以上热化学方程式判断,下列说法正确的是( )
| A. | 1molCO 完全燃烧,放出热量为 283 J | |
| B. | Na2O2(s)+CO2(s)=Na2CO3(s)+$\frac{1}{2}$ O2(g)△H=-226 kJ•mol-1 | |
| C. | CO(g)与 Na2O2(s)反应放出 509 kJ 热量时,电子转移数为 1.204×1024 | |
| D. | CO 的燃烧热为 566 kJ•mol-1 |
12.下列叙述中,不能用平衡移动原理解释的是( )
| A. | 红棕色的NO2气体,加压后颜色先变深后变浅 | |
| B. | 高压比常压有利于合成SO3的反应 | |
| C. | 氯气在水中溶解度大于饱和食盐水中的溶解度 | |
| D. | 由H2、I2蒸气、HI气体组成的平衡体系加压后颜色变深 |
9.下列各组物质中,所含分子数不相同的是( )
| A. | 10g H2 和10g O2 | B. | 5.6L N2(标准状况)和11g CO2 | ||
| C. | 9g H2O 和0.5mol Br2D | D. | 224mLH2 (标准状况)和0.01mol N2 |
16.已知热化学方程式:SO2(g)+$\frac{1}{2}$O2(g)?SO3(g)△H=-98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为( )
| A. | 98.32kJ | B. | 196.64kJ/mol | C. | <196.64kJ | D. | >196.64kJ |
7.莫尔法是一种沉淀滴定法,以K2CrO4为指示剂,用标准硝酸银溶液滴定待测液,进行测定溶液中Cl-的浓度.已知:
滴定终点的现象是滴入最后一滴标准液时,生成砖红色沉淀,且30s内不褪色.终点现象对应的离子反应方程式为2Ag++CrO42-=Ag2CrO4↓.为了测定产品中(NH4)2Cr2O7的含量,称取样品0.150 0g,置于锥形瓶中,加50mL水,再加入2g KI(过量)及稍过量的稀硫酸溶液,摇匀,暗处放置10min,然后加150mL蒸馏水并加入3mL 0.5%淀粉溶液,用0.1000mol/L Na2S2O3标准溶液滴定至终点,消耗Na2S2O3标准溶液30.00mL,则上述产品中(NH4)2Cr2O7的纯度为84%. (假定杂质不参加反应,已知:①Cr2O${\;}_{7}^{2-}$+6I-+14H+═2Cr3++3I2+7H2O,I2+2S2O${\;}_{3}^{2-}$═2I-+S4O${\;}_{6}^{2-}$;②(NH4)2Cr2O7的摩尔质量为252g/moL).
| 银盐 性质 | AgCl | AgBr | Ag2CrO4 |
| 颜色 | 白 | 浅黄 | 砖红 |
 苯乙酸铜是合成优良催化剂、传感材料--纳米氧化铜的重要前驱体之一,下面是它的一种实验室合成路线:
苯乙酸铜是合成优良催化剂、传感材料--纳米氧化铜的重要前驱体之一,下面是它的一种实验室合成路线: