题目内容
4.下列离子方程式中书写正确的是( )| A. | 氧化亚铁与稀盐酸反应:FeO+2H+═Fe3++H2O | |
| B. | 硫酸滴在铜片上:Cu+2H+=Cu2++H2↑ | |
| C. | 硫酸溶液和氢氧化钡溶液反应:Ba2++SO42-═BaSO4 | |
| D. | 硝酸银溶液与氯化钠溶液反应:Ag++Cl-═AgCl↓ |
分析 A.离子方程式两边正电荷不相等,违反了电荷守恒;
B.铜的活泼性较弱,无法置换出氢气;
C.漏掉了氢离子与氢氧根离子生成水的反应;
D.硝酸银与氯化钠溶液反应生成氯化银沉淀和硝酸钠.
解答 解:A.氧化亚铁与稀盐酸反应生成氯化亚铁和水,正确的离子方程式为:FeO+2H+═Fe2++H2O,故A错误;
B.Cu活泼性较弱,硫酸滴在铜片上无法生成氢气,故B错误;
C.硫酸与氢氧化钡生成硫酸钡和水,正确的离子方程式为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,故C错误;
D.硝酸银溶液与氯化钠溶液反应的离子方程式为:Ag++Cl-═AgCl↓,故D正确;
故选D.
点评 本题考查了离子方程式的判断,为高考的高频题,题目难度不大,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应能否发生,检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等).

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.为了除去KC1固体中少量MgSO4和CaCl2杂质.某同学进行了下列七项操作,正确的操作顺序是( )
①加水溶解 ②加热蒸发得到晶体 ③加入过量BaCl2溶液 ④加入过量盐酸 ⑤加入过量K2CO3⑥过滤 ⑦加入过量KOH.
①加水溶解 ②加热蒸发得到晶体 ③加入过量BaCl2溶液 ④加入过量盐酸 ⑤加入过量K2CO3⑥过滤 ⑦加入过量KOH.
| A. | ①⑤③⑦⑥④② | B. | ①⑤⑦③④⑥② | C. | ①⑦③⑤⑥④② | D. | ①⑦③④⑥⑤② |
12.下列叙述中,不能用平衡移动原理解释的是( )
| A. | 红棕色的NO2气体,加压后颜色先变深后变浅 | |
| B. | 高压比常压有利于合成SO3的反应 | |
| C. | 氯气在水中溶解度大于饱和食盐水中的溶解度 | |
| D. | 由H2、I2蒸气、HI气体组成的平衡体系加压后颜色变深 |
19.键能是指拆开1mol化学键需要吸收的能量或形成1mol化学键所释放的能量.表中列出了某些共价键的键能:
根据表中数据判断下列表述中正确的是( )
| 共价键 | 键能/ kJ•mol-1 | 共价键 | 键能/ kJ•mol-1 | 共价键 | 键能/ kJ•mol-1 |
| H-H | 436 | H-Br | 366 | Cl-Cl | 243 |
| H-O | 463 | H-I | 298 | Br-Br | 193 |
| H-Cl | 432 | O=O | 496 | I-I | 151 |
| A. | H2O中含有两个O-H共价键,故用氢气与氧气合成1 mol H2O放出的能量为926 kJ | |
| B. | 用单质合成1 mol H-Cl所放出的能量小于合成1 mol H-Br所放出的能量 | |
| C. | 当用表中卤素单质与氢气合成卤化氢时,所有的反应都是放热反应 | |
| D. | 合成溴化氢的热化学方程式为H2(g)+Br2(g)═2HBr(g)△H=+103 kJ•mol-1 |
9.下列各组物质中,所含分子数不相同的是( )
| A. | 10g H2 和10g O2 | B. | 5.6L N2(标准状况)和11g CO2 | ||
| C. | 9g H2O 和0.5mol Br2D | D. | 224mLH2 (标准状况)和0.01mol N2 |
16.已知热化学方程式:SO2(g)+$\frac{1}{2}$O2(g)?SO3(g)△H=-98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为( )
| A. | 98.32kJ | B. | 196.64kJ/mol | C. | <196.64kJ | D. | >196.64kJ |
15.亚硫酸钠和硫粉通过化合反应可制得硫代硫酸钠(Na2S2O3).
已知:Na2S2O3在酸性溶液中不能稳定存在.有关物质的溶解度随温度变化曲线如图2所示.某研究小组设计了制备Na2S2O3•5H2O的装置图(如图1).
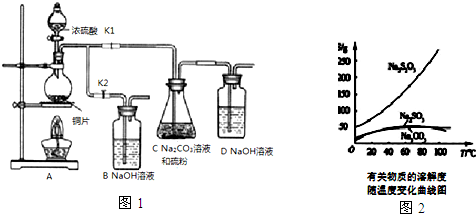
部分操作步骤如下:
①打开K1,关闭K2,向圆底烧瓶中加入足量浓硫酸,加热.
②C中混合液被气流搅动,反应一段时间后,硫粉的量逐渐减少.当C中溶液的pH接近7时,即停止C中的反应,停止加热
③过滤C中的混合液,并将滤液进行处理,得到产品.
(1)步骤①中,圆底烧瓶中发生反应的化学方程式是Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O.
(2)步骤②中,“当C中溶液的pH接近7时即停止C中的反应”的原因是Na2S2O3在酸性溶液中不能稳定存在.“停止C中的反应”的操作是打开K2,关闭K1.
(3)步骤③中,“过滤”用到的玻璃仪器是烧杯、漏斗、玻璃棒(填仪器名称).将滤液进行处理过程是将滤液经过加热浓缩、冷却结晶、过滤、洗涤、烘干,得到产品.
依据反应2S2O32-+I2→S4O62-+2I-,可用I2的标准溶液测定产品的纯度.取5.5g产品配制成100mL溶液.取10mL溶液,以淀粉溶液为指示剂,用浓度为0.050mol/L I2的标准溶液进行滴定,相关数据记录如表所示.
(4)判断达到滴定终点的现象是加入最后一滴I2标准溶液后,溶液变蓝,且半分钟不改变.
(5)Na2S2O3•5H2O在产品中的质量分数是90.2%.(计算结果请用百分数表示并保留1位小数)(Na2S2O3•5H2O的式量为248)
已知:Na2S2O3在酸性溶液中不能稳定存在.有关物质的溶解度随温度变化曲线如图2所示.某研究小组设计了制备Na2S2O3•5H2O的装置图(如图1).

部分操作步骤如下:
①打开K1,关闭K2,向圆底烧瓶中加入足量浓硫酸,加热.
②C中混合液被气流搅动,反应一段时间后,硫粉的量逐渐减少.当C中溶液的pH接近7时,即停止C中的反应,停止加热
③过滤C中的混合液,并将滤液进行处理,得到产品.
(1)步骤①中,圆底烧瓶中发生反应的化学方程式是Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O.
(2)步骤②中,“当C中溶液的pH接近7时即停止C中的反应”的原因是Na2S2O3在酸性溶液中不能稳定存在.“停止C中的反应”的操作是打开K2,关闭K1.
(3)步骤③中,“过滤”用到的玻璃仪器是烧杯、漏斗、玻璃棒(填仪器名称).将滤液进行处理过程是将滤液经过加热浓缩、冷却结晶、过滤、洗涤、烘干,得到产品.
依据反应2S2O32-+I2→S4O62-+2I-,可用I2的标准溶液测定产品的纯度.取5.5g产品配制成100mL溶液.取10mL溶液,以淀粉溶液为指示剂,用浓度为0.050mol/L I2的标准溶液进行滴定,相关数据记录如表所示.
| 编号 | 1 | 2 | 3 | 4 |
| 溶液的体积/mL | 10.00 | 10.00 | 10.00 | 10.00 |
| 消耗I2标准溶液的体积/mL | 19.99 | 19.98 | 17.13 | 20.03 |
(5)Na2S2O3•5H2O在产品中的质量分数是90.2%.(计算结果请用百分数表示并保留1位小数)(Na2S2O3•5H2O的式量为248)