题目内容
8.除去BaCl2 溶液的少量盐酸,最好选择的试剂是( )| A. | Ba(OH)2溶液 | B. | BaCO3粉末 | C. | AgNO3溶液 | D. | NaOH溶液 |
分析 盐酸可与氢氧化钡、碳酸钡反应生成氯化钡,其中碳酸钡不溶于水,可过滤除去,避免引入新杂质,以此解答.
解答 解:A.因不能确定盐酸的量,加入氢氧化钡,易引入新杂质,故A错误;
B.碳酸钡反应生成氯化钡,碳酸钡不溶于水,可过滤除去,可用于除杂,故B正确;
C.二者都与硝酸银反应生成沉淀,不能用于除杂,故C错误;
D.加入氢氧化钠,生成氯化钠,引入新杂质,故D错误.
故选B.
点评 本题考查物质的分离、提纯知识,为高考常见题型和高频考点,侧重于学生的分析能力和实验能力的考查,除杂时注意不能引入新的杂质且不能影响被提纯物质的性质,注意把握物质的性质的异同,难度不大.

练习册系列答案
相关题目
18.下列饱和溶液中通入过量的CO2气体,溶液不会变挥浊的是( )
| A. | NaAlO2溶液 | B. | Na2SiO3溶液 | C. | 苯酚钠溶液 | D. | CaCl2溶液 |
16. N2O5是一种新型硝化剂,其性质和制备受到人们的关注.
N2O5是一种新型硝化剂,其性质和制备受到人们的关注.
(1)一定温度下,在恒容密闭容器中N2O5可发生下列反应:N2O5(g)?4NO2(g)+O2(g);△H>0
①反应达平衡后,再通入一定量N2O5,则N2O5的转化率将减小.(填““增大”“减小”或“不变”);
②下表为反应在T1温度下的部分实验数据:
则500s内N2O5的分解速率为0.00296 mol•L-1•s-1.
③在T2温度下,反应1000s时测得NO2的浓度为4.98mol•L-1,则T2<T1.
(2)如图所示装置可用于制备N2O5,则N2O5在电解池的阳极区生成,其电极反应式为N2O4+2HNO3-2e-═2N2O5+2H+.
 N2O5是一种新型硝化剂,其性质和制备受到人们的关注.
N2O5是一种新型硝化剂,其性质和制备受到人们的关注.(1)一定温度下,在恒容密闭容器中N2O5可发生下列反应:N2O5(g)?4NO2(g)+O2(g);△H>0
①反应达平衡后,再通入一定量N2O5,则N2O5的转化率将减小.(填““增大”“减小”或“不变”);
②下表为反应在T1温度下的部分实验数据:
| t/s | 0 | 500 | 1 000 |
| c(N2O5)/mol•L-1 | 5.00 | 3.52 | 2.48 |
③在T2温度下,反应1000s时测得NO2的浓度为4.98mol•L-1,则T2<T1.
(2)如图所示装置可用于制备N2O5,则N2O5在电解池的阳极区生成,其电极反应式为N2O4+2HNO3-2e-═2N2O5+2H+.
3.下列各组物质相互混合反应后,既有气体生成,最终又有沉淀生成的是( )
①金属钠投入到FeCl3溶液中 ②过量NaOH溶液和明矾溶液混合
③少量Ca(OH)2投入过量NaHCO3溶液中 ④Na2O2投入FeCl2溶液中.
①金属钠投入到FeCl3溶液中 ②过量NaOH溶液和明矾溶液混合
③少量Ca(OH)2投入过量NaHCO3溶液中 ④Na2O2投入FeCl2溶液中.
| A. | 只有①④ | B. | 只有③ | C. | 只有②③ | D. | 只有①③④ |
13.完成如表实验与选择的装置或仪器(夹持装置已略去)能达到实验目的是( )
| A | B | C | D | |
| 实验 | 用酒精提取溴水中的Br2 | 除去氢氧化铁胶体中的铁离子 | 分离NH4Cl和I2的固体混合物 | 稀释10mL98% 的浓硫酸溶液 |
| 装置或仪器 | 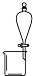 |  |  | 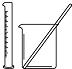 |
| A. | A | B. | B | C. | C | D. | D |
20.为除去括号内的杂质,所选用的试剂或方法不正确的是( )
| A. | NaCO3溶液(NaHCO3),选用适量NaOH溶液 | |
| B. | NaHCO3溶液(NaCO3),应通入过量CO2气体 | |
| C. | Na2O2粉末(Na2O),将混合物在空气中加热 | |
| D. | 镁粉(铝粉),选用过量的烧碱溶液 |
17.标准状况下,将体积为V L的圆底烧瓶中充满氨气,倒扣在含有足量水的水槽中(如图所示),实验完毕后立即将烧瓶从水槽中取出,所得溶液的密度为ρg•cm-3.下列说法错误的是( )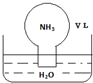

| A. | 水最终会充满整个烧瓶 | |
| B. | 所得溶液的物质的量浓度为$\frac{1}{22.4}$ mol•L-1 | |
| C. | 所得溶液的质量分数为$\frac{17}{22400}$ρ | |
| D. | 所得溶液中,n(NH3•H2O)+n(NH4+)=$\frac{V}{22.4}$mol |
18.在两个容积相同的密闭容器中,一个盛有HCl气体,另一个盛有H2和Cl2的混合气体,在同温同压下,两容器内的气体一定不能具有相同的( )
| A. | 密度 | B. | 颜色 | C. | 原子数 | D. | 分子数 |
 某小组以CoCl2•6H2O、NH4Cl、H2O2、浓氨水为原料,在活性炭催化下,合成橙黄色晶体X.为确定其组成,进行如下实验.
某小组以CoCl2•6H2O、NH4Cl、H2O2、浓氨水为原料,在活性炭催化下,合成橙黄色晶体X.为确定其组成,进行如下实验.