题目内容
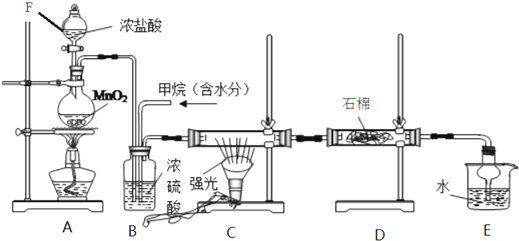
9.氯气是一种黄绿色气体.1974年,瑞典化学家舍勒发现软锰矿(主要成分是MnO2)和浓盐酸混合加热能制取氯气:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;通常也可用高锰酸钾和浓盐酸混合来制取氯气:2KMnO4+16HCl(浓)═2MnCl2+5Cl2↑+2KCl+8H2O;(1)若用这两种方法制氯气,请比较,它们的发生装置使用的不同仪器是前者需要酒精灯加热,后者不需要.
(2)现将29g纯度为60%的软锰矿(主要成分MnO2)与足量的浓盐酸充分反应(杂质不参加反应),把反应后所得溶液稀释到200mL.计算:
①生成的Cl2在标准状况下的体积.
②稀释后溶液中MnCl2的物质的量浓度.
分析 (1)根据反应条件确定制备装置的异同之处;
(2)①根据质量分数计算软锰矿中二氧化锰的质量,再根据n=$\frac{m}{M}$计算二氧化锰的物质的量,根据方程式计算生成的氯气的物质的量,利用V=nVm计算氯气的体积;
②消耗前后氯化锰的物质的量不变,由方程式可知n(MnCl2)=n(MnO2),根据c=$\frac{n}{V}$计算稀释后液中MnCl2的物质的量浓度.
解答 解:(1)软锰矿(主要成分是MnO2)和浓盐酸混合加热能制取氯气:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,需在加热条件下进行;用高锰酸钾和浓盐酸混合来制取氯气:2KMnO4+16HCl(浓)═2MnCl2+5Cl2↑+2KCl+8H2O,该反应无需加热,所以它们的发生装置使用的不同仪器是前者需要酒精灯加热,后者不需要,故答案为:前者需要酒精灯加热,后者不需要;
(2)①29g纯度为60%的软锰矿(主要成分MnO2)中MnO2的物质的量为:$\frac{29×60%}{87}$mol=0.2mol,则:
MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O
1 1
0.2mol n(Cl2)
所以n(Cl2)=0.2mol,故V(n(Cl2)=0.2mol×22.4L/mol=4.48L,
答:标准状况下生成的Cl2的体积为4.48L;
②消耗前后氯化锰的物质的量不变,由方程式可知n(MnCl2)=n(MnO2)=0.2mol,将反应后所得溶液稀释成200mL,稀释后液中MnCl2的物质的量浓度为$\frac{0.2mol}{0.2L}$=1mol/L,
答:稀释后液中MnCl2的物质的量浓度为1mol/L.
点评 本题考查根据方程式的计算、常用化学计量数的有关计算,比较基础,旨在考查学生对基础知识的理解掌握.

 名校课堂系列答案
名校课堂系列答案| A. | AgNO3、K2CO3 | B. | AgNO3、K2CO3、HNO3 | ||
| C. | K2CO3、AgNO3 | D. | K2CO3、AgNO3、HNO3 |
| A. | 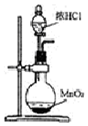 用如图装置制取氯气 | |
| B. | 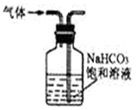 用如图装置除去CO2中的少量SO2气体 | |
| C. | 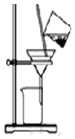 用如图装置分离饱和Na2CO3溶液中的NaHCO3晶体 | |
| D. |  用如图装置将MgCl2.6H2O加热得到MgCl2 |
| A. | 容器内气体压强不随时间变化 | |
| B. | 容器内气体密度不随时间变化 | |
| C. | 容器内X、Y、Z的浓度之比为1:2:2 | |
| D. | X的消耗速率和Z的生成速率之比为1:2 |
| A. | 2.0g重水(D2O)中含有的中子数为NA | |
| B. | 标准状况下22.4L的四氯化碳,含有四氯化碳分子数为NA | |
| C. | 23g金属钠变为钠离子时失去的电子数为NA | |
| D. | 常温常压下,48gO3和O2混合气体中含有的氧原子数为3NA |
| A. | ①③④⑦⑧⑨ | B. | ①④⑦⑧⑨⑩ | C. | ①③④⑥⑨⑩ | D. | ①②④⑤⑧⑨ |
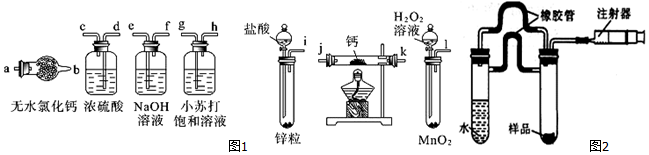
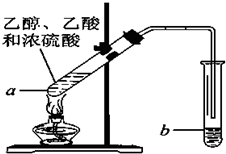 乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平.请回答下列问题.
乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平.请回答下列问题. ,结构简式H2C=CH2.
,结构简式H2C=CH2. ,反应类型是加聚反应.
,反应类型是加聚反应.