题目内容
1. 乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平.请回答下列问题.
乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平.请回答下列问题.(1)乙烯的电子式
 ,结构简式H2C=CH2.
,结构简式H2C=CH2.(2)已知 2CH3CHO+O2$→_{△}^{催化剂}$ 2CH3COOH.若以乙烯为主要原料合成乙酸,其合成路线所示.乙烯$\stackrel{①}{→}$A$\stackrel{②}{→}$B$\stackrel{③}{→}$乙酸
反应②的化学方程式为2CH3CH2OH+O2$→_{△}^{Cu或Ag}$2CH3CHO+2H2O,反应类型是氧化反应. 工业上以乙烯为原料可以生产一种重要的合成有机高分子化合物,其反应的化学方程式为
 ,反应类型是加聚反应.
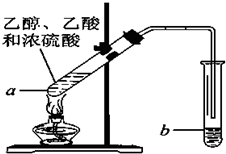
,反应类型是加聚反应.(3)实验室可以用乙酸按如图所示的装置制取乙酸乙酯,请回答下列问题.
试管a中发生反应的化学方程式为CH3COOH+C2H5OH$?_{△}^{浓硫酸}$CH3COOC2H5+H2O,反应类型是酯化反应.反应开始前,试管b中盛放的溶液是饱和碳酸钠溶液其作用是吸收乙酸乙酯,除去乙醇和乙酸、降低乙酸乙酯的溶解度,便于分层.可用分液的方法把制得的乙酸乙酯分离出来.
分析 (1)乙烯是含有碳碳双键的最简单的烯烃,根据电子式可以书写结构简式;
(2)乙烯可以和水加成生成乙醇,乙醇可以被氧化为乙醛,乙醛易被氧化为乙酸;乙烯可以发生加聚反应生成聚乙烯;
(3)乙酸和乙醇在浓硫酸作用下发生酯化反应,生成乙酸乙酯和水,属于酯化反应;制备乙酸乙酯时常用饱和碳酸钠溶液吸收乙酸乙酯,目的是除去乙醇和乙酸、降低乙酸乙酯的溶解度,便于分层;乙酸乙酯不溶于饱和碳酸钠溶液.
解答 解:(1)乙烯中含碳和碳之间以共价双键结合,电子式为 ,根据电子式可以书写结构简式为H2C=CH2,
,根据电子式可以书写结构简式为H2C=CH2,
故答案为: ;H2C=CH2;
;H2C=CH2;
(2)(4)乙烯可以和水加成生成乙醇,所以A是乙醇,乙醇可以被氧化为B乙醛,乙醛易被氧化为C乙酸,乙醇的催化氧化反应为:2CH3CH2OH+O2$→_{△}^{Cu或Ag}$2CH3CHO+2H2O,反应为氧化反应;乙烯可以发生加聚反应生成聚乙烯,反应为: ,属于加聚反应,
,属于加聚反应,
故答案为:2CH3CH2OH+O2$→_{△}^{Cu或Ag}$2CH3CHO+2H2O;氧化反应; ;加聚反应;
;加聚反应;
(3)乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,同时该反应可逆,反应的化学方程式为:CH3COOH+C2H5OH $?_{△}^{浓硫酸}$CH3COOC2H5+H2O,反应为酯化反应,制备乙酸乙酯时常用饱和碳酸钠溶液吸收乙酸乙酯,除去乙醇和乙酸、降低乙酸乙酯的溶解度,便于分层.乙酸乙酯不溶于饱和碳酸钠溶液,可用分液的方法分离,
故答案为:CH3COOH+C2H5OH$?_{△}^{浓硫酸}$ CH3COOC2H5+H2O;酯化反应;饱和碳酸钠溶液;吸收乙酸乙酯,除去乙醇和乙酸、降低乙酸乙酯的溶解度,便于分层;分液.
点评 本题考查乙烯的化学性质、制备方案的设计,题目难度不大,明确酯化反应原理为解答关键,注意掌握酯化反应中浓硫酸、饱和碳酸钠溶液溶液的作用,试题培养了学生的分析能力及化学实验能力.

 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案| A. | 铜丝 | B. | 熔融的MgCl2 | C. | NaCl溶液 | D. | SO3 |
| A. | KCl | B. | Na2S | C. | (NH4)2SO4 | D. | BaSO4 |
| A. |  测定中和热 | B. | 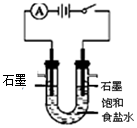 电解食盐水 | ||
| C. | 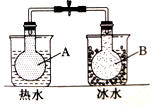 温度对化学平衡的影响 | D. | 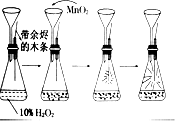 催化剂对反应速率的影响 |
(1)请帮他们完成以下实验报告:
实验目的:探究铁及其化合物的氧化性和还原性.
试剂:铁粉、FeCl3溶液、FeCl2溶液、氯水、锌片、铜片.
实验记录:
| 序号 | 实验内容 | 实验现象 | 离子方程式 | 实验结论 |
| ① | 在FeCl2溶液中滴入适量氯水 | 溶液由浅绿色变为棕黄色 | Fe2+具有还原性 | |
| ② | 在FeCl2溶液中加入锌片 | (不写) | Zn+Fe2+═Zn2++Fe | |
| ③ | 在FeCl3溶液中加入足量铁粉 | Fe+2Fe3+═3Fe2+ | Fe3+具有氧化性 | |
| ④ | (不写) | Fe3+具有氧化性 |
(2)根据以上结论判断,下列物质中既有氧化性,又有还原性的有:AEF.(填序号)
A.Cl2 B.Na C.Na+ D.Cl- E.SO2 F.NO2
(3)亚铁盐在溶液中易被氧化,而实验室中需要纯净的亚铁盐溶液.那么保存亚铁盐溶液时可以在溶液中加入少量铁粉以防止亚铁盐被氧化.
(4)检验亚铁盐溶液是否被氧化的操作步骤和现象是取少许亚铁盐溶液于试管中,滴加几滴KSCN溶液,如果溶液变红则说明亚铁盐被氧化.
(5)向FeCl2溶液滴加NaOH溶液最终生成Fe(OH)3浊液,该过程的现象为生成白色沉淀,迅速变成灰绿色,最终变成红褐色,此过程中发生的氧化还原反应的化学方程式4Fe(OH)2+O2+2H2O=4Fe(OH)3.
(1)滴定:用酸式滴定管盛装c mol/L盐酸标准液.实验中选用酚酞作指示剂,当滴入最后一滴盐酸时,溶液由红色变为无色、且半分钟内不变色现象时表示滴定达到终点.实验有关数据记录如下:
| 滴定 序号 | 待测液体积(mL) | 所消耗盐酸标准液的体积(mL) | ||
| 滴定前 | 滴定后 | 消耗的体积 | ||
| 1 | V | 0.50 | 25.80 | 25.30 |
| 2 | V | 6.00 | 31.35 | 25.35 |
(3)对下列几种假定情况进行讨论:(填“无影响”、“偏高”、“偏低”)
a.若滴定前用蒸馏水冲洗锥形瓶,则会使测定结果无影响;
b.读数时,若滴定前仰视,滴定后俯视,则会使测定结果偏低;
c.若在滴定过程中不慎将数滴酸液滴在锥形瓶外,则会使测定结果偏高;
d.滴加盐酸速度过快,未充分振荡,刚看到溶液变色,立刻停止滴定,则会使测定结果偏低.
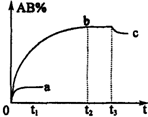 反应A2+B2?2AB;△H=Q,在不同温度和压强改变的条件下,产物AB的质量分数AB%生成情况如图:a为500℃时的情况;b为300℃时的情况;c为反应在300℃时从时间t3开始向容器中加压的情况.则下列叙述正确的是( )
反应A2+B2?2AB;△H=Q,在不同温度和压强改变的条件下,产物AB的质量分数AB%生成情况如图:a为500℃时的情况;b为300℃时的情况;c为反应在300℃时从时间t3开始向容器中加压的情况.则下列叙述正确的是( )| A. | A2、B2及AB均为气体,Q>0 | |
| B. | AB为气体,A2、B2中至少有一种为非气体,Q<0 | |
| C. | AB为气体,A2、B2中有一种为气体,Q<0 | |
| D. | AB为固体,A2、B2中有一种为非气体,Q>0 |