题目内容
13.下列离子方程式中,正确的是( )| A. | 碳酸钙与盐酸反应:CO32-+2H+═CO2↑+H2O | |
| B. | 硫酸铜溶液中滴加氢氧化钡溶液:Ba2++2OH-+Cu2++SO42-═BaSO4↓+Cu(OH)2↓ | |
| C. | 硝酸银溶液中加入铜粉:Ag++Cu═Cu2++Ag↓ | |
| D. | 铁与稀盐酸反应:2Fe+6H+═2Fe3++3H2↑ |
分析 A.碳酸钙是难溶物,不能拆成离子形式;
B.硫酸铜溶液中滴加氢氧化钡溶液反应生成硫酸钡和氢氧化铜;
C.铜活泼性大于银,可以从银盐溶液中置换出银,但左右电荷不守恒;
D.铁与稀盐酸反应生成氯化亚铁和氢气.
解答 解:A.碳酸钙是难溶物,不能拆成离子形式,碳酸钙与盐酸反应,反应为:CaCO3+2H+═Ca2++H2O+CO2↑,故A错误;
B.硫酸钡和氢氧化铜都为沉淀,硫酸铜溶液中滴加氢氧化钡溶液的离子反应为:SO42-+Cu2++Ba2++2OH-=Cu(OH)2↓+BaSO4↓,故B正确;
C.铜活泼性大于银,可以从银盐溶液中置换出银,硝酸银溶液中加入铜粉反应的离子方程式:2Ag++Cu═Cu2++2Ag,故C错误;
D.Fe与稀盐酸反应的离子反应为:Fe+2H+═Fe2++H2↑,故D错误;
故选B.
点评 本题考查离子反应的书写,注意从电荷守恒、原子守恒,明确发生的化学反应及离子反应中保留化学式的物质即可解答,注重基础知识的考查,题目难度不大.

练习册系列答案
相关题目
6.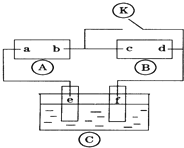 图中
图中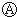 为直流电,
为直流电,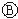 为浸透饱和氯化钠溶液和酚酞试液的滤纸,
为浸透饱和氯化钠溶液和酚酞试液的滤纸, 为电镀池.接通电路后发现
为电镀池.接通电路后发现 上的c点显红色.为实现铁上镀锌,接通
上的c点显红色.为实现铁上镀锌,接通 后,使c、d两点短路.下列叙述正确的是( )
后,使c、d两点短路.下列叙述正确的是( )
 图中
图中 为直流电,
为直流电, 为浸透饱和氯化钠溶液和酚酞试液的滤纸,
为浸透饱和氯化钠溶液和酚酞试液的滤纸, 为电镀池.接通电路后发现
为电镀池.接通电路后发现 上的c点显红色.为实现铁上镀锌,接通
上的c点显红色.为实现铁上镀锌,接通 后,使c、d两点短路.下列叙述正确的是( )
后,使c、d两点短路.下列叙述正确的是( )| A. | b为直流电的正极 | B. | e电极为铁 | ||
| C. | f极发生还原反应 | D. | d极发生的反应为:2H++2e-=H2↑ |
4.做实验时不小心使皮肤上沾上了一些高锰酸钾,形成的黑斑很久才能消除,如果用草酸(乙二酸)的稀溶液洗涤,黑斑可以迅速褪去,其离子方程式为:MnO4-+C2O42-+H+═CO2↑+Mn2++( )下列有关叙述正确的是( )
| A. | 发生还原反应的是C2O42- | |
| B. | 该离子方程式右侧横线上的产物是OH- | |
| C. | 10molH+参加反应时,电子转移5mol | |
| D. | 该反应的氧化剂为KMnO4 |
1.下列离子方程式中,正确的是( )
| A. | 钠和冷水反应:Na+2H2O═Na++2OH-+H2↑ | |
| B. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ | |
| C. | 三氯化铁溶液中加入铁粉:Fe3++Fe═2 Fe2+ | |
| D. | FeCl2溶液跟Cl2反应:2Fe2++Cl2═2Fe3++2Cl- |
8.下列金属中,遇到盐酸和氢氧化钠溶液都能放出气体的是( )
| A. | Cu | B. | Mg | C. | Fe | D. | Al |
2.下列实验现象,与新制氯水中的某些成分(括号内物质)没有关系的( )
| A. | 将NaHCO3固体加入新制氯水,有无色气泡(H+) | |
| B. | 滴加AgNO3溶液生成白色沉淀(Cl-) | |
| C. | 向KI溶液中滴加氯水,再滴加CCl4溶液,发现CCl4溶液呈紫色(Cl2) | |
| D. | 使红色布条褪色(HCl) |
1.Na2S2O3可用作纺织工业氯气漂白布匹后的“脱氯剂”,4Cl2+Na2S2O3+5H2O═2NaCl+2H2SO4+□,有关该反应的叙述不正确的是( )
| A. | Na2S2O3是还原剂 | |
| B. | 根据该反应可判断氧化性:Cl2>SO42-、 | |
| C. | □的物质是HCl | |
| D. | 上述反应中,每生成1mol SO42-,转移2mole- |