题目内容
25℃时,1mol/L的NH4Cl、CH3COONH4、NH4HSO4、NH3?H2O四种溶液中,测得c(NH4+)分别为a、b、c、d(单位为mol/L),下列判断正确的是( )
| A、a=b=c=d |
| B、a>b>d>c |
| C、d>a>c>b |
| D、c>a>b>d |
考点:离子浓度大小的比较
专题:
分析:相同温度、相同浓度的这四种种盐溶液,硫酸氢铵溶液中的氢离子抑制铵根离子水解;醋酸铵溶液中醋酸根离子促进铵根离子水解,铵根离子水解程度较大,则溶液中铵根离子浓度越小;一水合氨为弱碱,溶液中部分电离出铵根离子,铵根离子浓度最小,据此进行判断.
解答:
解:相同温度、相同浓度的这三种盐溶液,NH4Cl溶液中铵根离子正常水解;
NH4HSO4溶液中氢离子抑制铵根离子水解,铵根离子浓度较大;
CH3COONH4溶液中醋酸根离子促进铵根离子水解,铵根离子水解程度越大,则溶液中铵根离子浓度越小;
NH3?H2O为弱电解质,在溶液中部分电离出铵根离子,则四种溶液中铵根离子浓度最小,
所以溶液中铵根离子浓度大小顺序为:c>a>b>d,
故选D.
NH4HSO4溶液中氢离子抑制铵根离子水解,铵根离子浓度较大;
CH3COONH4溶液中醋酸根离子促进铵根离子水解,铵根离子水解程度越大,则溶液中铵根离子浓度越小;
NH3?H2O为弱电解质,在溶液中部分电离出铵根离子,则四种溶液中铵根离子浓度最小,
所以溶液中铵根离子浓度大小顺序为:c>a>b>d,
故选D.
点评:本题考查了弱电解质的电离、盐类水解原理及其影响,题目难度中等,明确影响盐类水解的因素是解本题关键,注意掌握弱电解质的电离情况,试题有利于培养学生灵活应用所学知识的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
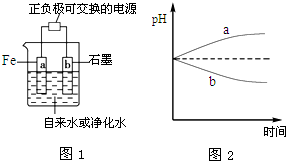 推销净水器的商人用自来水做电解实验,一段时间后两极间产生灰绿色沉淀,并很快变成红褐色,然后用净水器净化后的水做电解实验,两极上只有气体产生,水中并无沉淀,用以证明自来水很“脏”.人们将自来水送检,却是合格的,下列有关说法,合理的是( )
推销净水器的商人用自来水做电解实验,一段时间后两极间产生灰绿色沉淀,并很快变成红褐色,然后用净水器净化后的水做电解实验,两极上只有气体产生,水中并无沉淀,用以证明自来水很“脏”.人们将自来水送检,却是合格的,下列有关说法,合理的是( )| A、商人电解自来水时,用石墨做阳极;电解净化水时,用铁做阳极 |
| B、电解自来水时,阴极反应式:O2+2H2O+4e-═4OH- |
| C、电解净化水时,a、b两极的pH变化如图2所示 |
| D、电解自来水实验中,若阴极产生气体为3.36L(标况),则阳极质量减小5.6克 |
下列关于糖的说法不正确的是( )
| A、糖类是含有醛基或羰基的有机物物质 |
| B、淀粉和纤维素都是天然高分子化合物 |
| C、葡萄糖的分子式是C6H12O6,它是一种多羟基醛 |
| D、蔗糖和麦芽糖都是二糖,它们互为同分异构体 |
下列离子在溶液中能大量共存的是( )
| A、Fe3+、NH4+、SCN-、Cl- |
| B、Na+、H+、NO3-、SiO32-、 |
| C、OH-、Ba2+、Na+、AlO2- |
| D、Fe2+、NH4+、Cl- OH- |
在0.1mol?L-1的Na2CO3溶液中,下列关系正确的是( )
| A、C[Na+]>C[CO32-]>C[HCO3-]>C[OH-]>C[H+] |
| B、C[Na+]>C[CO32-]>C[OH-]>C[HCO3-]>C[H+] |
| C、C[Na+]+C[H+]=C[CO32-]+C[OH-]+C[HCO3-] |
| D、C[CO32-]+C[HCO3-]=0.1mol?L-1 |
下列有关金属及其化合物的说法中,错误的是( )
| A、生活中用碱液洗涤铝制饮具 |
| B、用小苏打治疗胃酸过多 |
| C、用过氧化钠做潜水呼吸面具供氧剂 |
| D、铁、铜制品应要保持干燥,以防生锈 |
下列不属于硅酸盐产品的是( )
| A、二氧化硅 | B、陶瓷 |
| C、玻璃 | D、水泥 |