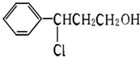
��Ŀ����
 ��ҵ��ˮ�к��ж����к��ɷ֣������ŷŽ����������Ⱦ�����з��ദ����������ŷţ�
��ҵ��ˮ�к��ж����к��ɷ֣������ŷŽ����������Ⱦ�����з��ദ����������ŷţ���1������Cu2+�����ӵķ�ˮ��������FeS������������Ϊ��������ȥ���������ӷ���ʽ˵���������ӵ�ԭ��
��2��������ˮ�ж���Σ���ܴ����������ں�+6�۸��ķ�ˮ�м���һ���������������������ʹ+6�۸���ԭ��+3�۸����ٵ�����ҺpH��6��8֮�䣬ʹFe3+��Cr3+ת��ΪFe��OH��3��Cr��OH��3��������ȥ�������ӷ���ʽ��ʾ��ҺpH���ܳ���10��ԭ��
��֪��
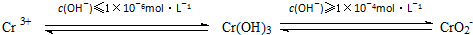
��3����ˮ�еİ����Ի��������ã�
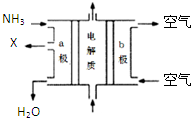
�ٰ�����Ƴ���ͼ��ʾ�ļ���ȼ�ϵ�أ�������X�����ֱ���ŷŵ������У�a�缫��
�ڼ�ˮϡ�Ͱ�ˮ�Ĺ����У����б���ʽ����ֵ������
A��c��H+�� B��
| c(OH-) |
| c(NH3?H2O) |
C��c��H+��?c��OH-�� D��c��NH4+��+c��H+��
��T���£�NH3?H2O�ĵ��볣��ΪKa��NH4+��ˮ��ƽ�ⳣ��ΪKh������¶���ˮ�����ӻ�����Kw=
��һ�������£���ij�ܱ������м���һ������N2��H2�������淴Ӧ��N2��g��+3H2��g���T2NH3��g����H=-92.2kJ?mol-1�����0��10s�ڣ�c��H2����С��0.75mol?L-1������˵����ȷ����
A���÷�Ӧ���淴Ӧ�Ļ�ܲ�С��92.2kJ?mol-1
B��10s�ڰ�����ƽ����Ӧ����Ϊ0.025mol?L-1?s-1
C��10s��15s��c��NH3����������0.25mol?L-1
D����ƽ����������NH3��ƽ��������Ӧ�����ƶ���v������
���㣺���������ˮ��Һ�еĵ���ƽ��,��ѧ��Դ���͵��,��ѧƽ��ļ���,����ˮ���ԭ��,���ʵķ��롢�ᴿ�ͳ���
ר�⣺��ѧƽ��ר��,����ƽ������Һ��pHר��,�绯ѧר��
��������1������ת�Ƶķ��������Ÿ����ܵķ����ƶ���H2Sͨ������NaOH��Һ������Na2S�����������غ������
��2������������Ϣ��֪pH����10ʱ��Cr��OH��3���ܽ⣻
��3���ٰ�����ȼ��Ӧ���븺����������ȼ�ϵ�����������ӳ�����缫��Ӧ�������е�Nʧȥ���ӻ��ϼ����ߣ�����X����Ⱦ����ȷ��XΪ������
��һˮ�ϰ�Ϊ������ʣ���ˮϡ�ʹٽ���ˮ�ĵ��룬c��OH-����С����c��H+������Ka��Kw���䣻
�ۼ�ĵ���ƽ�ⳣ�������������ӵ�ˮ��ƽ�ⳣ����ˮ�����ӻ�����֮��Ĺ�ϵΪKa?Kh=Kw��
��A����H=����Ӧ�Ļ��-�淴Ӧ�Ļ�ܣ�
B������������Ũ�ȱ仯���������Ũ�ȱ仯������Ӧ���ʣ�
C���淴Ӧ���з�Ӧ���Ũ�ȼ�С����Ӧ���ʼ�С��
D�������������Ũ�ȣ���Ӧ���ʼ�С��
��2������������Ϣ��֪pH����10ʱ��Cr��OH��3���ܽ⣻
��3���ٰ�����ȼ��Ӧ���븺����������ȼ�ϵ�����������ӳ�����缫��Ӧ�������е�Nʧȥ���ӻ��ϼ����ߣ�����X����Ⱦ����ȷ��XΪ������
��һˮ�ϰ�Ϊ������ʣ���ˮϡ�ʹٽ���ˮ�ĵ��룬c��OH-����С����c��H+������Ka��Kw���䣻
�ۼ�ĵ���ƽ�ⳣ�������������ӵ�ˮ��ƽ�ⳣ����ˮ�����ӻ�����֮��Ĺ�ϵΪKa?Kh=Kw��
��A����H=����Ӧ�Ļ��-�淴Ӧ�Ļ�ܣ�
B������������Ũ�ȱ仯���������Ũ�ȱ仯������Ӧ���ʣ�
C���淴Ӧ���з�Ӧ���Ũ�ȼ�С����Ӧ���ʼ�С��
D�������������Ũ�ȣ���Ӧ���ʼ�С��
���
�⣺��1������ͬ������CuS���ܽ�ȱ�FeS��С����������������CuS�ķ�����У������ӷ���ʽΪFeS��s��+Cu2+��aq��=CuS��s��+Fe2+��aq����H2Sͨ������NaOH��Һ������Na2S��Na2S��Һ�д��������غ㣬��n��Na��=2n��S������c��Na+��=2[c��S2-��+c��HS-��+c��H2S��]��
�ʴ�Ϊ��FeS��s��+Cu2+��aq��=CuS��s��+Fe2+��aq����2[c��S2-��+c��HS-��+c��H2S��]��
��2������������Ϣ��֪pH����10����c��OH-����10-4mol/Lʱ��Cr��OH��3���ܽ�����CrO2-���䷴Ӧ�����ӷ���ʽΪ��Cr��OH��3+OH-=CrO2-+2H2O��
�ʴ�Ϊ��Cr��OH��3+OH-=CrO2-+2H2O��
��3������ȼ�ϵ���У���ȼ����븺����������NH3�����a����������������X����Ϊ���������ֱ���ŷŵ������У�˵��X�Դ�������Ⱦ�����XΪ�������ɸ�ȼ�ϵ��ʾ��ͼ��֪������Ӧ������ˮ�������Ǽ��Ե�أ�����������Ҳ���븺���缫��Ӧ������������д��������Ӧʽ��2NH3+6OH--6e-=N2+6H2O��
�ʴ�Ϊ������2NH3+6OH--6e-=N2+6H2O��
��A��һˮ�ϰ�Ϊ������ʣ���ˮϡ�ʹٽ���ˮ�ĵ��룬c��OH-����С����c��H+������A��ѡ��
B����ˮϡ�ʹٽ���ˮ�ĵ��룬��n��OH-������n��NH3?H2O����С������
����Bѡ��
C��c��H+��?c��OH-��=Kw�dz���������Ũ�ȵı仯���仯����C��ѡ��
D��c��NH4+��+c��H+��=c��OH-������ˮϡ����Һ��PH��С����c��OH-����С������c��NH4+��+c��H+����С����D��ѡ��
�ʴ�Ϊ��B��
��T���£�NH3?H2O�ĵ��볣��ΪKa��NH4+��ˮ��ƽ�ⳣ��ΪKh������¶���ˮ�����ӻ�����Kw=c��H+��?c��OH-��=
��
=Ka?Kh��
�ʴ�Ϊ��Ka?Kh��
��A����֪N2��g��+3H2��g���T2NH3��g����H=-92.2kJ?mol-1����H=����Ӧ�Ļ��-�淴Ӧ�Ļ��=-92.2kJ?mol-1�����淴Ӧ�Ļ��=����Ӧ�Ļ��+92.2kJ?mol-1�������淴Ӧ�Ļ�ܲ�С��92.2kJ?mol-1����A��ȷ��
B�����0��10s�ڣ�c��H2����С��0.75mol?L-1����c��NH3��������0.5mol?L-1������10s�ڰ�����ƽ����Ӧ����Ϊ��
=0.05mol?L-1?s-1����B����
C���淴Ӧ���з�Ӧ���Ũ�ȼ�С����Ӧ���ʼ�С������10s��15s��c��NH3��������С��0.25mol?L-1����C��ȷ��
D�������������Ũ�ȣ���Ӧ���ʼ�С�����ƽ����������NH3��ƽ��������Ӧ�����ƶ���v����С����D����
�ʴ�Ϊ��AC��
�ʴ�Ϊ��FeS��s��+Cu2+��aq��=CuS��s��+Fe2+��aq����2[c��S2-��+c��HS-��+c��H2S��]��
��2������������Ϣ��֪pH����10����c��OH-����10-4mol/Lʱ��Cr��OH��3���ܽ�����CrO2-���䷴Ӧ�����ӷ���ʽΪ��Cr��OH��3+OH-=CrO2-+2H2O��
�ʴ�Ϊ��Cr��OH��3+OH-=CrO2-+2H2O��
��3������ȼ�ϵ���У���ȼ����븺����������NH3�����a����������������X����Ϊ���������ֱ���ŷŵ������У�˵��X�Դ�������Ⱦ�����XΪ�������ɸ�ȼ�ϵ��ʾ��ͼ��֪������Ӧ������ˮ�������Ǽ��Ե�أ�����������Ҳ���븺���缫��Ӧ������������д��������Ӧʽ��2NH3+6OH--6e-=N2+6H2O��
�ʴ�Ϊ������2NH3+6OH--6e-=N2+6H2O��
��A��һˮ�ϰ�Ϊ������ʣ���ˮϡ�ʹٽ���ˮ�ĵ��룬c��OH-����С����c��H+������A��ѡ��
B����ˮϡ�ʹٽ���ˮ�ĵ��룬��n��OH-������n��NH3?H2O����С������
| c(OH-) |
| c(NH3?H2O) |
C��c��H+��?c��OH-��=Kw�dz���������Ũ�ȵı仯���仯����C��ѡ��
D��c��NH4+��+c��H+��=c��OH-������ˮϡ����Һ��PH��С����c��OH-����С������c��NH4+��+c��H+����С����D��ѡ��
�ʴ�Ϊ��B��
��T���£�NH3?H2O�ĵ��볣��ΪKa��NH4+��ˮ��ƽ�ⳣ��ΪKh������¶���ˮ�����ӻ�����Kw=c��H+��?c��OH-��=
| c(NH4+)?c(OH-) |
| c(NH3?H2O) |
| c(NH3?H2O)?c(H+) |
| c(NH4+) |
�ʴ�Ϊ��Ka?Kh��
��A����֪N2��g��+3H2��g���T2NH3��g����H=-92.2kJ?mol-1����H=����Ӧ�Ļ��-�淴Ӧ�Ļ��=-92.2kJ?mol-1�����淴Ӧ�Ļ��=����Ӧ�Ļ��+92.2kJ?mol-1�������淴Ӧ�Ļ�ܲ�С��92.2kJ?mol-1����A��ȷ��
B�����0��10s�ڣ�c��H2����С��0.75mol?L-1����c��NH3��������0.5mol?L-1������10s�ڰ�����ƽ����Ӧ����Ϊ��
| 0.5mol?L-1 |
| 10s |
C���淴Ӧ���з�Ӧ���Ũ�ȼ�С����Ӧ���ʼ�С������10s��15s��c��NH3��������С��0.25mol?L-1����C��ȷ��
D�������������Ũ�ȣ���Ӧ���ʼ�С�����ƽ����������NH3��ƽ��������Ӧ�����ƶ���v����С����D����
�ʴ�Ϊ��AC��
���������⿼���˳�����ת�������ӷ���ʽ����д��������ʵĵ��롢��Ӧ���ʵļ��㡢Ӱ��ƽ������ʵ����صȣ������Ѷ��еȣ������漰��֪ʶ��϶࣬ע�����ջ�ѧƽ����й�֪ʶ����ȷ����ƽ�ⳣ����ˮ�ⳣ����ˮ�����ӻ�����֮��Ĺ�ϵ��

��ϰ��ϵ�д�
�����Ŀ
�����йػ�ѧ����ʹ����ȷ���ǣ�������
A����ԭ�ӵ�ԭ�ӽṹʾ��ͼ�� | ||
B��NH3���ӵĵ���ʽ��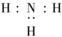 | ||
C��ԭ�Ӻ�����8�����ӵ���ԭ�ӣ�
| ||
| D�������Ľṹʽ��N��N |
���е��뷽��ʽ��д������ǣ�������
| A��Na2CO3=2Na++CO32- |
| B��NaHSO4=Na++H++SO42- |
| C��H2SO4=H++SO42- |
| D��KClO3=K++ClO3- |
��NA��ʾ�����ӵ�������ֵ��������������ȷ���ǣ�������
| A��16g O3��16g O2������ͬ����ԭ���� |
| B��2.3g Na+�к��еĵ�����Ϊ0.1NA |
| C��1mol O2������ԭ����ΪNA |
| D��2.4gþ��ΪMg2+ʱʧȥ�ĵ�����Ϊ0.1NA |
�ṹΪ��-CH=CH-CH=CH-CH=CH-CH=CH-���ĸ߷��ӻ������õ������������䵼�������������ߣ������߷��ӻ�����ĵ����ǣ�������
| A����Ȳ | B����ϩ |
| C����ϩ | D��1��3-����ϩ |
 ϵͳ����Ϊ
ϵͳ����Ϊ