题目内容
已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增加.相关信息如表所示,根据推断回答下列问题:(答题时A、B、C、D、E用所对应的元素符号表示)
(1)C在周期表中位于第 周期第 族,E基态原子核外电子排布式是
(2)A、B、D三种元素电负性由大到小排列顺序为 ,其中A的最高价氯化物构成晶体的微粒间作用力为
(3)A和B的最简单氢化物中较稳定的是 (填化学式).B的最简单氢化物和E的黑色氧化物固体在加热时可反应,写出其反应方程式
(4)E的单质和过氧化氢在稀硫酸中可反应,有人将这个反应设计成原电池,请写出正极反应方程式
(5)煤燃烧产生的烟气中有B的氧化物,会引起严重的环境问题,因此,常用AH4催化还原以消除污染,已知:
AH4(g)+2BO2(g)═B2(g)+AO2(g)+2H2O(g)△H1=-867kJ/mol
2BO2(g)?B2O4(g)△H2=-56.9kJ/mol
写出AH4和B2O4反应的热化学方程式 .
| A | A的最高价氧化物对应的水化物化学式为H2AO3 |
| B | B元素的第一电离能比同周期相邻两个元素都大 |
| C | C原子在同周期原子中半径最大(稀有气体除外),其单质焰色为黄色 |
| D | D的基态原子最外层电子排布式为3s23p2 |
| E | E与C位于不同周期,E原子核外最外层电子数与C相同,其余各层电子均充满 |
(2)A、B、D三种元素电负性由大到小排列顺序为
(3)A和B的最简单氢化物中较稳定的是
(4)E的单质和过氧化氢在稀硫酸中可反应,有人将这个反应设计成原电池,请写出正极反应方程式
(5)煤燃烧产生的烟气中有B的氧化物,会引起严重的环境问题,因此,常用AH4催化还原以消除污染,已知:
AH4(g)+2BO2(g)═B2(g)+AO2(g)+2H2O(g)△H1=-867kJ/mol
2BO2(g)?B2O4(g)△H2=-56.9kJ/mol
写出AH4和B2O4反应的热化学方程式
考点:位置结构性质的相互关系应用,不同晶体的结构微粒及微粒间作用力的区别,热化学方程式
专题:化学反应中的能量变化,元素周期律与元素周期表专题
分析:A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增加,C原子在同周期原子中半径最大(稀有气体除外),其单质焰色为黄色,则C为Na;A的最高价氧化物对应的水化物化学式为H2AO3,最高正价为+4,原子序数小于Na,故A为碳元素;B的原子序数介于碳、氧之间,则B为N元素,第一电离能高于碳、氧;D的基态原子最外层电子排布式为3s23p2,则D为Si;E与C位于不同周期,原子序数对C(Na),则E处于第四周期,E原子核外最外层电子数与C相同,其余各层电子均充满,原子核外电子数=2+8+18+1=29,则E为Cu,据此解答.
解答:
解:A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增加,C原子在同周期原子中半径最大(稀有气体除外),其单质焰色为黄色,则C为Na;A的最高价氧化物对应的水化物化学式为H2AO3,最高正价为+4,原子序数小于Na,故A为碳元素;B的原子序数介于碳、氧之间,则B为N元素,第一电离能高于碳、氧;D的基态原子最外层电子排布式为3s23p2,则D为Si;E与C位于不同周期,原子序数对C(Na),则E处于第四周期,E原子核外最外层电子数与C相同,其余各层电子均充满,原子核外电子数=2+8+18+1=29,则E为Cu,
(1)C为Na,在周期表中位于第三周期第ⅠA族,E为Cu,基态原子核外电子排布式是:1s22s22p63s23p63d104s1,
故答案为:三、ⅠA;1s22s22p63s23p63d104s1;
(2)C、N、Si同周期,随原子序数增大电负性增大,同主族自上而下电负性减小,故电负性由大到小顺序为:N>C>Si,其中A的最高价氯化物为CCl4,形成分子晶体,构成晶体的微粒间作用力为:范德华力,
故答案为:N>C>Si;范德华力;
(3)非金属性C<N,故最简单氢化物中NH3较稳定,氨气与CuO反应生成Cu氮气与水,其化学反应方程式 为:3CuO+2NH3
N2+3Cu+3H2O,
故答案为:NH3;3CuO+2NH3
N2+3Cu+3H2O;
(4)Cu的单质和过氧化氢在稀硫酸中可反应,正极发生还原反应,过氧化氢在正极获得电子,在氢离子参与反应下生成水,正极电极反应式为:H2O2+2e-+2H+=2H2O,
故答案为:H2O2+2e-+2H+=2H2O;
(5)已知:①、CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g)△H1=-867kJ/mol
②、2NO2(g)?N2O4(g)△H2=-56.9kJ/mol
由盖斯定律,①-②得:CH4(g)+N2O4(g)═N2(g)+CO2(g)+2H2O(g)△H=-810.1kJ/mol,
故答案为:CH4(g)+N2O4(g)═N2(g)+CO2(g)+2H2O(g)△H=-810.1kJ/mol.
(1)C为Na,在周期表中位于第三周期第ⅠA族,E为Cu,基态原子核外电子排布式是:1s22s22p63s23p63d104s1,
故答案为:三、ⅠA;1s22s22p63s23p63d104s1;
(2)C、N、Si同周期,随原子序数增大电负性增大,同主族自上而下电负性减小,故电负性由大到小顺序为:N>C>Si,其中A的最高价氯化物为CCl4,形成分子晶体,构成晶体的微粒间作用力为:范德华力,
故答案为:N>C>Si;范德华力;
(3)非金属性C<N,故最简单氢化物中NH3较稳定,氨气与CuO反应生成Cu氮气与水,其化学反应方程式 为:3CuO+2NH3
| ||
故答案为:NH3;3CuO+2NH3
| ||
(4)Cu的单质和过氧化氢在稀硫酸中可反应,正极发生还原反应,过氧化氢在正极获得电子,在氢离子参与反应下生成水,正极电极反应式为:H2O2+2e-+2H+=2H2O,
故答案为:H2O2+2e-+2H+=2H2O;
(5)已知:①、CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g)△H1=-867kJ/mol
②、2NO2(g)?N2O4(g)△H2=-56.9kJ/mol
由盖斯定律,①-②得:CH4(g)+N2O4(g)═N2(g)+CO2(g)+2H2O(g)△H=-810.1kJ/mol,
故答案为:CH4(g)+N2O4(g)═N2(g)+CO2(g)+2H2O(g)△H=-810.1kJ/mol.
点评:本题考查结构性质位置关系应用,题目比较综合,涉及核外电子排布、电负性、原电池、热化学方程式等,侧重考查学生对知识的迁移应用,难度中等.

练习册系列答案
相关题目
设NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A、在标况下,11.2L NO与11.2L O2混合后所含分子数为0.75NA |
| B、常温常压下,16g O3所含的电子数为8NA |
| C、0.1mol Na2O2晶体中含有0.4NA个离子 |
| D、铝跟氢氧化钠溶液反应生成1mol氢气时,转移的电子数为NA |
分子式为C9H11Cl的有机物,属于芳香族化合物且苯环上具有两个取代基的化合物共有(不考虑立体异构)( )
| A、9种 | B、12种 |
| C、15种 | D、18种 |
下列反应的离子方程式书写正确的是( )
| A、NaAlO2溶液中通入少量CO2:2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- |
| B、向FeBr2溶液中滴加足量的氯水:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- |
| C、向40mL、8mol/L的硝酸溶液中加入5.6 g铁粉:Fe+4H++NO3-═Fe3++NO↑+2H2O |
| D、Mg(HCO3)2溶液中加入过量石灰水:Mg2++2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+MgCO3↓ |
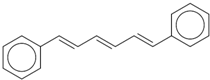 美国马丁?卡普拉等三位科学家因“在开发多尺度复杂化学系统模型”方面所做的贡献,获得了2013年诺贝尔化学奖.他们模拟出了1,6-二苯基-1,3,5-己三烯的分子模型,其结构简式如图所示.下列说法正确的是( )
美国马丁?卡普拉等三位科学家因“在开发多尺度复杂化学系统模型”方面所做的贡献,获得了2013年诺贝尔化学奖.他们模拟出了1,6-二苯基-1,3,5-己三烯的分子模型,其结构简式如图所示.下列说法正确的是( )| A、该有机物属于芳香烃,与苯互为同系物 |
| B、该有机物的分子式为C18H18 |
| C、1mol该有机物在常温下最多能与9mol Br2发生加成反应 |
| D、该有机物可以发生氧化反应、取代反应、加成反应 |
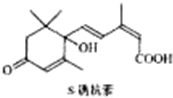 对盆栽鲜花施用S-诱抗素制剂,可以保持鲜花盛开.S-诱抗素的分子结构如图,则1mol该物质与足量的NaOH溶液反应时最多可消耗NaOH的物质的量为( )
对盆栽鲜花施用S-诱抗素制剂,可以保持鲜花盛开.S-诱抗素的分子结构如图,则1mol该物质与足量的NaOH溶液反应时最多可消耗NaOH的物质的量为( )| A、1mol | B、2mol |
| C、3mol | D、4mol |
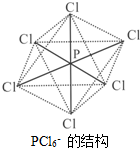 氮、磷属于同主族元素,广泛存在于生产生活的各种物质中.
氮、磷属于同主族元素,广泛存在于生产生活的各种物质中. M、N、O、P、Q是元素周期表中原子序数依次递增的前四周期元素.M原子最外层电子数为内层电子数的3倍;N的焰色反应呈黄色;O的氢化物是一种强酸,其浓溶液可与M、Q的化合物反应生成O的单质;P是一种金属元素,其基态原子中有6个未成对电子.请回答下列问题:
M、N、O、P、Q是元素周期表中原子序数依次递增的前四周期元素.M原子最外层电子数为内层电子数的3倍;N的焰色反应呈黄色;O的氢化物是一种强酸,其浓溶液可与M、Q的化合物反应生成O的单质;P是一种金属元素,其基态原子中有6个未成对电子.请回答下列问题: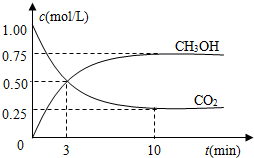 随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.
随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.