题目内容
4.KNO3是重要的化工产品,下面是一种已获得专利的KN03制备方法的主要步骤: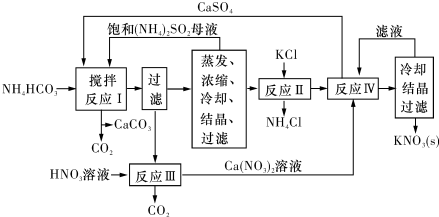
(1)反应工中,CaS04与NH4 HCO3的物质的量之比为1:2,该反应的化学方程式为CaSO4+2NH4HCO3=CaCO3↓+(NH4)2SO4+H2O+CO2↑.
(2)反应Ⅱ需在干态、加热的条件下进行,加热的目的是分离NH4Cl与K2SO4,加快化学反应速率;
(3)从反应Ⅳ所得混合物中分离出CaS04的方法是趁热过滤,趁热过滤的目的是防止KNO3结晶,提高KNO3的产率.
(4)整个流程中,可循环利用的物质有(NH4)2SO4、CaSO4、KNO3(填化学式).
(5)将硝酸与浓KC1溶液混合,也可得到KNO3,同时生成等体积的气体A和气体B(NOCl),该反应的化学方程式为NOCl.
分析 反应Ⅰ中,CaSO4与NH4HCO3的物质的量之比为1:2,由流程题可知生成CaCO3、(NH4)2SO4和CO2,过滤后在滤液的主要成分为(NH4)2SO4,加入KCl,在干态、加热的条件下进行,分离出氯化铵,可得硫酸钾,在滤液中加入硝酸钙,可得到硫酸钙和硝酸钾,经过滤、蒸发、浓缩结晶可得硝酸钾,以此解答该题.
解答 解:(1)反应Ⅰ中,CaSO4与NH4HCO3的物质的量之比为1:2,由流程题可知生成CaCO3、(NH4)2SO4和CO2,由质量守恒可知反应的方程式为CaSO4+2NH4HCO3=CaCO3↓+(NH4)2SO4+H2O+CO2↑,
故答案为:CaSO4+2NH4HCO3=CaCO3↓+(NH4)2SO4+H2O+CO2↑;
(2)(NH4)2SO4加入KCl,在干态、加热的条件下进行,可生成易分解的氯化铵,加热时氯化铵分解生成氯化氢和氨气,温度降低又生成氯化铵,以此可分离出氯化铵,得硫酸钾,且能加快反应的速率;故答案为:分离NH4Cl与K2SO4,加快化学反应速率;
(3)从反应Ⅳ所得混合物中分离出CaSO4的方法是趁热过滤,趁热过滤的目的是防止KNO3结晶,提高KNO3的产率,
故答案为:防止KNO3结晶,提高KNO3的产率;
(4)整个流程中,可循环利用的物质除(NH4)2SO4外,还有CaSO4、KNO3,故答案为:(NH4)2SO4、CaSO4、KNO3;
(5)硝酸与浓KC1反应生成硝酸钾和氯气以及NOCl,反应的化学方程式为4HNO3+3KCl=NOCl↑+Cl2↑+3KNO3++2H2O,
故答案为:4HNO3+3KCl=NOCl↑+Cl2↑+3KNO3++2H2O.
点评 本题考查物质的制备实验方案的设计,侧重于学生的分析能力、实验能力和计算能力的考查,为高考常见题型,注意根据流程图把握实验的原理和操作方法,难度较大.

| A. | 推广“低碳经济”,减少温室气体的排放 | |
| B. | 开发太阳能、风能和氢能等能源代替化石燃料,有利于节约资源、保护环境 | |
| C. | 采用“绿色化学”工艺,使原料尽可能转化为所需要的物质 | |
| D. | 关停化工企业,消除污染源头 |
| A. | pH均为12的烧碱溶液与Ba(OH)2溶液的物质的量浓度之比 | |
| B. | (NH4)2SO4溶液中c(NH4+)与c(SO42-)之比 | |
| C. | 0.2mol/L的CH3COOH溶液与0.1mol/L和CH3COOH溶液中c(H+)之比 | |
| D. | 0.2mol/L的HCl与0.1mol/LHNO3溶液中n(H+)之比 |
| A. | 此白色固体不可能是KHCO3和KOH的混合物 | |
| B. | 此白色固体中含有K2CO36.90g | |
| C. | 原KOH溶液的物质的量浓度是0.500 mol•L-1 | |
| D. | 此白色固体可能为KOH和K2CO3的混合物 |
| A. | 铜片插入硝酸银溶液中:Cu+Ag+═Cu2++Ag | |
| B. | 碳酸氢钙与过量的NaOH溶液反应:Ca2++2HCO3-+2OH-═CaCO3↓+2H2O+CO32- | |
| C. | 用稀硝酸除去试管内壁银:Ag+2H++NO3-═Ag++NO2↑+H2O | |
| D. | 向氨水中通入过量SO2:SO2+2NH3•H2O═2NH4++SO32-+H2O |
| A. | SiH4分子呈正四面体形 | |
| B. | SiH4分子是非极性分子 | |
| C. | 因为Si-H键键能比C-H键键能低,所以SiH4沸点低于CH4沸点 | |
| D. | SiH4分子稳定性低于CH4分子,因为C-H键键能高 |
| A. | PCl3的水解产物是PH3和HCl | B. | CuCl2的水解产物是Cu(OH)2和HCl | ||
| C. | NaClO的水解产物是HClO和NaOH | D. | CaO2的水解产物是Ca(OH)2和H2O2 |
| A. | NaHCO3═Na++H++CO32- | B. | NaHSO4═Na++HSO4- | ||
| C. | Al2 (SO4)3═Al 3++SO42- | D. | Na2SO4═2Na++SO42 |
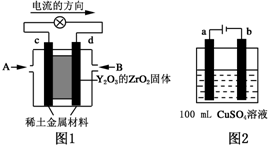 (1)科学家制造出一种使用固体电解质的燃料电池,其效率更高,可用于航空航天.如图1所示装置中,以稀土金属材料为惰性电极,在两极上分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO2固体,它在高温下能传导阳极生成的O2-(O2+4e--→2O2-).
(1)科学家制造出一种使用固体电解质的燃料电池,其效率更高,可用于航空航天.如图1所示装置中,以稀土金属材料为惰性电极,在两极上分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO2固体,它在高温下能传导阳极生成的O2-(O2+4e--→2O2-).