题目内容
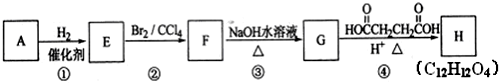
9.乙烯是石油化学工业最重要的基础原料,用乙烯可以制得许多工业材料和日用品,乙烯能发生下列转化关系: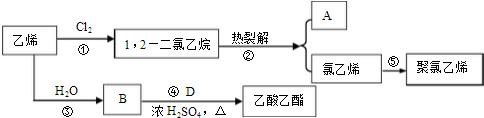
(1)反应①的化学方程式为:CH2=CH2+Cl2→CH2Cl-CH2Cl该反应属于加成反应.
(2)B中所含官能团的电子式为
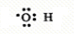 ,D中官能团的名称为羧基.
,D中官能团的名称为羧基.(3)已知氯乙烯不溶于水.沸点为-13.9℃,则反应②产物A分离的方法为蒸馏;聚氯乙烯(PVC)曾是世界上产量最大的通用塑料,应用非常广泛.关于聚氯乙烯的说法正确的是B.
A.属于纯净物 B.可以燃烧 C.能使溴水褪色 D.可用作食品保鲜膜.
分析 乙烯与水发生加成反应生成B为CH3CH2OH,乙醇与D发生酯化反应生成乙酸乙酯,故D为CH3COOH.乙烯与氯气发生加成反应生成1,2-二氯乙烷,1,2-二氯乙烷发生热裂解得到A与氯乙烯,则A为HCl,氯乙烯发生加聚反应生成聚氯乙烯,以此解答该题.
解答 解:乙烯与水发生加成反应生成B为CH3CH2OH,乙醇与D发生酯化反应生成乙酸乙酯,故D为CH3COOH.乙烯与氯气发生加成反应生成1,2-二氯乙烷,1,2-二氯乙烷发生热裂解得到A与氯乙烯,则A为HCl,氯乙烯发生加聚反应生成聚氯乙烯,
(1)反应①是乙烯与氯气发生加成反应生成1,2-二氯乙烷,反应方程式为:CH2=CH2+Cl2→CH2Cl-CH2Cl,故答案为:CH2=CH2+Cl2→CH2Cl-CH2Cl;加成;
(2)B为乙醇,官能团为羟基,电子式为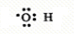 ,D为乙酸,含有的官能团为羧基,故答案为:
,D为乙酸,含有的官能团为羧基,故答案为: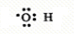 ;羧基;
;羧基;
(3)氯乙烯不溶于水,沸点为-13.9℃,反应②在加热的条件下生成氯化氢和氯乙烯气体,因氯乙烯的沸点较高,可用蒸馏的方法分离,聚氯乙烯为高聚物,属于混合物,不含碳碳双键,则与溴水不反应,可燃烧,聚乙烯不能用于保鲜膜,含有的添加剂以及受热释放出的物质对人体有害,
故答案为:蒸馏;B.
点评 本题考查有机物推断、石油化工等,为高频考点,侧重于学生的分析能力的考查,涉及烯烃、醇、羧酸的性质与转化,题目基础性强,注意对基础知识的理解掌握.

练习册系列答案
相关题目
20.向含有下列各组离子的溶液中滴加NaOH溶液,得到白色沉淀的是( )
| A. | Ba2+ HCO3- K+ Cl- | B. | CO32- OH- Na+ NO3- | ||
| C. | OH- Na+ SO42- CO32- | D. | Cu2+ Cl- Na+ NO3- |
17.能正确表示下列反应的离子方程式的是( )
| A. | NH4Fe(SO4)2加入过量NaOH溶液中::NH4++Fe3++4OH-═NH3•H2O+Fe(OH)3↓ | |
| B. | 次氯酸钠溶液中通入过量的二氧化硫:ClO-+SO2+H2O═HSO3-+HClO | |
| C. | Ba(OH)2溶液和稀硫酸反应:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| D. | 澄清的石灰水中加入过量的NaHCO3溶液:Ca2++OH-+HCO3-═CaCO3↓+H2O |
4.下列说法中正确的是( )
| A. | 有离子键的化合物中一定没有共价键 | |
| B. | 有共价键的化合物中一定没有离子键 | |
| C. | 物质的熔化过程可能既破坏离子键又破坏共价键 | |
| D. | 物质的熔化过程可能不破坏任何化学键 |
8.山梨酸是应用广泛的食品防腐剂,其结构如图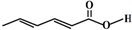 ,下列关于山梨酸的说法错误的是( )
,下列关于山梨酸的说法错误的是( )
 ,下列关于山梨酸的说法错误的是( )
,下列关于山梨酸的说法错误的是( )| A. | 分子式为C7H8O2 | |
| B. | 1mol该物质最多可与2mol Br2发生加成反应 | |
| C. | 可使酸性KMnO4溶液褪色 | |
| D. | 可与醇发生取代反应 |
 .
.
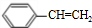 +Br2→
+Br2→