题目内容
下列电离方程式书写正确的是( )
| A、Ca(OH)2?Ca2++2OH- |
| B、H2SO3?2H++SO32- |
| C、NaHS?Na++HS- |
| D、HCO3-?H++CO32- |
考点:电离方程式的书写
专题:离子反应专题
分析:强电解质完全电离,用等号,弱电解质部分电离,用可逆号,多元弱酸分部电离,以第一步为主.
解答:
解:A.氢氧化钙为强电解质,完全电离生成钙离子和氢氧根离子,电离方程式为:Ca(OH)2=Ca2++2OH-,故A错误;
B.亚硫酸为多元弱酸,分部电离,以第一步为主,电离方程式:H2SO3?H++HSO3-,故B错误;
C.NaHS为强电解质,完全电离生成钠离子和硫氢根离子,电离方程式为:NaHS=Na++HS-,故C错误;
D.碳酸为多元弱酸的酸式根离子,部分电离生成氢离子和碳酸根离子,电离方程式为:HCO3-?H++CO32-,故D正确;
故选:D.
B.亚硫酸为多元弱酸,分部电离,以第一步为主,电离方程式:H2SO3?H++HSO3-,故B错误;
C.NaHS为强电解质,完全电离生成钠离子和硫氢根离子,电离方程式为:NaHS=Na++HS-,故C错误;
D.碳酸为多元弱酸的酸式根离子,部分电离生成氢离子和碳酸根离子,电离方程式为:HCO3-?H++CO32-,故D正确;
故选:D.
点评:本题考查了电离方程式的判断,明确电解质的强弱、掌握正确书写电离方程式的方法是解题关键,注意多元弱酸分步电离.

练习册系列答案
相关题目
对水垢的主要成分是CaCO3和Mg(OH)2而不是CaCO3和MgCO3的解释正确的是( )
| A、Mg(OH)2的溶度积大于MgCO3的溶度积,且在水中发生了沉淀转化 |
| B、Mg(OH)2的溶度积小于MgCO3的溶度积,且在水中发生了沉淀转化 |
| C、MgCO3电离出的CO32-发生水解,使水中OH-浓度减小,对Mg(OH)2的沉淀溶解平衡而言,Qc<Ksp生成Mg(OH)2沉淀 |
| D、MgCO3电离出的CO32-发生水解,使水中OH-浓度增大,对Mg (OH)2的沉淀溶解平衡而言,Qc>Ksp生成Mg(OH)2沉淀 |
在8NH3+3Cl2═6NH4Cl+N2反应中,若有2mol N2生成,发生氧化反应的物质的量是( )
| A、16 mol NH3 |
| B、8 mol NH3 |
| C、4 mol NH3 |
| D、3 mol NH3 |
(1)已知氢气的燃烧热为285.8kJ/mol,则H2(g)+
O2(g)═H2O(l)△H= ;
(2)用离子方程式来表示强酸和强碱的中和热(焓变的数值为57.3):
H+(aq)+ ═ ,△H= .
| 1 |
| 2 |
(2)用离子方程式来表示强酸和强碱的中和热(焓变的数值为57.3):
H+(aq)+
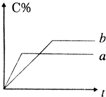 可逆反应A(s)+B(g)?n C (g)△H=Q (n为正整数)在不同条件下反应混合物中C的百分含量和反应过程所需时间的关系曲线如右图所示.下列有关叙述中一定正确的是( )
可逆反应A(s)+B(g)?n C (g)△H=Q (n为正整数)在不同条件下反应混合物中C的百分含量和反应过程所需时间的关系曲线如右图所示.下列有关叙述中一定正确的是( )| A、其他条件相同,a表示使用了催化剂,b没有使用催化剂 |
| B、其他条件相同,若只改变压强,则a比b的压强大且n≥2 |
| C、其他条件相同,若只改变温度,则a比b的温度高且Q>0 |
| D、其他条件相同,a表示减少A的物质的量 |
根据厦门气象台报道,近年每到春季,厦门市经常出现大雾天气,致使高速公路关闭,航班停飞.雾属于下列分散系中的( )
| A、溶液 | B、悬浊液 |
| C、乳浊液 | D、胶体 |