题目内容
16.为验证卤素单质氧化性的相对强弱,某小组用如图所示装置进行实验(夹持、加热仪器已略去,气密性已检验).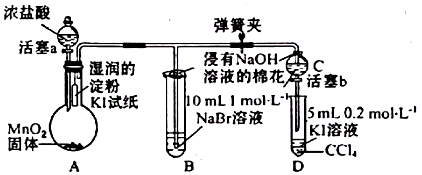
实验过程;
I.打开弹簧夹,打开活塞a,清加浓盐酸.
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹.
Ⅲ.当B中溶液由黄色变为棕色时,关闭活塞a.
Ⅳ…
(1)A中产生的是黄绿色气体,其离子方程式为4HCl(浓)+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,在该反应中浓盐酸表现了酸性、还原性.
(2)验证氯气的氧化性强于碘的实验现象是湿润的淀粉KI试纸变蓝.
(3)B中溶液发生反应的离子方程式是Cl2+2Br-═Br2+2Cl-.
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是打开活塞b,将少量C中溶液滴入D中,关闭活塞b,取下D振荡.静止后CCl4层溶液变为紫红色.
(5)浸有NaOH溶液的棉花作用是吸收尾气,防止氯气污染空气;离子方程式为Cl2+2OH-═Cl-+ClO-+H2O.
(6)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下原子半径逐渐增大,得电子能力逐渐减弱.
分析 验证卤素单质氧化性的相对强弱,装置A:二氧化锰和浓盐酸加热反应生成氯化锰、氯气和水,装置A中生成氯气,烧瓶上端湿润的碘化钾淀粉试纸变蓝色,验证氯气的氧化性强于碘,装置B:装置B中盛有溴化钠,氯气进入装置B中,氯气氧化溴离子为溴单质,溶液呈橙红色,验证氯的氧化性强于溴,氯气有毒,能被氢氧化钠吸收,浸有氢氧化钠的棉花防止氯气污染空气,当B和C中的溶液都变为黄色时,夹紧弹簧夹,为验证溴的氧化性强于碘,实验时应避免氯气的干扰,当B中溶液由黄色变为棕红色时,说明有大量的溴生成,此时应关闭活塞a,否则氯气过量,影响实验结论.
(1)氯气颜色为黄绿色,高锰酸钾具有强氧化性,与浓盐酸反应生成氯气;
(2)氯气氧化性强于单质碘,碘遇淀粉变蓝色;
(3)氯气的氧化性强于溴,将氯气通入NaBr溶液中会有单质溴生成;
(4)如CCl4层溶液变为紫红色,则说明有碘生成;
(5)浸有NaOH溶液的棉花作用是吸收剩余氯气,氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水;
(6)从原子结构(电子层数、原子半径)的角度分析.
解答 解:验证卤素单质氧化性的相对强弱,装置A:二氧化锰和浓盐酸加热反应生成氯化锰、氯气和水,装置A中生成氯气,烧瓶上端湿润的碘化钾淀粉试纸变蓝色,验证氯气的氧化性强于碘,装置B:装置B中盛有溴化钠,氯气进入装置B中,氯气氧化溴离子为溴单质,溶液呈橙红色,验证氯的氧化性强于溴,氯气有毒,能被氢氧化钠吸收,浸有氢氧化钠的棉花防止氯气污染空气,当B和C中的溶液都变为黄色时,夹紧弹簧夹,为验证溴的氧化性强于碘,实验时应避免氯气的干扰,当B中溶液由黄色变为棕红色时,说明有大量的溴生成,此时应关闭活塞a,否则氯气过量,影响实验结论.
(1)黄绿色气体为氯气,由二氧化锰和浓盐酸加热发生氧化还原反应生成氯化锰、氯气和水,方程式为:4HCl(浓)+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,反应中浓盐酸做酸和还原剂,
故答案为:4HCl(浓)+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;酸性、还原;
(2)淀粉变蓝色,说明有单质碘生成,说明氯气氧化性强于单质碘,
故答案为:湿润的淀粉KI试纸变蓝;
(3)氯气的氧化性强于溴,将氯气通入NaBr溶液中会有单质溴生成,发生反应的离子方程式为Cl2+2Br-═Br2+2Cl-,
故答案为:Cl2+2Br-═Br2+2Cl-;
(4)为验证溴的氧化性强于碘,应将C中生成的溴加入到盛有KI溶液的D中,如发生氧化还原反应,则静至后CCl4层溶液变为紫红色,
故答案为:打开活塞b,将少量C中溶液滴入D中,关闭活塞b,取下D震荡,静至后CCl4层溶液变为紫红色;
(5)浸有NaOH溶液的棉花作用是吸收尾气,防止氯气污染空气,离子方程式为:Cl2+2OH-═Cl-+ClO-+H2O,
故答案为:吸收尾气,防止氯气污染空气; Cl2+2OH-═Cl-+ClO-+H2O;
(6)因同一主族元素,从上到下,电子层数依次增多,原子半径逐渐增大,元素的金属性逐渐增强,得电子能力逐渐减弱,
故答案为:原子半径逐渐增大.
点评 本题主要考查卤素单质氧化性的相对强弱的验证,根据实验现象并用卤素性质进行解释是解答关键,注意要排除干扰因素的存在,题目难度中等.

 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案| A. | 标准状况下,22.4 LH2O中含有极性键的数目为2NA | |
| B. | 78 g Na2O2中含有的阴离子数为NA | |
| C. | 11 g重水(D218O)中含有的电子数力5NA | |
| D. | 常温常压下,5.6 g铁粉在7.1 g氯气中充分燃烧,转移的电子数为0.2NA |
①该电池负极的电极反应式为CH3OH-6e-+8OH-=CO32-+6H2O.
②若以该电池为电源,用石墨作电极电解200mL含有如下离子的溶液.
| 离子 | Cu2+ | H+ | Cl- | SO42- |
| c/(mol•L-1) | 0.5 | 2 | 2 | 0.5 |
| 实验方案 | 实验现象 |
| ①用砂纸打磨后的镁带与沸水反应;再向反应液中滴加酚酞 | 产生气体,气体可燃,溶液变浅红色 |
| ②向新制得Na2S饱和溶液中滴加新制氯水 | 生成淡黄色沉淀 |
| ③钠与滴有酚酞试液的冷水反应 | 浮于水面上,熔成小球,四处游动,逐渐缩小,溶液变红色 |
| ④镁带与2mol/L的盐酸反应 | 剧烈反应,产生的气体可燃 |
| ⑤铝条与2mol/L的盐酸反应 | 反应不十分剧烈;产生的气体可燃 |
| ⑥向AlCl3溶液中滴加NaOH溶液至过量 | 先生成白色絮状沉淀,最后沉淀全部溶解 |
| 实验方案 | 实验现象 | 有关离子方程式 |
| ① | 不填 | 不填 |
| ② | S2-+Cl2=S↓+2Cl- | |
| ③ | 不填 | 2Na+2H2O=2Na++2OH-+H2↑ |
| ④ | 不填 | 不填 |
| ⑤ | 不填 | 2Al+6H+=2Al3++3H2↑ |
| ⑥ | 先生成白色絮状沉淀,最后沉淀全部溶解 | Al3++3OH-=Al(OH)3↓,Al(OH)3+OH-=AlO2-+2H2O |
(2)实验用品:略.
(3)实验内容:(填写题给信息表中相应的实验现象,并在有空格处写出相对应的离子方程式)
(4)实验结论:同周期元素随原子序数的增大,元素的金属性逐渐减弱,而非金属性逐渐增强.
(5)问题与讨论:
请从原子结构理论上简单说明具有上述结论的原因是同周期元素随核电荷数的增加,原子核对核外电子的束缚力增强,原子半径减小,原子失电子能力减弱,而得到电子能力增强,即元素金属性逐渐减弱,二非金属性逐渐增强.
| A. | 绿色植物的光合作用是把热能转化为化学能的过程 | |
| B. | 生物能是与化学反应无关的一种能源 | |
| C. | 化学能只能以热能的形式释放 | |
| D. | 葡萄糖在人体内的氧化是放热反应 |
| A. | HA是强酸 | |
| B. | 混合液中,c(HA)+c(A-)=0.4mol•L-1 | |
| C. | 混合液中,c(Na+)+c(H+)=$\frac{Ka(HA)•c(HA)+Kw}{c({H}^{+})}$ | |
| D. | 向混合液中加入蒸馏水,c(A-)与c(HA)的比值将增大 |
| A. | SO2使品红、酸性高锰酸钾溶液褪色,均体现SO2的漂白性 | |
| B. | 完全由非金属元素组成的化合物不一定是共价化合物 | |
| C. | 元素周期表有18列,就有18个族 | |
| D. | SO2的水溶液能导电,所以SO2是电解质 |
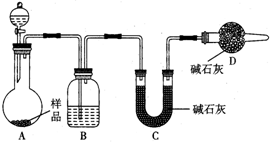 为测定放置已久的小苏打样品中纯碱的质量分数,设计如下实验方案:
为测定放置已久的小苏打样品中纯碱的质量分数,设计如下实验方案: