题目内容
已知Fe(OH)3能与次氯酸盐发生如下反应(未配平):Fe(OH)3+ClO-+OH-→FeO4n-+Cl-+H2O
(1)已知有10.7gFe(OH)3参加反应,共转移了0.3NA个电子,则n= ,FeO4n- 中铁元素的化合价为 .
(2)根据所学的知识,推测FeO4n-能和下列 (填序号)物质反应.
A、KMnO4 B、SO2 C、H2S D、O2.
(1)已知有10.7gFe(OH)3参加反应,共转移了0.3NA个电子,则n=
(2)根据所学的知识,推测FeO4n-能和下列
A、KMnO4 B、SO2 C、H2S D、O2.
考点:氧化还原反应
专题:氧化还原反应专题
分析:(1)10.7gFe(OH)3的物质的量=
=0.1mol,0.1mol氢氧化铁完全反应转移0.3NA个电子,则转移电子的物质的量为0.3mol,物质的量之比等于其个数之比,所以每个三价铁失去3个电子,则高铁酸根离子中Fe显+6价,据此判断n;
(2)高铁酸根离子具有强氧化性,能和强还原性微粒反应.
| 10.7g |
| 107g/mol |
(2)高铁酸根离子具有强氧化性,能和强还原性微粒反应.
解答:
解:(1)10.7gFe(OH)3的物质的量=
=0.1mol,0.1mol氢氧化铁完全反应转移0.3NA个电子,则转移电子的物质的量为0.3mol,物质的量之比等于其个数之比,则氢氧化铁和转移电子个数之比为1:3,所以每个三价铁失去3个电子,则高铁酸根离子中Fe显+6价,所以n为2,
故答案为:2;+6;
(2)高铁酸根离子中Fe元素为+6价,为最高化合价,所以高铁酸根离子具有强氧化性,能和强还原性微粒反应,高锰酸钾、氧气都具有强氧化性,所以高铁酸根离子和高锰酸钾、氧气不反应,二氧化硫和硫化氢具有还原性,所以能被高铁酸根离子氧化,故选BC.
| 10.7g |
| 107g/mol |
故答案为:2;+6;
(2)高铁酸根离子中Fe元素为+6价,为最高化合价,所以高铁酸根离子具有强氧化性,能和强还原性微粒反应,高锰酸钾、氧气都具有强氧化性,所以高铁酸根离子和高锰酸钾、氧气不反应,二氧化硫和硫化氢具有还原性,所以能被高铁酸根离子氧化,故选BC.
点评:本题考查氧化还原反应,同时考查学生运用知识解决问题能力,知道元素化合价与物质氧化性和还原性的关系,题目难度不大.

练习册系列答案
相关题目
用NA表示阿伏加德罗常数,下列说法正确的是( )
| A、78 g Na2O2与足量水反应中电子转移了0.2NA |
| B、1 mol甲基中含有7 NA 个电子 |
| C、62 g白磷中含P-P键为3 NA |
| D、1 mol氖气含有的原子数为2 NA |
下列方程式中,正确的是( )
| A、S2-水解反应:S2-+2H2O?H2S+2OH- |
| B、氯气与氯化亚铁溶液反应:Cl2+2Fe2+═2Fe3++2Cl- |
| C、H2CO3在水中电离:H2CO3?2H++CO32- |
| D、氢氧化钠溶液吸收过量的二氧化碳:2NaOH+CO2═Na2CO3+2H2O |
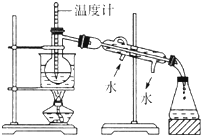 某化学课外小组以海带为原料制取少量碘水,现用CCl4 从碘水中萃取碘并用分液漏斗分离两种溶液.其实验可分解为如下各步:
某化学课外小组以海带为原料制取少量碘水,现用CCl4 从碘水中萃取碘并用分液漏斗分离两种溶液.其实验可分解为如下各步: