题目内容
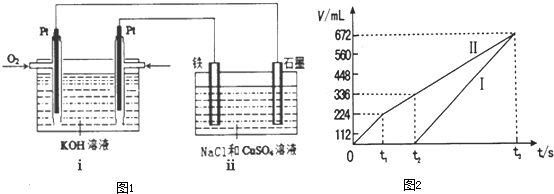
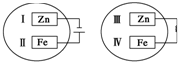 把锌片和铁片放在盛有稀食盐水和K3[Fe(CN)6]试液混合溶液的培养皿中(如图所示平面图),经过一段时间后,下列说法中正确的是( )
把锌片和铁片放在盛有稀食盐水和K3[Fe(CN)6]试液混合溶液的培养皿中(如图所示平面图),经过一段时间后,下列说法中正确的是( )| A、Ⅰ附近溶液pH降低 |
| B、Ⅱ附近很快出现蓝色沉淀 |
| C、Ⅲ附近产生黄绿色气体 |
| D、Ⅳ附近很快生成铁锈 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:第一个装置是电解池,铁为阳极,铁失电子生成亚铁离子,亚铁离子遇K3[Fe(CN)6]生成蓝色沉淀,溶液中的H+在Ⅰ处得电子,破坏了锌片附近水的电离平衡,使得OH-浓度增大,pH增大.第二个装置是原电池,Zn为负极,溶液中的氧气在Ⅳ处得电子生成OH-,发生了锌的吸氧腐蚀,据此解答.
解答:
解:A、Ⅰ附近溶液pH升高,故A错误;
B、第一个装置是电解池,铁为阳极,铁失电子生成亚铁离子,亚铁离子遇K3[Fe(CN)6]生成蓝色沉淀,故B正确;
C、第二个装置是原电池,Zn为负极,失电子生成锌离子,故C错误;
D、氧气在Ⅳ处得电子生成OH-,发生了锌的吸氧腐蚀,不会生成铁锈,故D错误;
故选B.
B、第一个装置是电解池,铁为阳极,铁失电子生成亚铁离子,亚铁离子遇K3[Fe(CN)6]生成蓝色沉淀,故B正确;
C、第二个装置是原电池,Zn为负极,失电子生成锌离子,故C错误;
D、氧气在Ⅳ处得电子生成OH-,发生了锌的吸氧腐蚀,不会生成铁锈,故D错误;
故选B.
点评:本题考查了原电池和电解池的工作原理的应用,主要是电解反应的离子变化,题目难度中等.

练习册系列答案
 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案
相关题目
有一瓶Na2CO3与NaHCO3固体混合物,要得到纯净的Na2CO3,可以采取的办法是( )
| A、过滤 | B、加热 | C、蒸馏 | D、溶解 |
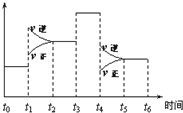 一密闭体系中发生反应:2SO2(g)+O2(g)?2SO3(g),如图表示该反应的速率(v)在某一时间(t)段内的变化.则下列时间段中,SO3的百分含量最高的是( )
一密闭体系中发生反应:2SO2(g)+O2(g)?2SO3(g),如图表示该反应的速率(v)在某一时间(t)段内的变化.则下列时间段中,SO3的百分含量最高的是( )| A、t0→t1 |
| B、t2→t3 |
| C、t3→t4 |
| D、t5→t6 |
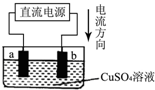 化学兴趣小组的同学用如图实验装置电解硫酸铜溶液,a、b为惰性电极.则下列说法错误的是( )
化学兴趣小组的同学用如图实验装置电解硫酸铜溶液,a、b为惰性电极.则下列说法错误的是( )| A、a是电解池的阴极、b是电解池的阳极 |
| B、b电极上的电极反应为:4OH--4e-=2H2O+O2↑ |
| C、通电一段时间后,溶液的PH减小 |
| D、通电一段时间后,欲使电解液恢复到起始状态,应向溶液中加入适量的CuSO4 |
室温下,有两种溶液:①0.01mol?L-1NH3?H2O溶液、②0.01mol?L-1NH4Cl溶液,下列操作可以使两种溶液中c(NH4+)都增大的是( )
| A、通入少量HCl气体 |
| B、加入少量NaOH固体 |
| C、加入少量H2O |
| D、适当升高温度 |
下列做法中用到物质氧化性的是( )
| A、铁红做红色颜料 |
| B、水玻璃做木材防火剂 |
| C、氧化铝做耐火材料 |
| D、氯气给自来水杀菌、消毒 |
已知aAn+、bB(n+1)+、cCn-、dD(n+1)-均具有相同的电子层结构,下列判断正确的是( )
| A、元素金属性:B>A;元素非金属性:D>C |
| B、原子半径:A>B>C>D |
| C、离子半径:D(n+1)->C n->B (n+1)+>A n+ |
| D、原子序数:b>a>c>d |
经测定甲醇和环己烷组成混合物中,氧的质量分数为8%,则此混合物中氢的质量分数为( )
| A、78% | B、28% |
| C、14% | D、13% |