题目内容
电解质不仅在工农业生产中占有重要地位,而且在各种生命活动中也起着重要作用,则下列有关电解质的叙述正确的是( )
| A、化合物都是电解质 |
| B、电解质一定是化合物 |
| C、SO3溶于水形成的溶液能导电,所以SO3是电解质 |
| D、NaCl固体不导电,所以NaCl不是电解质 |
考点:电解质与非电解质
专题:
分析:A、有些化合物不能电离出自由移动的离子,此种化合物属于非电解质,如蔗糖、酒精等;
B、电解质与非电解质一定是化合物,单质与混合物既不是电解质也不是非电解质;
C、非电解质:在熔融状态和水溶液中都不能导电的化合物,三氧化硫溶于水生成硫酸导电;
D、NaCl固体在水中或熔化状态下能导电.
B、电解质与非电解质一定是化合物,单质与混合物既不是电解质也不是非电解质;
C、非电解质:在熔融状态和水溶液中都不能导电的化合物,三氧化硫溶于水生成硫酸导电;
D、NaCl固体在水中或熔化状态下能导电.
解答:
解:A、有些化合物不能电离出自由移动的离子,此种化合物属于非电解质,如蔗糖、酒精等,故A错误;
B、电解质与非电解质一定是化合物,单质与混合物既不是电解质也不是非电解质,故B正确;
C、SO3 溶于水形成的硫酸溶液能导电,但三氧化硫自身不能电离,所以SO3 是非电解质,故C错误;
D、NaCl固体在水中或熔化状态下能导电,是电解质,故D错误;
故选B.
B、电解质与非电解质一定是化合物,单质与混合物既不是电解质也不是非电解质,故B正确;
C、SO3 溶于水形成的硫酸溶液能导电,但三氧化硫自身不能电离,所以SO3 是非电解质,故C错误;
D、NaCl固体在水中或熔化状态下能导电,是电解质,故D错误;
故选B.
点评:本题考查电解质、非电解质概念的辨析,强弱电解质溶液导电能力的关系,难度不大.解题时紧抓住电解质必须是化合物,以及导电是在水溶液或熔化状态下为条件.

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目
已知Ksp(PbCl2)=1.6×10-5,Ksp(PbI2)=7.1×10-9,Ksp(PbS)=8.0×10-28.若沉淀过程中依次看到白色PbCl2、黄色PbI2和黑色PbS三种沉淀,则往Pb2+溶液中滴加沉淀剂的顺序是( )
| A、Na2S、NaI、NaCl |
| B、NaCl、NaI、Na2S |
| C、NaCl、Na2S、NaI |
| D、NaI、NaCl、Na2S |
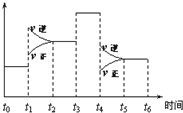 一密闭体系中发生反应:2SO2(g)+O2(g)?2SO3(g),如图表示该反应的速率(v)在某一时间(t)段内的变化.则下列时间段中,SO3的百分含量最高的是( )
一密闭体系中发生反应:2SO2(g)+O2(g)?2SO3(g),如图表示该反应的速率(v)在某一时间(t)段内的变化.则下列时间段中,SO3的百分含量最高的是( )| A、t0→t1 |
| B、t2→t3 |
| C、t3→t4 |
| D、t5→t6 |
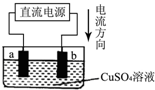 化学兴趣小组的同学用如图实验装置电解硫酸铜溶液,a、b为惰性电极.则下列说法错误的是( )
化学兴趣小组的同学用如图实验装置电解硫酸铜溶液,a、b为惰性电极.则下列说法错误的是( )| A、a是电解池的阴极、b是电解池的阳极 |
| B、b电极上的电极反应为:4OH--4e-=2H2O+O2↑ |
| C、通电一段时间后,溶液的PH减小 |
| D、通电一段时间后,欲使电解液恢复到起始状态,应向溶液中加入适量的CuSO4 |
下列做法中用到物质氧化性的是( )
| A、铁红做红色颜料 |
| B、水玻璃做木材防火剂 |
| C、氧化铝做耐火材料 |
| D、氯气给自来水杀菌、消毒 |
下列说法正确的是( )
| A、在化学反应中发生物质变化的同时,一定发生能量变化 |
| B、△H>0表示放热反应,△H<0表示吸热反应 |
| C、△H的大小与热化学方程式中化学计量数无关 |
| D、生成物释放的总能量大于反应物吸收的总能量时,△H>0 |