题目内容
10.在一定温度下,CO和CH4燃烧的热化学方程式分别为2CO(g)+O2(g)═2CO2(g)△H=-566kJ/mol
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890kJ/mol
2molCO和2mol CH4组成的混合气体,在相同条件下完全燃烧时,释放的热量为( )
| A. | 2022 kJ | B. | 2670 kJ | C. | 1698kJ | D. | 2346 kJ |
分析 热化学反应中,物质的量与反应中能量变化成正比,以此来解答.
解答 解:由2CO(g)+O2(g)═2CO2(g)△H=-566kJ/mol可知,2molCO完全燃烧放出热量为566kJ,
由CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890kJ/mol可知,1molCH4完全燃烧放出热量为890kJ,
2molCO和2mol CH4组成的混合气体,在相同条件下完全燃烧时,释放的热量为566kJ+2×890kJ=2346kJ,
故选D.
点评 本题考查反应热与焓变,为高频考点,把握物质的量与热量的关系为解答的关键,侧重分析与计算能力的考查,注意热化学方程式的应用,题目难度不大.

练习册系列答案
相关题目
20.氢气可通过下列反应制得:CO(g)+H2O(g)$\frac{\underline{\;催化剂\;}}{\;}$CO2(g)+H2(g)△H<0,为了提高氢气在平衡体系中所占的比例,可采取的措施是( )
| A. | 减小压强 | B. | 降低温度 | C. | 更换催化剂 | D. | 减小CO的浓度 |
1.某化学兴趣小组欲探究浓硫酸的性质,请帮助他们完成相关实验报告:
(1)浓硫酸与木炭粉在加热条件下的化学方程式为C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$2SO2↑+CO2↑+2H2O.
(2)已知KMnO4酸性溶液可以吸收SO2,试用图中各装置设计一个实验,验证上述反应所产生的各种产物.这些装置的连接顺序(按产物气流从左到右的方向)是(填装置的编号):④→②→①→③.
(3)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色.A瓶溶液的作用是:验证产物气流中是否有SO2,B瓶溶液的作用是将SO2全部氧化吸收,C瓶溶液的作用是确证产物中SO2已被B瓶溶液全部氧化.
(4)装置②中所加的固体药品是无水CuSO4(或变色硅胶),可确证的产物是:水蒸气.确定装置②在整套装置中位置的理由是由于产物气流通过①③时会带出水蒸气,所以②必须在①③之前.
(5)装置③中所盛溶液是澄清石灰水,可验证的产物是CO2 .
(1)浓硫酸与木炭粉在加热条件下的化学方程式为C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$2SO2↑+CO2↑+2H2O.
(2)已知KMnO4酸性溶液可以吸收SO2,试用图中各装置设计一个实验,验证上述反应所产生的各种产物.这些装置的连接顺序(按产物气流从左到右的方向)是(填装置的编号):④→②→①→③.
| 编号 | ① | ② | ③ | ④ |
| 装置 | 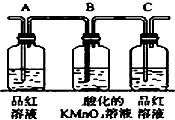 | 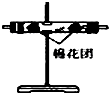 |  | 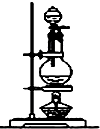 |
(4)装置②中所加的固体药品是无水CuSO4(或变色硅胶),可确证的产物是:水蒸气.确定装置②在整套装置中位置的理由是由于产物气流通过①③时会带出水蒸气,所以②必须在①③之前.
(5)装置③中所盛溶液是澄清石灰水,可验证的产物是CO2 .
18.25℃、101kPa时,使1.0g钠与足量的氯气反应,生成氯化钠晶体并放出17.87kJ的热量,则生成1mol NaCl的反应热是( )
| A. | -441 kJ/mol | B. | +441 kJ/mol | C. | -882 kJ/mol | D. | +882 kJ/mol |
5.肼(H2N-NH2)是一种高能燃料,有关化学反应的为N2H4(g)+O2═N2(g)+2H2O(g)△H=-576KJ/mol,已知断裂1mol化学键所需的能量(kJ):N≡N为942、O=O为500、N-N为154,H-O为463则断裂1molN-H键所需的能量(kJ)是( )
| A. | 391 | B. | 194 | C. | 516 | D. | 658 |
19.下列说法中有明显错误的是( )
| A. | 活化分子之间发生的碰撞一定为有效碰撞 | |
| B. | 升高温度,一般可使活化分子的百分数增大,因而反应速率增大 | |
| C. | 对有气体参加的化学反应增大压强体系体积减小,可使单位体积内活化分子数增加,因而反应速率增大 | |
| D. | 加入适宜的催化剂,可使活化分子的百分数大大增加,从而成千上万倍地增大化学反应的速率 |
20.如图装置中,若关闭活塞,则品红试液无变化,石蕊试液变红,澄清石灰水变浑浊;若打开活塞,则品红试液褪色,石蕊试液变红,澄清石灰水变浑浊.据此判断气体和广口瓶中盛放的物质是( )
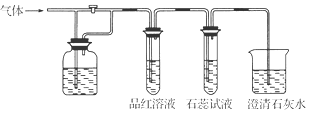

| A. | H2S和浓H2SO4 | B. | SO2和NaHCO3溶液 | C. | Cl2和NaHCO3溶液 | D. | Cl2和氯水 |