题目内容
18.25℃、101kPa时,使1.0g钠与足量的氯气反应,生成氯化钠晶体并放出17.87kJ的热量,则生成1mol NaCl的反应热是( )| A. | -441 kJ/mol | B. | +441 kJ/mol | C. | -882 kJ/mol | D. | +882 kJ/mol |
分析 1.0g钠与足量的氯气反应,生成氯化钠晶体并放出17.87kJ的热量,即$\frac{1}{23}$molNa与足量的氯气反应,生成氯化钠晶体并放出17.87kJ的热量,结合物质的量与能量变化成正比计算.
解答 解:1.0g钠与足量的氯气反应,生成氯化钠晶体并放出17.87kJ的热量,即$\frac{1}{23}$molNa与足量的氯气反应,生成氯化钠晶体并放出17.87kJ的热量,则生成1mol NaCl的放出热量是17.87kJ×23=411kJ,即生成1mol NaCl的反应热△H=-441 kJ/mol,
故选A.
点评 本题考查反应热与焓变,为高频考点,把握物质的量与能量变化的关系为解答的关键,侧重分析与计算能力的考查,注意热量与焓变的关系,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
13.已知乙醇在加热的条件下可与HBr反应得到溴乙烷(CH3CH2Br),二者某些物理性质如表所示:
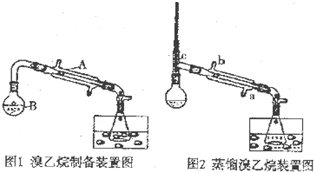
某研究性学习小组的同学将乙醇、80%的硫酸、NaBr固体按一定比例混合后(总体积约为140mL)置于图1的反应容器B中后进行加热(两个装置中的加热、固定装置及沸石均省略).
(1)①仪器A的名称是直形冷凝管
(2)两个水槽中的液体均是冰水,使用冰水的目的是降温,减少溴乙烷的挥发.
(3)HBr与乙醇反应生成目标产物的化学方程式HBr+CH3CH2OH$\stackrel{△}{→}$CH3CH2Br+H2O.
(4)图1中收集到的产品中含有一定量的杂质Br2,为除去该杂质,可先向混合液中加入适量的(从下面所给试剂中选取,填选项字母)b,然后再进行分液操作即可.
a.四氯化碳 b.碳酸钠溶液 c.无水CaCl2 d.浓硫酸
(5)经过(4)处理后的目标产物中还含有少量的水等杂质,可通过向产品中加入一定量的c(从上面的a--d中选取,填选项字母),充分作用后,过滤,将滤液使用图2中的装置进行提纯,冷却水应从a口(填a或b)进入.
(6)若试验中使用的无水乙醇的体积是46mL,蒸馏后得到纯溴乙烷的体积是50mL,则溴乙烷的产率为80%.
| 溶解性 | 沸点 | 密度(g/mL) | |
| 乙醇 | 与水互溶 | 78.5 | 0.8 |
| 溴乙烷 | 难溶于水 | 38.4 | 1.4 |

某研究性学习小组的同学将乙醇、80%的硫酸、NaBr固体按一定比例混合后(总体积约为140mL)置于图1的反应容器B中后进行加热(两个装置中的加热、固定装置及沸石均省略).
(1)①仪器A的名称是直形冷凝管
(2)两个水槽中的液体均是冰水,使用冰水的目的是降温,减少溴乙烷的挥发.
(3)HBr与乙醇反应生成目标产物的化学方程式HBr+CH3CH2OH$\stackrel{△}{→}$CH3CH2Br+H2O.
(4)图1中收集到的产品中含有一定量的杂质Br2,为除去该杂质,可先向混合液中加入适量的(从下面所给试剂中选取,填选项字母)b,然后再进行分液操作即可.
a.四氯化碳 b.碳酸钠溶液 c.无水CaCl2 d.浓硫酸
(5)经过(4)处理后的目标产物中还含有少量的水等杂质,可通过向产品中加入一定量的c(从上面的a--d中选取,填选项字母),充分作用后,过滤,将滤液使用图2中的装置进行提纯,冷却水应从a口(填a或b)进入.
(6)若试验中使用的无水乙醇的体积是46mL,蒸馏后得到纯溴乙烷的体积是50mL,则溴乙烷的产率为80%.
3.下列说法正确的是( )
| A. | 放热反应在常温下一定是很容易发生 | |
| B. | 需要加热才能发生的反应一定是吸热反应 | |
| C. | 由C(石墨)→C(金刚石)△H=+1.9 kJ•mol-1可知,金刚石比石墨稳定 | |
| D. | 等量的硫蒸气和硫固体分别完全燃烧,前者放出的热量多 |
10.在一定温度下,CO和CH4燃烧的热化学方程式分别为
2CO(g)+O2(g)═2CO2(g)△H=-566kJ/mol
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890kJ/mol
2molCO和2mol CH4组成的混合气体,在相同条件下完全燃烧时,释放的热量为( )
2CO(g)+O2(g)═2CO2(g)△H=-566kJ/mol
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890kJ/mol
2molCO和2mol CH4组成的混合气体,在相同条件下完全燃烧时,释放的热量为( )
| A. | 2022 kJ | B. | 2670 kJ | C. | 1698kJ | D. | 2346 kJ |
7.C60自被发现以来,已逐步应用到超导、材料等各个领域.下列有关说法正确的是( )

| A. | C60的摩尔质量是720 g•moL-1 | |
| B. | 1 mol C60完全燃烧生成22.4 L CO2 | |
| C. | C60属于有机化合物 | |
| D. | C60的结构与金刚石一样 |
 配制100mL 1.0mol?L-1的氯化钠溶液过程中,
配制100mL 1.0mol?L-1的氯化钠溶液过程中,