题目内容
2.请将下列反应的双线桥写出(1)8H++2NO3-+3Cu=Cu 2++2NO↑+4H2O
(2)KClO3+6HCl=KCl+3Cl2↑+3H2O.
分析 氧化还原反应中失电子的元素化合价升高,得电子的元素化合价降低,化合价降低数目=化合价升高数目=转移的电子数目,
(1)反应中铜元素0价变化为+2价,3mol铜反应失去电子为6mol,氮元素化合价+5价变化为+2价,2mol硝酸根离子失电子生成NO,得到6mol电子;
(2)反应中KClO3+6HCl=KCl+3Cl2↑+3H2O中,只有Cl元素化合价发生变化,Cl元素化合价分别由+5价、-1价变化为0价,当有3mol Cl2生成时,转移5mol电子,以此解答该题.
解答 解:(1)反应中铜元素0价变化为+2价,3mol铜反应失去电子为6mol,氮元素化合价+5价变化为+2价,2mol硝酸根离子失电子生成NO,得到6mol电子则电子转移的方向和数目为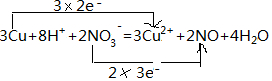 ,
,
答:反应的双线桥表示的氧化还原反应为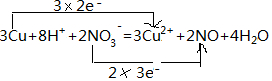 ;
;
(2)在KClO3+6HCl═KCl+3Cl2↑+3H2O反应中,氯酸钾中氯元素的化合价由+5价变为0价,所以氯酸钾是氧化剂,HCl中Cl元素化合价由-1价升高到0价,被氧化,既是氧化产物也是还原产物,得电子与失电子个数相等,比值为1:1,氧化产物和还原产物的质量之比是5:1,只有Cl元素化合价发生变化,当有3mol Cl2生成时,转移5mol电子,则电子转移的方向和数目为 ,
,
答:反应的双线桥表示的氧化还原反应为 .
.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化及发生的反应为解答的关键,侧重双线桥表示电子转移方向和数目的考查,注重基础知识的夯实,题目难度不大.

练习册系列答案
相关题目
12.已知N2(g)+3H2(g)$?_{催化剂}^{高温高压}$2NH3(g)△H=-92.22kJ•mol-1.下列对该反应的说法正确的是.
| A. | 可利用该反应进行人工固氮 | |
| B. | 将3mol N2(g)和3mol H2(g)混合,在高温、高压和催化条件下充分反应,放出热量92.22kJ | |
| C. | 因为反应需要加热,所以反应放出热量 | |
| D. | 其他条件相同时,采用更高效的正催化剂,既能提高反应速率,又能增大反应放热量 |
13.已知乙醇在加热的条件下可与HBr反应得到溴乙烷(CH3CH2Br),二者某些物理性质如表所示:
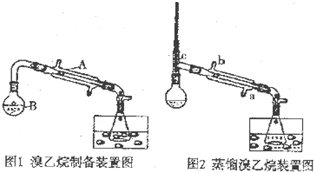
某研究性学习小组的同学将乙醇、80%的硫酸、NaBr固体按一定比例混合后(总体积约为140mL)置于图1的反应容器B中后进行加热(两个装置中的加热、固定装置及沸石均省略).
(1)①仪器A的名称是直形冷凝管
(2)两个水槽中的液体均是冰水,使用冰水的目的是降温,减少溴乙烷的挥发.
(3)HBr与乙醇反应生成目标产物的化学方程式HBr+CH3CH2OH$\stackrel{△}{→}$CH3CH2Br+H2O.
(4)图1中收集到的产品中含有一定量的杂质Br2,为除去该杂质,可先向混合液中加入适量的(从下面所给试剂中选取,填选项字母)b,然后再进行分液操作即可.
a.四氯化碳 b.碳酸钠溶液 c.无水CaCl2 d.浓硫酸
(5)经过(4)处理后的目标产物中还含有少量的水等杂质,可通过向产品中加入一定量的c(从上面的a--d中选取,填选项字母),充分作用后,过滤,将滤液使用图2中的装置进行提纯,冷却水应从a口(填a或b)进入.
(6)若试验中使用的无水乙醇的体积是46mL,蒸馏后得到纯溴乙烷的体积是50mL,则溴乙烷的产率为80%.
| 溶解性 | 沸点 | 密度(g/mL) | |
| 乙醇 | 与水互溶 | 78.5 | 0.8 |
| 溴乙烷 | 难溶于水 | 38.4 | 1.4 |

某研究性学习小组的同学将乙醇、80%的硫酸、NaBr固体按一定比例混合后(总体积约为140mL)置于图1的反应容器B中后进行加热(两个装置中的加热、固定装置及沸石均省略).
(1)①仪器A的名称是直形冷凝管
(2)两个水槽中的液体均是冰水,使用冰水的目的是降温,减少溴乙烷的挥发.
(3)HBr与乙醇反应生成目标产物的化学方程式HBr+CH3CH2OH$\stackrel{△}{→}$CH3CH2Br+H2O.
(4)图1中收集到的产品中含有一定量的杂质Br2,为除去该杂质,可先向混合液中加入适量的(从下面所给试剂中选取,填选项字母)b,然后再进行分液操作即可.
a.四氯化碳 b.碳酸钠溶液 c.无水CaCl2 d.浓硫酸
(5)经过(4)处理后的目标产物中还含有少量的水等杂质,可通过向产品中加入一定量的c(从上面的a--d中选取,填选项字母),充分作用后,过滤,将滤液使用图2中的装置进行提纯,冷却水应从a口(填a或b)进入.
(6)若试验中使用的无水乙醇的体积是46mL,蒸馏后得到纯溴乙烷的体积是50mL,则溴乙烷的产率为80%.
10.在一定温度下,CO和CH4燃烧的热化学方程式分别为
2CO(g)+O2(g)═2CO2(g)△H=-566kJ/mol
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890kJ/mol
2molCO和2mol CH4组成的混合气体,在相同条件下完全燃烧时,释放的热量为( )
2CO(g)+O2(g)═2CO2(g)△H=-566kJ/mol
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890kJ/mol
2molCO和2mol CH4组成的混合气体,在相同条件下完全燃烧时,释放的热量为( )
| A. | 2022 kJ | B. | 2670 kJ | C. | 1698kJ | D. | 2346 kJ |
7.C60自被发现以来,已逐步应用到超导、材料等各个领域.下列有关说法正确的是( )

| A. | C60的摩尔质量是720 g•moL-1 | |
| B. | 1 mol C60完全燃烧生成22.4 L CO2 | |
| C. | C60属于有机化合物 | |
| D. | C60的结构与金刚石一样 |
14.某碱性蓄电池在充电和放电时发生的反应为:Fe+NiO2+2H2O$?_{充电}^{放电}$ Fe(OH)2+Ni(OH)2,下列说法中正确的是( )
| A. | 充电时,阳极附近 pH 值减小 | |
| B. | 充电时,阴极反应是:Ni(OH)2-2e-+2OH-=NiO2+2H2O | |
| C. | 放电时,负极上发生反应的物质是Fe(OH)2 | |
| D. | 放电时,正极反应是:NiO2+2e-+2H+=Ni(OH)2 |
11.燃料电池是一种新型电池,它利用燃料在反应过程中把化学能直接转化为电能.氢氧燃料电池的基本反应如下:X极,$\frac{1}{2}$O2(g)+H2O(l)+2e-═2OH-;Y极,H2(g)+2OH--2e-═2H2O(l).下列判断中,正确的是( )
| A. | X是负极 | B. | Y是正极 | C. | Y极发生还原反应 | D. | Y极发生氧化反应 |
12.下列对实验过程的评价正确的是( )
| A. | 某固体中加入稀盐酸,产生了无色气体,证明该固体一定是CaCO3 | |
| B. | 某溶液中滴加BaCl2溶液,生成不溶于稀硝酸的白色沉淀,该溶液中一定含SO42- | |
| C. | 验证烧碱溶液中是否含有Cl-,先加稀盐酸除去OH-,再加硝酸银溶液,有白色沉淀出现,证明含Cl- | |
| D. | 某无色溶液滴入无色酚酞试液显红色,该溶液一定显碱性 |