题目内容
(1)化学反应中的少量,适量,足量,过量有什么区别?
(2)氯水分别与少量,适量,足量,过量的铁粉反应,最后的产物是什么?
(2)氯水分别与少量,适量,足量,过量的铁粉反应,最后的产物是什么?
考点:氯气的化学性质
专题:
分析:(1)少量:使自身全部发生反应,其它反应物可能刚好,可能过量.
适量:使自身和其它反应物刚好全部发生反应,在反应产物中无剩余.
足量:使其它反应物全部发生反应,自身可能刚好,可能过量.
过量:使另其它反应物全部发生反应,自身过量,在反应产物中存在.
(2)氯水分别与少量,适量,足量,过量的铁粉反应,最后的产物分别是氯化铁、氯化铁、氯化铁或氯化亚铁、氯化亚铁;
适量:使自身和其它反应物刚好全部发生反应,在反应产物中无剩余.
足量:使其它反应物全部发生反应,自身可能刚好,可能过量.
过量:使另其它反应物全部发生反应,自身过量,在反应产物中存在.
(2)氯水分别与少量,适量,足量,过量的铁粉反应,最后的产物分别是氯化铁、氯化铁、氯化铁或氯化亚铁、氯化亚铁;
解答:
解:(1)少量:指某一化学反应,其中某一反应物相对其它反应物物质的量少,不能使其它反应物完全反应掉,如Fe+CuSO4═Cu+FeSO4,1molFe相对于2molCuSO4少量,铁能完全反应,而硫酸铜过量;
适量:指某一化学反应,各反应物恰好完全反应,无反应物剩余,如Fe+CuSO4═Cu+FeSO4,1molFe和1molCuSO4恰好完全反应,无铁、硫酸铜剩余;
足量:指某一化学反应,其中某一反应物能使其它反应物全部反应掉,而自身刚好或过量,如Fe+CuSO4═Cu+FeSO4,1molFe相对于1molCuSO4,硫酸铜能完全反应,铁也无剩余,当1molFe和0.5molCuSO4,铁足量,且铁剩余;
过量:指某一化学反应,其中某一反应物使其它反应物全部发生反应,自身过量,在反应产物中存在,如Fe+CuSO4═Cu+FeSO4,1molFe和0.5molCuSO4,铁过量有剩余;
答:化学反应中的少量:指自身不足其它过量,适量:指两者恰好反应,足量:自身适量或过量,过量:自身过量;
(2)溶液中存在反应:Cl2+H2O?HCl+HClO,是可逆反应,存在电离:H2O?H++OH-,HClO?H++ClO-,
HCl=H++Cl-.所以溶液中存在的微粒有:分子:Cl2、HClO、H2O;离子:H+、Cl-、ClO-、OH-,
氯水与少量铁粉反应,Fe+2H+═H2↑+Fe2+,2Fe2++Cl2=2Fe3++2Cl-,最后的产物是氯化铁;
适量铁粉反应,Fe+2H+═H2↑+Fe2+,2Fe2++Cl2=2Fe3++2Cl-,最后的产物是氯化铁;
足量铁粉反应,Fe+2H+═H2↑+Fe2+,2Fe2++Cl2=2Fe3++2Cl-,或铁粉过量,发生Fe+2Fe3+=3Fe2+,
最后的产物是氯化铁或氯化亚铁;
过量的铁粉反应,Fe+2H+═H2↑+Fe2+,2Fe2++Cl2=2Fe3++2Cl-,Fe+2Fe3+=3Fe2+,最后的产物是氯化亚铁;
答:氯水分别与少量,适量,足量,过量的铁粉反应,最后的产物分别是氯化铁、氯化铁、氯化铁或氯化亚铁、氯化亚铁;
适量:指某一化学反应,各反应物恰好完全反应,无反应物剩余,如Fe+CuSO4═Cu+FeSO4,1molFe和1molCuSO4恰好完全反应,无铁、硫酸铜剩余;
足量:指某一化学反应,其中某一反应物能使其它反应物全部反应掉,而自身刚好或过量,如Fe+CuSO4═Cu+FeSO4,1molFe相对于1molCuSO4,硫酸铜能完全反应,铁也无剩余,当1molFe和0.5molCuSO4,铁足量,且铁剩余;
过量:指某一化学反应,其中某一反应物使其它反应物全部发生反应,自身过量,在反应产物中存在,如Fe+CuSO4═Cu+FeSO4,1molFe和0.5molCuSO4,铁过量有剩余;
答:化学反应中的少量:指自身不足其它过量,适量:指两者恰好反应,足量:自身适量或过量,过量:自身过量;
(2)溶液中存在反应:Cl2+H2O?HCl+HClO,是可逆反应,存在电离:H2O?H++OH-,HClO?H++ClO-,
HCl=H++Cl-.所以溶液中存在的微粒有:分子:Cl2、HClO、H2O;离子:H+、Cl-、ClO-、OH-,
氯水与少量铁粉反应,Fe+2H+═H2↑+Fe2+,2Fe2++Cl2=2Fe3++2Cl-,最后的产物是氯化铁;
适量铁粉反应,Fe+2H+═H2↑+Fe2+,2Fe2++Cl2=2Fe3++2Cl-,最后的产物是氯化铁;
足量铁粉反应,Fe+2H+═H2↑+Fe2+,2Fe2++Cl2=2Fe3++2Cl-,或铁粉过量,发生Fe+2Fe3+=3Fe2+,
最后的产物是氯化铁或氯化亚铁;
过量的铁粉反应,Fe+2H+═H2↑+Fe2+,2Fe2++Cl2=2Fe3++2Cl-,Fe+2Fe3+=3Fe2+,最后的产物是氯化亚铁;
答:氯水分别与少量,适量,足量,过量的铁粉反应,最后的产物分别是氯化铁、氯化铁、氯化铁或氯化亚铁、氯化亚铁;
点评:本题考查了化学基本概念以及氯水的性质,注意化学概念辨析时需抓住关键字词,注意氯水的化学性质,题目难度不大.

练习册系列答案
相关题目
下列反应的离子方程式正确的是( )
| A、石灰石溶于醋酸:CaCO3+2H+=Ca2++CO2↑+H2O |
| B、向NaAlO2溶液中通入少量的CO2:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3- |
| C、过量的二氧化碳与氢氧化钠反应:CO2+OH-=HCO3- |
| D、少量的氢氧化钠和碳酸氢钙反应:Ca2++2HCO3-+OH-=CaCO3↓+CO32-+2H2O |
下列过程中发生氧化还原反应的是( )
| A、用活性炭去除冰箱中的异味 |
| B、用热碱水清除炊具上残留的油污 |
| C、用浸泡过高锰酸钾溶液的硅藻土保存水果 |
| D、用含碱石灰的透气小袋与食品一起密封包装 |
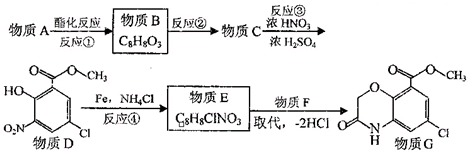
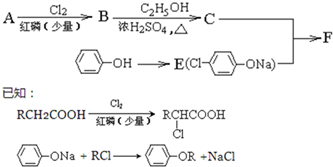
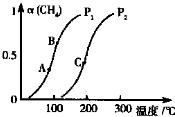 天然气在工农业生产中具有重要意义.
天然气在工农业生产中具有重要意义.
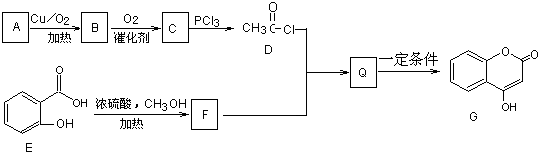
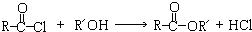
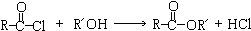 .
.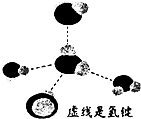 元素X、Y、Z、Q、W原子序数依次增大,其中X、Y、Z、Q为短周期元素.Z元素的焰色反应为黄色;X与Y形成的气体能使酚酞溶液变红,X与Q形成18电子的分子,
元素X、Y、Z、Q、W原子序数依次增大,其中X、Y、Z、Q为短周期元素.Z元素的焰色反应为黄色;X与Y形成的气体能使酚酞溶液变红,X与Q形成18电子的分子,