题目内容
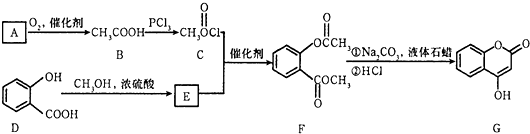
呋喃甲醇和呋喃甲酸是有机合成中的常用试剂,可用呋喃甲醛制备,其实验原理如图:

制备方法如下:
①在50mL烧杯中放置3.28mL(0.04mol)呋喃甲醛,并用冰水冷却;称取1.6gNaOH溶于少量水中,在搅拌下滴加氢氧化钠水溶液于呋喃甲醛中.
②在8~12℃下连续搅拌40min.
③向反应混合物加入适量水使其恰好完全溶解,甩乙醚萃取分液.
④乙醚萃取物用无水硫酸镁干燥后,先在水浴中蒸去乙醚,然后蒸馏,收集169~172℃馏分得1.4g产品.
⑤在乙醚提取后的水溶液中慢慢滴加浓盐酸到pH=3,搅拌,冷却,结晶,抽滤.
⑥产物用少量冷水洗涤,抽干后,收集粗产物.再提纯后得精产品1.5g.
(1)本实验中,氢氧化钠必须溶于少量的水,否则水量过大主要会影响 收率.
(2)本实验中要充分连续搅拌40min,其目的是 .
(3)萃取时,用到的主要硅酸盐质的仪器是 ,抽滤的优点是 .
(4)呋喃甲酸粗产品提纯的方法是 .
(5)本实验中呋喃甲酸的产率为 .

制备方法如下:
①在50mL烧杯中放置3.28mL(0.04mol)呋喃甲醛,并用冰水冷却;称取1.6gNaOH溶于少量水中,在搅拌下滴加氢氧化钠水溶液于呋喃甲醛中.
②在8~12℃下连续搅拌40min.
③向反应混合物加入适量水使其恰好完全溶解,甩乙醚萃取分液.
④乙醚萃取物用无水硫酸镁干燥后,先在水浴中蒸去乙醚,然后蒸馏,收集169~172℃馏分得1.4g产品.
⑤在乙醚提取后的水溶液中慢慢滴加浓盐酸到pH=3,搅拌,冷却,结晶,抽滤.
⑥产物用少量冷水洗涤,抽干后,收集粗产物.再提纯后得精产品1.5g.
(1)本实验中,氢氧化钠必须溶于少量的水,否则水量过大主要会影响
(2)本实验中要充分连续搅拌40min,其目的是
(3)萃取时,用到的主要硅酸盐质的仪器是
(4)呋喃甲酸粗产品提纯的方法是
(5)本实验中呋喃甲酸的产率为
考点:物质的分离、提纯的基本方法选择与应用,有机物的合成
专题:有机化合物的获得与应用
分析:(1)呋喃甲醇更易溶于有机溶剂,而呋喃甲酸易溶于水;
(2)反应在两相中进行的反应,长时间充分搅拌使其充分接触反应;
(3)萃取时,用到的主要硅酸盐质的仪器是分液漏斗;抽滤的优点是:过滤和洗涤速度加快,母液和晶体分离较完全,且产品易干燥;
(4)呋喃甲酸溶于水,其粗产品用重结晶方法进行提纯;
(5)根据化学方程式计算理论得到呋喃甲酸的物质的量,根据m=nM计算其质量,进而计算产率.
(2)反应在两相中进行的反应,长时间充分搅拌使其充分接触反应;
(3)萃取时,用到的主要硅酸盐质的仪器是分液漏斗;抽滤的优点是:过滤和洗涤速度加快,母液和晶体分离较完全,且产品易干燥;
(4)呋喃甲酸溶于水,其粗产品用重结晶方法进行提纯;
(5)根据化学方程式计算理论得到呋喃甲酸的物质的量,根据m=nM计算其质量,进而计算产率.
解答:
解:(1)呋喃甲醇更易溶于有机溶剂,而呋喃甲酸易溶于水,水量过大主要会影响呋喃甲酸的产率,故答案为:呋喃甲酸;
(2)由于反应在两相中进行的反应,长时间充分搅拌使其充分接触反应,保证反应完全,故答案为:在两相中进行的反应,长时间充分搅拌使其充分接触,保证反应完全;
(3)萃取时,用到的主要硅酸盐质的仪器是分液漏斗;抽滤的优点是:过滤和洗涤速度加快,母液和晶体分离较完全,且产品易干燥,故答案为:分液漏斗;过滤和洗涤速度加快,母液和晶体分离较完全,且产品易干燥;
(4)呋喃甲酸溶于水,其粗产品用重结晶方法进行提纯,故答案为:重结晶;
(5)由方程式可知,理论上应得到0.02mol呋喃甲酸,所以呋喃甲酸的产率为
×100%=67%,故答案为:67%.
(2)由于反应在两相中进行的反应,长时间充分搅拌使其充分接触反应,保证反应完全,故答案为:在两相中进行的反应,长时间充分搅拌使其充分接触,保证反应完全;
(3)萃取时,用到的主要硅酸盐质的仪器是分液漏斗;抽滤的优点是:过滤和洗涤速度加快,母液和晶体分离较完全,且产品易干燥,故答案为:分液漏斗;过滤和洗涤速度加快,母液和晶体分离较完全,且产品易干燥;
(4)呋喃甲酸溶于水,其粗产品用重结晶方法进行提纯,故答案为:重结晶;
(5)由方程式可知,理论上应得到0.02mol呋喃甲酸,所以呋喃甲酸的产率为
| 1.5g |
| 0.02mol×112g/mol |
点评:本题考查有机物的合成实验,是对学生综合能力的考查,需要学生具备扎实的基础,基本不属于中学内容,难度较大.

练习册系列答案
相关题目
下列与实验相关的叙述正确的是( )
| A、金属钠着火时,可用泡沫灭火器灭火 |
| B、蒸发结晶时应将溶液蒸干 |
| C、分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 |
| D、在氢氧化钠溶液中滴入氯化铁饱和溶液可以制得氢氧化铁胶体 |
有关下列溶液的叙述不正确的是( )
| A、C H3COOH与CH3COONa的混合溶液中:c(CH3COO-)+c(OH-)=c(Na+)+c(H+) |
| B、常温下,0.1mol.L-1CH3COONa溶液和0.1mol.L-1NaHCO3溶液,NaHCO3溶液的pH大 |
| C、0.1mol.L-1的(NH4)2SO4溶液中:c(SO42-)>c(NH4+)>c(H+)>c(OH-) |
| D、将l mol KC1、l mol KHS溶于水配成的混合溶液中:n(K+)=n(S2-)+n(HS-)+n(H2S) |
常温下,对于下列电解质溶液的说法正确的是( )
| A、pH=1的溶液中,Fe3+、I-、NO3-、K+可以大量共存 |
| B、用过量的NaOH溶液吸收SO2的离子方程式:SO2+OH-=HSO3- |
| C、在c(SO32-)=0.1 mol.L-1的溶液中,Na+、C1-、H+、Ca2+可以大量共存 |
| D、向澄清石灰水中通入氯气,反应的离子方程式:2OH-+Cl2=C1-+C1O-+H2O |
两名日本科学家与一名美国科学家利用钯作催化剂,将有机物进行“裁剪”、“缝合”,创造出具有特殊功能的新物质而获2010年诺贝尔化学奖.下列说法正确的是( )
| A、有机物中一定含有碳和氢两种元素 |
| B、一定条件下,催化剂能提高反应物的转化率 |
| C、将有机物进行“缝合”可以不遵循原子守恒定律 |
| D、将有机物进行“裁剪”需要破坏旧的化学键 |
下列离子方程式中,正确的是( )
| A、Na2O2与H2O反应:Na2O2+H2O=2Na++2OH-+O2↑ |
| B、AlCl3溶液中滴加过量的氨水:Al3++4 NH3?H2O=AlO2-+2H2O+4NH4+ |
| C、铜与稀硝酸反应:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O |
| D、向小苏打溶液中滴入醋酸:CO32-+2CH3COOH=CO2↑+H2O+2CH3COO- |
下列反应中,H2O2只表现氧化性的是( )
A、2H2O2
| ||||
| B、H2O2+2Fe3+═2Fe2++2H++O2↑ | ||||
| C、H2O2+SO2═H2SO4 | ||||
| D、H2O2+2Fe2++2H+═2Fe3++2H2O |