题目内容
17.恒容容器中,2SO2(g)+O2(g)?2SO3 (g)△H=-296.6kJ/mol,下列判断不正确的是( )| A. | 2体积SO2和足量O2反应,一定不能生成2体积SO3 | |
| B. | 其他条件不变,增大压强,正反应速率增大逆反应速率也增大 | |
| C. | 加入2molSO2和1molO2放出的热量是加入1molSO2和0.5molO2放出热量的2倍 | |
| D. | 平衡后再加入1molSO3,SO2的转化率增大 |
分析 A.为可逆反应,不能完全转化;
B.增大压强,正逆反应速率均增大;
C.物质的量越大,压强越大,平衡正向进行的趋势越大;
D.平衡后再加入1molSO3,压强增大.
解答 解:A.为可逆反应,不能完全转化,则2体积SO2和足量O2反应,一定不能生成2体积SO3,故A正确;
B.增大压强,正逆反应速率均增大,平衡正向移动,且正反应速率大于逆反应速率,故B正确;
C.物质的量越大,压强越大,平衡正向进行的趋势越大,则加入2molSO2和1molO2放出的热量大于加入1molSO2和0.5molO2放出热量的2倍,故C错误;
D.平衡后再加入1molSO3,压强增大,平衡正向移动,SO2的转化率增大,故D正确;
故选C.
点评 本题考查化学平衡的移动,为高频考点,把握压强对平衡移动的影响为解答的关键,侧重分析与应用能力的考查,注意可逆反应不能完全转化及选项C为解答的难点,题目难度不大.

练习册系列答案
相关题目
5.已知在25℃,101kPa下,1g C8H18(辛烷)燃烧生成二氧化碳和液态水时放出48.4kJ热量.表示上述反应的热化学方程式正确的是( )
| A. | C8H18(l)+$\frac{25}{2}$O2(g)═8CO2(g)+9H2O(g)△H=-48.4 kJ•mol-1 | |
| B. | C8H18(l)+$\frac{25}{2}$O2(g)═8CO2(g)+9H2O(l)△H=-5517.6 kJ•mol-1 | |
| C. | C8H18(l)+$\frac{25}{2}$O2(g)═8CO2(g)+9H2O(l)△H=+5517.6 kJ•mol-1 | |
| D. | C8H18(l)+$\frac{25}{2}$O2(g)═8CO2(g)+9H2O(l)△H=-48.4 kJ•mol-1 |
2.研究碳及其化合物的相互转化对能源的充分利用、低碳经济有着重要的作用.
(1)已知:①CH4(g)+H2O(g)?CO(g)+3H2(g)△H1=+206.1kJ•mol-1
②2H2(g)+CO(g)?CH3OH(l)△H2=-128.3kJ•mol-1
③2H2(g)+O2(g)?2H2O (g)△H3=-483.6kJ•mol-1
25℃时,在合适的催化剂作用下,采用甲烷和氧气一步合成液态甲醇的热化学方程式为CH4(g)+$\frac{1}{2}$O2(g)?CH3OH(l)△H1=-164.0kJ•mol-1.
(2)利用反应①来制备氢气,为了探究温度、压强对反应①速率、转化率的影响,某同学设计了以下三组对比实验(温度为400℃或500℃,压强为101kPa或404kPa).
①实验2和实验3相比,其平衡常数关系是K2>K3(填“>”、“<”或“=”).
②将等物质的量的CH4和水蒸气充入1L恒容密闭容器中,发生上述反应,在400℃下达到平衡,平衡常数K=27,此时容器中CO物质的量为0.10mol,则CH4的转化率为90.9%.
(3)科学家提出由CO2制 取 C的太阳能工艺如图1所示.
2“重整系统”发生的反应中n(FeO):n(CO2)=6:1,则Fe xOy的化学式为Fe3O4.
②“热分解系统”中每分解l mol Fe xOy,转移电子的物质的量为2mol.
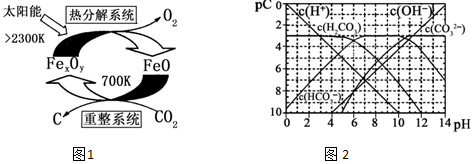
(4)pC类似pH,是指极稀溶液中的溶质浓度的常用负对数值.若某溶液中溶质的浓度为1×10-3mol•L-1,则该溶液中溶质的pC=-lg(1×10-3)=3.如图2为25℃时H2CO3溶液的pC-pH图.请回答下列问题 (若离子浓度小于10-5mol/L,可认为该离子不存在):
①在同一溶液中,H2CO3、HCO3-、CO32-不能(填“能”或“不能”)大量共存.
②求H2CO3一级电离平衡常数的数值Ka1=1×10-6.
③人体血液里主要通过碳酸氢盐缓冲体系$\frac{c({H}_{2}C{O}_{3})}{c(HC{O}_{3}^{-})}$可以抵消少量酸或碱,维持pH=7.4.当过量的酸进入血液中时,血液缓冲体系中的$\frac{c({H}^{+})}{c({H}_{2}C{O}_{3})}$最终将A.
A.变大B.变小C.基本不变D.无法判断.
(1)已知:①CH4(g)+H2O(g)?CO(g)+3H2(g)△H1=+206.1kJ•mol-1
②2H2(g)+CO(g)?CH3OH(l)△H2=-128.3kJ•mol-1
③2H2(g)+O2(g)?2H2O (g)△H3=-483.6kJ•mol-1
25℃时,在合适的催化剂作用下,采用甲烷和氧气一步合成液态甲醇的热化学方程式为CH4(g)+$\frac{1}{2}$O2(g)?CH3OH(l)△H1=-164.0kJ•mol-1.
(2)利用反应①来制备氢气,为了探究温度、压强对反应①速率、转化率的影响,某同学设计了以下三组对比实验(温度为400℃或500℃,压强为101kPa或404kPa).
| 实验序号 | 温度℃ | 压强/kPa | CH4初始浓度/mol•L-1 | H2O初始浓度/mol•L-1 |
| 1 | 400 | p | 3.0 | 7.0 |
| 2 | t | 101 | 3.0 | 7.0 |
| 3 | 400 | 101 | 3.0 | 7.0 |
②将等物质的量的CH4和水蒸气充入1L恒容密闭容器中,发生上述反应,在400℃下达到平衡,平衡常数K=27,此时容器中CO物质的量为0.10mol,则CH4的转化率为90.9%.
(3)科学家提出由CO2制 取 C的太阳能工艺如图1所示.
2“重整系统”发生的反应中n(FeO):n(CO2)=6:1,则Fe xOy的化学式为Fe3O4.
②“热分解系统”中每分解l mol Fe xOy,转移电子的物质的量为2mol.

(4)pC类似pH,是指极稀溶液中的溶质浓度的常用负对数值.若某溶液中溶质的浓度为1×10-3mol•L-1,则该溶液中溶质的pC=-lg(1×10-3)=3.如图2为25℃时H2CO3溶液的pC-pH图.请回答下列问题 (若离子浓度小于10-5mol/L,可认为该离子不存在):
①在同一溶液中,H2CO3、HCO3-、CO32-不能(填“能”或“不能”)大量共存.
②求H2CO3一级电离平衡常数的数值Ka1=1×10-6.
③人体血液里主要通过碳酸氢盐缓冲体系$\frac{c({H}_{2}C{O}_{3})}{c(HC{O}_{3}^{-})}$可以抵消少量酸或碱,维持pH=7.4.当过量的酸进入血液中时,血液缓冲体系中的$\frac{c({H}^{+})}{c({H}_{2}C{O}_{3})}$最终将A.
A.变大B.变小C.基本不变D.无法判断.
9.已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.在恒温条件下将一定量NO2和N2O4的混合气体通入一容积为2L的密闭容器中,反应物浓度随时间变化关系如图.下列说法不正确的是( )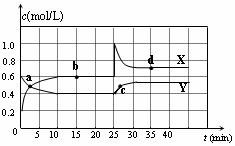

| A. | 图中的两条曲线,X表示NO2浓度随时间的变化曲线 | |
| B. | 前10 min内用v(N2O4)=0.02 mol/(L•min) | |
| C. | 25 min时,NO2转变为N2O4的反应速率增大,其原 因是将密闭容器的体积缩小为1L | |
| D. | 该温度下反应的平衡常数 K=1.11 L/mol |
6.学习化学过程中需要经常做实验,下列实验操作正确的是( )
| A. |  闻气味 | B. |  倾倒液体 | C. |  取粉末 | D. |  过滤 |
7.“84”消毒液和漂白粉都是氯气与碱反应在生活中的实际应用,下面说法错误的是( )
| A. | “84”消毒液有漂白和消毒作用 | |
| B. | 工业中将氯气通入石灰乳中制取漂白粉 | |
| C. | 漂白粉的有效成分是CaCl2和Ca(ClO)2 | |
| D. | 漂白粉在空气中久置失效 |
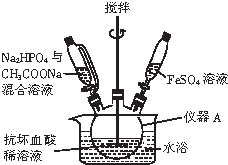 磷酸亚铁晶体[Fe3(PO4)2•8H2O]是蓝白色单斜晶体,溶于稀强酸,不溶于水、醋酸、醇,主要用于制作磷酸铁锉电池.实验室制备磷酸亚铁晶体的装置、反应原理和实验步骤如下:
磷酸亚铁晶体[Fe3(PO4)2•8H2O]是蓝白色单斜晶体,溶于稀强酸,不溶于水、醋酸、醇,主要用于制作磷酸铁锉电池.实验室制备磷酸亚铁晶体的装置、反应原理和实验步骤如下: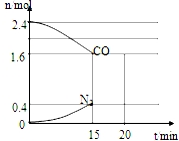 CO和NO是汽车尾气的主要污染物.消除汽车尾气的反应式之一为:2NO(g)+2CO(g)?N2(g)+2CO2(g).请回答下列问题:
CO和NO是汽车尾气的主要污染物.消除汽车尾气的反应式之一为:2NO(g)+2CO(g)?N2(g)+2CO2(g).请回答下列问题: