题目内容
8. CO和NO是汽车尾气的主要污染物.消除汽车尾气的反应式之一为:2NO(g)+2CO(g)?N2(g)+2CO2(g).请回答下列问题:
CO和NO是汽车尾气的主要污染物.消除汽车尾气的反应式之一为:2NO(g)+2CO(g)?N2(g)+2CO2(g).请回答下列问题:(1)一定温度下,在一体积为VL的密闭容器中充入一定量的NO和CO时,反应进行到t时刻时达到平衡状态,此时n(CO)=a mol、n(NO)=2a mol、n(N2)=b mol,且N2占平衡混合气体总价体积的$\frac{1}{4}$
①该反应的平衡常数K=$\frac{27V}{a}$(用只含a、V的式子表示)
②判断该反应达到平衡的标志是BD(填序号)
A.v(CO2)生成=v(CO)消耗
B.混合气体的平均相对分子质量不再改变
C.混合气体的密度不再改变
D.NO、CO、N2、CO2的物质的量浓度均不再变化
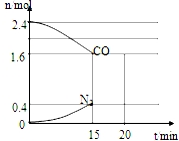
(2)在一定温度下,将2.0molNO、2.4molCO通入固定容积2L的密闭中,反应过程中部分物质的物质的量变化如图所示,则
①有害气体NO的转化率是40%,0~15min CO2的平均反应速率v(CO2)=0.027mol/(L.min)(保留小数点后三位).
②20min时,若改变反应条件,导致CO浓度减小,则改变的条件是CD(填序号)
A.增加CO2的量 B.加入催化剂 C.降低温度 D.扩大容积体积.
分析 (1)①平衡时n(CO)=amol、n(NO)=2amol、n(N2)=bmol,则根据方程式可知生成CO2是2bmol.又因为N2占平衡混合气体总体积的$\frac{1}{4}$,所以平衡时混合气体的总的物质的量是4b mol,则4bmol=bmol+2bmol+amol+2amol,解得b=3a,再由平衡常数表达式K=$\frac{c({N}_{2})×{c}^{2}(C{O}_{2})}{{c}^{2}(NO)×{c}^{2}(CO)}$计算;
②可逆反应到达平衡时,正逆反应速率相等,反应各组分的浓度、含量不变,由此衍生的其它物理量不变,判断平衡的物理量应随反应进行发生变化,该物理量由变化到不再变化,说明到达平衡;
(2)①发生反应:2NO+2CO=N2+2CO2,计算消耗CO物质的量,根据方程式计算消耗NO物质的量,进而计算NO转化率;根据v=$\frac{△c}{△t}$计算v(N2),再利用速率之比等于化学计量数之比计算v(CO2);
②20min时,若改变反应条件,导致CO浓度减小,可以使平衡向正反应方向移动,不能增大CO浓度、不能增大压强,否则到达平衡时CO浓度会增大,也可以扩大容器体积.
解答 解:(1)①平衡时n(CO)=amol、n(NO)=2amol、n(N2)=bmol,则根据方程式可知生成CO2是2bmol.又因为N2占平衡混合气体总体积的$\frac{1}{4}$,所以平衡时混合气体的总的物质的量是4b mol,则4bmol=bmol+2bmol+amol+2amol,解得b=3a,平衡常数K=$\frac{c({N}_{2})×{c}^{2}(C{O}_{2})}{{c}^{2}(NO)×{c}^{2}(CO)}$=$\frac{\frac{3a}{V}×(\frac{6a}{V})^{2}}{(\frac{2a}{V})^{2}×(\frac{a}{V})^{2}}$=$\frac{27V}{a}$,
故答案为:$\frac{27V}{a}$;
②A.v(CO2)生成=v(CO)消耗,均表示正反应速率,所以不能说明反应达到平衡状态,故A错误;
B.混合气体总质量不变,但物质的量是变化的,因此混合气体的平均相对分子质量不再改变可以说明反应达到平衡状态,故B正确;
C.在反应过程中气体总质量和容积始终是不变的,因此密度始终是不变的,则混合气体的密度不再改变不能说明反应达到平衡状态,故C错误;
D.NO、CO、N2、CO2的物质的量浓度均不再变化,说明正逆反应速率相等,反应达到平衡状态,故D正确,
故答案为:BD;
(2)①发生反应:2NO+2CO=N2+2CO2,平衡时CO是1.6mol,则消耗CO是2.4mol-1.6mol=0.8mol,根据方程式可知消耗NO是0.8mol,因此有害气体NO的转化率是$\frac{0.8mol}{2.0mol}$×100%=40%,
v(N2)=$\frac{\frac{0.4mol}{2L}}{15min}$=$\frac{1}{75}$mol/(L.min),速率之比等于化学计量数之比,v(CO2)=2v(N2)=2×$\frac{1}{75}$mol/(L.min)=0.027mol/(L.min),
故答案为:40%;0.027mol/(L.min);
②A.增加CO的量,CO浓度增大,故A错误;
B.加入催化剂平衡不移动,CO浓度不变,故B错误;
C.减小CO2的量,平衡向正反应方向进行,CO浓度减小,故C正确;
D.扩大容积体积,压强减小,平衡虽然向逆反应方向进行,但平衡常数不变,CO浓度仍然减小,故D正确,
故答案为:CD.
点评 本题考查化学平衡有关计算,为高频考点,侧重于学生的分析、计算能力的考查,题目涉及平衡状态判断、以及外界条件对平衡状态的影响等,是对学生综合能力的考查,难度中等.

 优百分课时互动系列答案
优百分课时互动系列答案 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案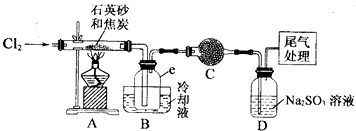
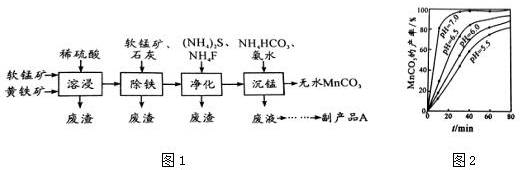
实验过程中;石英砂中的铁、铝等杂质也能转化为相应氯化物,SiCl4,A1C13,FeC13遇水均易水解,有关物质的物理常数见下表:
| 物质 | SiC14 | A1C13 | FeC13 |
| 沸点/℃ | 57.7 | - | 315 |
| 熔点/℃ | -70.0 | - | - |
| 升华温度/℃ | - | 180 | 300 |
(I)实验室制备氛气有以下五步操作,其正确操作顺序为④③⑤②①(填标号).
①向烧瓶中装入二氧化锰固体,向分液漏斗中加入浓盐酸
②检查装置的气密性
③把酒精灯放在铁架台上,根据酒精灯火焰确定铁圈高度,固定铁圈,放上石棉网
④在烧瓶上装好分液漏斗,安装好导气管
⑤将烧瓶固定在铁架台上
(2)装置A的硬质玻璃管中发生主要反应的化学方程式是2C+SiO2+2Cl2$\frac{\underline{\;高温\;}}{\;}$SiCl4+2CO↑;,置A.B间导管短且粗的原因是防止生成物中的AlCl3、FeCl3等杂质凝结成固体堵塞导管,实验中尾气处理的方法是连接一个加热的装有CuO粉末的反应管.
(3)装置B中e瓶收集到的粗产物可通过精馏(类似多次蒸馏)得到高纯度四氛化硅.在精馏过程中,不可能用到的仪器有CD(填正确答案标号).
A.圆底烧瓶 B.温度计 C.吸滤瓶 D球形冷凝管 E.接收器
(4)装置D中的Na2SO3的作用主要是吸收未反应完的Cl2请设计一个实验,证明装置D中的Na2SO3已被氧化(简述实验步骤):取少量溶液置于洁净的试管中,向其中滴加稀盐酸至不再产生气体;再向其中滴入氯化钡溶液,若产生白色沉淀,证明亚硫酸钠被氧化.
(5)SiCl4极易水解,其完全水解的产物为H4SiO4(或H2SiO3)和HCl;H2还原SiCl4制得高纯硅的过程中若混入O2,可能引起的后果是可能引起爆炸、硅被氧化得不到高纯硅.
| A. | 降低温度 | B. | 增大N的浓度 | C. | 减小X的浓度 | D. | 增大压强 |
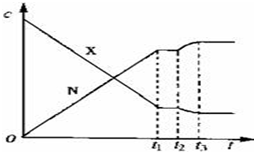
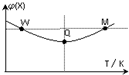 在2L恒容密闭容器中充入2mol X和1mol Y发生反应:2X(g)+Y(g)?3Z(g)△H<0,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示.下列推断正确的是( )
在2L恒容密闭容器中充入2mol X和1mol Y发生反应:2X(g)+Y(g)?3Z(g)△H<0,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示.下列推断正确的是( )| A. | 升高温度,平衡常数增大 | |
| B. | W点X的正反应速率小于M点X的正反应速率 | |
| C. | Q点时,Y的转化率最小 | |
| D. | 平衡时充入Z,达到新平衡时Z的体积分数比原平衡时大 |
| A. | 2体积SO2和足量O2反应,一定不能生成2体积SO3 | |
| B. | 其他条件不变,增大压强,正反应速率增大逆反应速率也增大 | |
| C. | 加入2molSO2和1molO2放出的热量是加入1molSO2和0.5molO2放出热量的2倍 | |
| D. | 平衡后再加入1molSO3,SO2的转化率增大 |
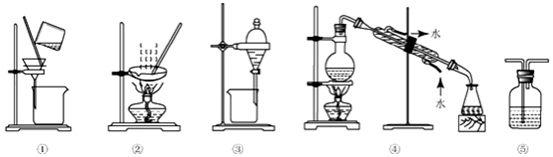
| A. | 粗盐提纯,选①和② | B. | 用CC14提取碘水中的碘,选③ | ||
| C. | 分离Na2CO3溶液和CCl4,选④ | D. | 用FeC12溶液吸收C12,选⑤ |