题目内容
足量的Fe与1mol Cl2反应,转移 mol电子.
考点:化学方程式的有关计算
专题:计算题
分析:计算时根据量少的物质进行计算,Fe是足量的,反应中Cl2生成FeCl3,Cl的化合价由0价变为-1价,1mol Cl2转移2mol电子.
解答:
解:Fe是足量的,反应中Cl2生成FeCl3,Cl的化合价由0价变为-1价,1mol Cl2转移2mol电子,故答案为:2.
点评:本题考查氧化还原反应计算,明确元素化合价变化是解本题关键,根据氧化剂或还原剂与转移电子之间的关系式计算即可,题目难度不大.

练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
同温同压下两个容积相等的贮气瓶,一个装有NO气体,另一个装有O2和N2的混合气体,则两瓶内的气体不一定相同的是( )
| A、气体质量 | B、气体的物质的量 |
| C、分子总数 | D、原子数 |
火星表面还有火星表面还有黄钾铁矾,其组成的化学式为KFe3(SO4)2(OH)6,易溶于稀硫酸,下列说法不正确的是( )
| A、黄钾铁矾中铁元素显+3价 |
| B、黄钾铁矾属于碱 |
| C、黄钾铁矾溶于硫酸后,滴加KSCN溶液,溶液变红 |
| D、黄钾铁矾晶体在酒精灯火焰上灼烧,透过蓝色的钴玻璃可观察到紫色火焰 |
0.1mol/L氨水中,溶液中随着水量的增加而减少的是( )
A、
| ||
B、
| ||
| C、C(H+)和C(OH-)的乘积 | ||
| D、OH-的物质的量 |
下列能达到实验目的是( )
A、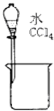 分离水和CCl4 |
B、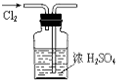 干燥Cl2 |
C、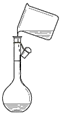 转移溶液 |
D、 蒸发食盐水 |
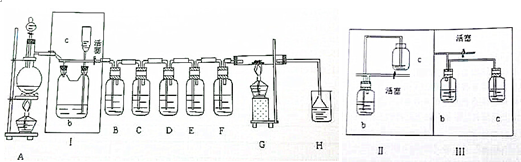
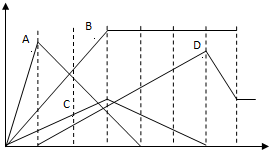 如图中,纵坐标为沉淀物的物质的量,横坐标为某溶液中加入反应物的物质的量,试按题意将相应图示的字母填入下表.
如图中,纵坐标为沉淀物的物质的量,横坐标为某溶液中加入反应物的物质的量,试按题意将相应图示的字母填入下表. 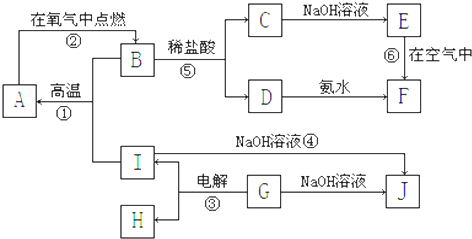
 现用物质的量浓度为a mol/L的标准盐酸去测定VmL NaOH溶液的物质的量浓度,请填写下列空白:
现用物质的量浓度为a mol/L的标准盐酸去测定VmL NaOH溶液的物质的量浓度,请填写下列空白: