题目内容
15.以NA代表阿伏加德罗常数,下列说法正确的是( )| A. | 常温常压下,32gO2含2NA个原子 | |
| B. | 标准状况下,11.2LH2O含有的原子数目为1.5NA | |
| C. | 1mol的Cl-含有NA个电子 | |
| D. | 0.5mol/L的NaCl溶液中Cl-的个数为0.5 NA |
分析 A.根据n=$\frac{m}{M}$计算出氧气的物质的量,再计算出含有氧原子的物质的量及数目;
B.标准状况下,水的状态不是气态;
C.氯离子中含有18个电子,1mol氯离子含有18mol电子;
D.缺少溶液体积,无法计算氯离子的物质的量.
解答 解:A.32g氧气的物质的量为$\frac{32g}{32g/mol}$=1mol,1mol氧气分子中含有2molO原子,含2NA个原子,故A正确;
B.标准状况下水不是气体,不能使用标准状况下的气体摩尔体积计算,故B错误;
C.1mol的Cl-含有18mol电子,含有18NA个电子,故C错误;
D.没有告诉0.5mol/L的NaCl溶液的体积,无法计算溶液中含有氯离子的物质的量,故D错误;
故选A.
点评 本题考查了阿伏伽德罗常数的判断,题目难度不大,明确气体摩尔体积的使用条件为解答关键,注意掌握物质的量与其它物理量之间的转化关系,试题培养了学生的化学计算能力.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
5.下列溶液中,Cl-的物质的量浓度与50mL 1mol•L-1AlCl3溶液中Cl-的物质的量浓度相等的是( )
| A. | 75mL 2mol•L-1FeCl3溶液 | B. | 25mL 2mol•L-1KCl溶液 | ||
| C. | 150mL 1mol•L-1NaCl溶液 | D. | 20mL 1.5mol•L-1 MgCl2溶液 |
6.实验室里需480mL1.0mol/LNaOH溶液,若用固体NaOH配制,则应选择的容量瓶规格为( )
| A. | 480mL | B. | 1000mL | C. | 100mL | D. | 500mL |
3.化学反应Fe2O3+2Al $\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3的反应类型是( )
| A. | 分解反应 | B. | 置换反应 | C. | 复分解反应 | D. | 化合反应 |
20.油脂在人体内完全水解的产物是高级脂肪酸和( )
| A. | 葡萄糖 | B. | 甘油 | C. | 多酞 | D. | 氨基酸 |
4.下列物质的电离方程式正确的是( )
| A. | H2CO3?2H++CO32- | B. | Ba(OH)2?Ba2++2OH- | ||
| C. | NaHCO3?Na++HCO3- | D. | HClO?H++ClO- |
10.下列说法正确的是( )
| A. | 高锰酸钾充分加热后的剩余固体、碘酒、空气都是混合物 | |
| B. | Na2O和NH3的水溶液均能导电,故均为电解质 | |
| C. | 氧化还原反应中非金属单质只作氧化剂 | |
| D. | 酸碱中和反应的实质是H+与OH-结合生成水,故酸碱中和反应都可用H++OH-═H2O表示 |
 用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: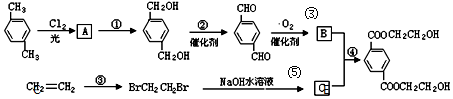
 、B、
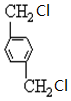
、B、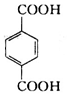 、C.HOCH2CH2OH、
、C.HOCH2CH2OH、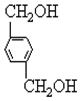 +2NaCl;
+2NaCl; ,反应的化学方程式是
,反应的化学方程式是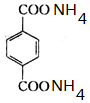 +2H2O.
+2H2O.