题目内容
12.六种短周期元素A、B、C、D、E、F的原子序数依次增大,其中A与E同主族,B与F同主族,E与F同周期.已知常温下单质A与E的状态不同,D的核电荷数是B的最外层电子数的2倍,单质F是一种重要的半导体材料.则下列推断中正确的是( )| A. | D、E两种元素仅可组成化学式为E2D的化合物 | |
| B. | 原子半径:E>F>C>D | |
| C. | F与D形成的化合物性质很不活泼,不与任何酸反应 | |
| D. | 元素的非金属性:D>C>F>B |
分析 六种短周期元素A、B、C、D、E、F的原子序数依次增大,单质F是一种重要的半导体材料,则F是Si元素,B与F同主族,则B是C元素;
E与F同周期,A与E同主族,常温下单质A与E的状态不同,则A是H元素、E是Na元素,
D的核电荷数是B的最外层电子数的2倍,则D是O元素,C元素原子序数大于B而小于D,则C是N元素;
A.D、E是O、Na元素,二者形成的化合物有两种;
B.原子电子层数越多,其原子半径越大,同一周期元素,原子半径随着原子序数增大而减小;
C.F是Si元素、D是O元素,二者形成的化合物是SiO2,二氧化硅能和HF反应;
D.同一周期元素,元素非金属性随着原子序数增大而增强,同一主族元素,元素非金属性随着原子序数增大而减弱.
解答 解:六种短周期元素A、B、C、D、E、F的原子序数依次增大,单质F是一种重要的半导体材料,则F是Si元素,B与F同主族,则B是C元素;
E与F同周期,A与E同主族,常温下单质A与E的状态不同,则A是H元素、E是Na元素,
D的核电荷数是B的最外层电子数的2倍,则D是O元素,C元素原子序数大于B而小于D,则C是N元素;
A.D、E是O、Na元素,二者形成的化合物有Na2O、Na2O2,故A错误;
B.原子电子层数越多,其原子半径越大,同一周期元素,原子半径随着原子序数增大而减小,所以原子半径E>F>C>D,故B正确;
C.F是Si元素、D是O元素,二者形成的化合物是SiO2,二氧化硅能和HF反应生成四氟化硅和水,故C错误;
D.同一周期元素,元素非金属性随着原子序数增大而增强,同一主族元素,元素非金属性随着原子序数增大而减弱,则非金属性D>C>B>F,故D错误;
故选B.
点评 本题考查原子结构和元素周期律,为高频考点,侧重考查学生分析判断及知识综合运用能力,涉及元素化合物性质、元素周期律等知识点,明确原子结构和元素周期律、元素化合物性质是解本题关键,易错选项是C,注意二氧化硅性质的特殊性.

| A. | “地沟油”是指从泔水中提取的油脂,它也是一种资源,但不能食用,可用于生产燃料油或用于制肥皂 | |
| B. | 媒体曝光的制造问题胶囊的工业明胶的主要成分是蛋白质 | |
| C. | 塑化剂DEHP是邻苯二甲酸(2─乙基己基)二酯,对人体无害可用作食品添加剂 | |
| D. | PM2.5是指大气中直径≤2.5×10-6m的颗粒物(气溶胶),可通过加水吸收后再用半透膜渗析的方法分离PM2.5微粒与可溶性吸附物 |
Ⅰ.世界最早工业生产碳酸钠的方法是路布兰(N.Leblanc)法.其流程如下:
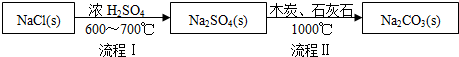
(1)流程I的另一产物是HCl,流程Ⅱ的反应分步进行:a.Na2SO4+4C $\frac{\underline{\;1000℃\;}}{\;}$ Na2S+4CO↑;
b.Na2S与石灰石发生复分解反应,总反应方程式可表示为Na2SO4+4C+CaCO3$\frac{\underline{\;1000℃\;}}{\;}$Na2CO3+CaS+4CO↑.
Ⅱ.1862年,比利时人索尔维(Ernest Solvay)用氨碱法生产碳酸钠.反应原理如下:
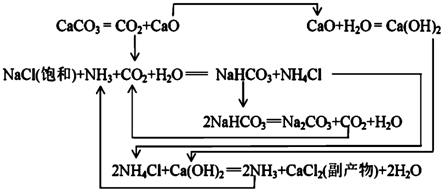
20℃时一些物质在水中的溶解度/g•(100gH2O)-1
| NaCl | NH4Cl | NaHCO3 | NH4HCO3 | Na2CO3 |
| 35.9 | 37.2 | 9.6 | 21.7 | 21.5 |
(3)饱和NaCl溶液通NH3和CO2能生成NaHCO3的原因有:反应体系中NaHCO3溶解度最小,反应消耗水,NaHCO3相对分子质量最大.
Ⅲ.我国化工专家侯德榜研究出联合制碱法,其反应原理和氨碱法类似,但将制氨和制碱联合,提高了原料利用率.
(4)生产中需向分离出NaHCO3后所得的溶液中加入NaCl固体并通入NH3,在0~10℃(填温度范围)下析出NH4Cl.(填化学式)

| A. | CH4,H2O2,NH3 | B. | H2O,CO2,Na2O2 | C. | Na2O,NaCl,MgCl2 | D. | NaOH,NaClO,Na2O |
| A. | Na2O2是碱性氧化物,具有强氧化性可用于杀菌消毒 | |
| B. | 乙烯能使溴水和酸性高锰酸钾溶液褪色,且褪色原理相同 | |
| C. | Mg(OH)2难溶于水,但可缓慢溶于浓的NH4Cl溶液 | |
| D. | 油脂在酸性条件下可以水解,可用此反应可以制作肥皂 |
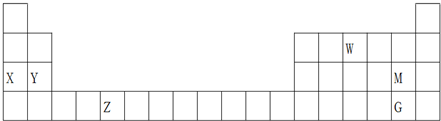
| A. | 最高价氧化物的水化物的碱性:X<Y | |
| B. | W的氢化物的球棍模型为: | |
| C. | 酸性:HMO4<HGO4 | |
| D. | Z的某些化合物可以用作反应的催化剂 |
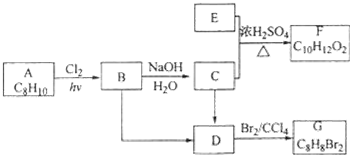
 .
. .
. (填结构简式)
(填结构简式)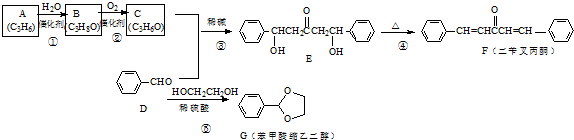
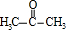 ;A加聚产物的结构简式是
;A加聚产物的结构简式是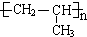 .
.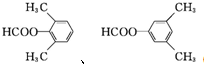 .
.