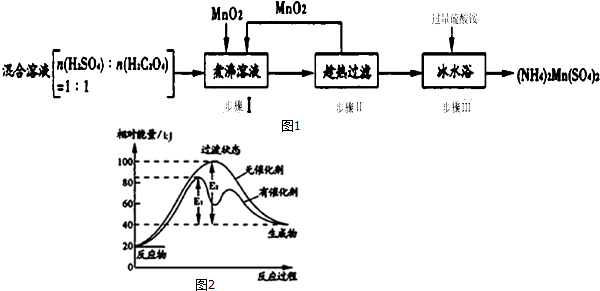
��Ŀ����
17��̼���Ƶ���;�ܹ㣬������ұ�𡢷�֯��ƯȾ�ȹ�ҵ�Ļ���ԭ�ϣ����������ش��������⣺���������繤ҵ����̼���Ƶķ�����·������N��Leblanc���������������£�
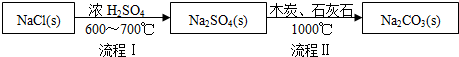
��1������I����һ������HCl�����̢�ķ�Ӧ�ֲ����У�a��Na2SO4+4C $\frac{\underline{\;1000��\;}}{\;}$ Na2S+4CO����
b��Na2S��ʯ��ʯ�������ֽⷴӦ���ܷ�Ӧ����ʽ�ɱ�ʾΪNa2SO4+4C+CaCO3$\frac{\underline{\;1000��\;}}{\;}$Na2CO3+CaS+4CO����
��1862�꣬����ʱ������ά��Ernest Solvay���ð������̼���ƣ���Ӧԭ�����£�
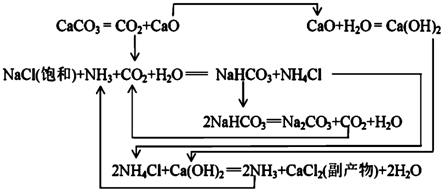
20��ʱһЩ������ˮ�е��ܽ��/g•��100gH2O��-1
| NaCl | NH4Cl | NaHCO3 | NH4HCO3 | Na2CO3 |
| 35.9 | 37.2 | 9.6 | 21.7 | 21.5 |
��3������NaCl��ҺͨNH3��CO2������NaHCO3��ԭ���У���Ӧ��ϵ��NaHCO3�ܽ����С����Ӧ����ˮ��NaHCO3��Է����������
���ҹ�����ר�Һ�°��о��������Ƽ���䷴Ӧԭ���Ͱ�����ƣ������ư����Ƽ����ϣ������ԭ�������ʣ�
��4����������������NaHCO3�����õ���Һ�м���NaCl���岢ͨ��NH3����0��10�棨���¶ȷ�Χ��������NH4Cl�����ѧʽ��

���� ��·������������ʳ�ξ����Ũ�����ڸ����·�Ӧ���������ƺ��Ȼ��⣬������C��ʯ��ʯ�������Ƹ��¼�������̼���ƣ�
��1�����̢����������ƣ���һ�ֲ�������������غ��ԭ���غ��жϣ�������ʯ��ʯ�������ֽⷴӦ�Ļ�ѧ����ʽΪNa2S+CaCO3$\frac{\underline{\;����\;}}{\;}$Na2CO3+CaS����������ʽ��Ӽ��ɵõ��ܷ�Ӧʽ��
������ά�ð������̼���ƣ���Ӧԭ��Ϊ���ð������͵�NaCl��CO2��Ӧ�õ�NaHCO3����̼�����Ʒֽ⼴�ɵõ�����̼���ƣ�
��2������ά�ð������̼���ƣ�ԭ��CO2��Դ��ʯ��ʯ��CaCO3���ķֽ⣬����ʳ�Ρ�������ˮ����̼�����Ʒֽ�����CO2�ʹ���Ȼ�茶���ֽ����ɰ�����
��3����ͬ�¶��£�̼�����Ƶ��ܽ������С��̼���ƣ�
��°��о��������ƼΪ�ڱ��͵��Ȼ�����Һ��ֱ��ͨ�백����CO2���õ��Ȼ�狀�̼�����ƾ��壬������̼�����Ƶķֽ��Ƶô��
��4�������Ƽ�ᾧ��̼̼�����ƺ����Һ����Ҫ�����Ȼ�泥������Ȼ��Ʋ�ͨNH3���ɴٽ�NH4Cl��s��?NH4+��aq��+Cl-��aq���ܽ�ƽ�������ƶ������������Ȼ�泥���ѡ���ڵ����½��У��Է�ֹ�����������壮
��� �⣺��·������������ʳ�ξ����Ũ�����ڸ����·�Ӧ���������ƺ��Ȼ��⣬������C��ʯ��ʯ�������Ƹ��¼�������̼���ƣ�
��1�����̢����ø߷е����ƻӷ�����ԭ�����Ȼ�����Ũ�����ϼ��ȣ����������ƺ��Ȼ��⣻a��Na2SO4+4C$\frac{\underline{\;1000��\;}}{\;}$Na2S+4CO����b��Na2S��ʯ��ʯ�������ֽⷴӦ�Ļ�ѧ����ʽΪNa2S+CaCO3$\frac{\underline{\;1000��\;}}{\;}$Na2CO3+CaS����������ʽ��Ӽ��ɵõ��ܷ�Ӧʽ Na2SO4+4C+CaCO3 $\frac{\underline{\;1000��\;}}{\;}$Na2CO3+CaS+4CO����
�ʴ�Ϊ��HCl�� Na2SO4+4C+CaCO3 $\frac{\underline{\;1000��\;}}{\;}$Na2CO3+CaS+4CO����
������ά�ð������̼���ƣ���Ӧԭ��Ϊ���ð������͵�NaCl��CO2��Ӧ�õ�NaHCO3����̼�����Ʒֽ⼴�ɵõ�����̼���ƣ�
��2������ά��ʳ�Ρ�ˮ��������CO2��Ӧ�Ʊ�̼�����ƣ����п�����ʯ��ʯ��CaCO3���ֽ�õ�CO2��̼�����Ʒֽⴿ�ͬʱ�õ�CO2�����⸱��Ʒ�Ȼ�茶���ֽ������ɰ����������������ѭ�����ã�����ת����·ʯ��ʯ��CaCO3���ֽ�õ������ƺ�CO2�����ɵ��Ȼ�刺������������Ʒ�Ӧ��CaO��NH4ClҲ��ѭ��ʹ�ã�
�ʴ�Ϊ��ʳ�Ρ�ʯ��ʯ��CaO��CO2��NH4Cl��NH3��
��3������ͬ�¶��£�̼�����Ƶ��ܽ������С��̼���ƣ���NaCl��ҺͨNH3��CO2ֻ������NaHCO3��ͬʱ��Ӧ����ˮ��������������̼�����ƣ�
�ʴ�Ϊ����Ӧ��ϵ��NaHCO3�ܽ����С����Ӧ����ˮ��NaHCO3��Է����������
��°��о��������ƼΪ�ڱ��͵��Ȼ�����Һ��ֱ��ͨ�백����CO2���õ��Ȼ�狀�̼�����ƾ��壬������̼�����Ƶķֽ��Ƶô��
��4���ں����Ȼ�淋���Һ�У������Ȼ��Ʋ�ͨNH3���������Һ��Cl-��NH4+��Ũ�ȣ��ٽ�NH4Cl��s��?NH4+��aq��+Cl-��aq���ܽ�ƽ�������ƶ������������Ȼ�泥���NH4Cl�������ܽ�ȱȽ�С�����¸���NH4Cl�������������Է�ֹ�����������壬
�ʴ�Ϊ��0��10�棻NH4Cl��
���� ����̽�����ֲ�ͬ����Ʊ�����̼���Ƶ�ʵ��ԭ�����漰��Ӧԭ�����ܽ�ȼ������ķ���������������Կ��飬�Ѷ����У��ѵ�Ϊ��Ӧԭ���ķ�����

 �����������Ů��ͯ������ϵ�д�
�����������Ů��ͯ������ϵ�д�| A�� | c��F-����c��OH-����c��HCN����c��HF�� | B�� | c��F-��+c��HF����c��CN-��+c��HCN�� | ||
| C�� | c��OH-����c��F-����c��CN-����c��H+�� | D�� | c��OH-����c��HF����c��HCN����c��H+�� |
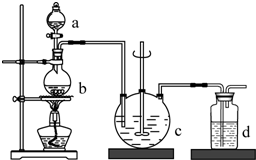 ��������ƣ�Na2S2O3�����������������մ�ͨ��Ϊ��ɫ���壬������ˮ�������ھƾ������ȡ������ֽ⣮ҽѧ�����������軯���ж��������ڵ⻯���IJ�������ҵ�Ʊ��ķ�Ӧԭ��Ϊ��2Na2S+Na2CO3+4SO2�T3Na2S2O3+CO2��ʵ����ģ��ù�ҵ���̵�װ����ͼ��ʾ���ش��������⣺
��������ƣ�Na2S2O3�����������������մ�ͨ��Ϊ��ɫ���壬������ˮ�������ھƾ������ȡ������ֽ⣮ҽѧ�����������軯���ж��������ڵ⻯���IJ�������ҵ�Ʊ��ķ�Ӧԭ��Ϊ��2Na2S+Na2CO3+4SO2�T3Na2S2O3+CO2��ʵ����ģ��ù�ҵ���̵�װ����ͼ��ʾ���ش��������⣺��1��c���Լ�Ϊ������Һ��̼������Һ��
��2����Ӧ��ʼ��c�����е���ɫ���Dz��������ֱ�Ϊ���壬�˻����������S��
��3��ʵ����Ҫ����SO2�������ʣ��ɲ�ȡ�Ĵ�ʩ�п��Ʒ�Ӧ�¶ȡ�������ĵμ��ٶȻ�������Ũ�ȵȣ�д��һ������
��4������c�е���Һ��pH�ӽ�7��ֹͣͨ��SO2����δ���ƺã�������ҺpH��7����Ӱ����ʣ�ԭ���ǣ������ӷ���ʽ��ʾ��S2O32-+2H+=S��+H2O+SO2����
��5��dװ��ʢ�ŵ�����������Һ������������SO2��β������ֹ��Ⱦ������
��6��ֹͣͨ��SO2����c�м�������������������Һ������Һת�Ƶ��������У�ˮԡ����Ũ������ȴ�ᾧ�����ˡ�ϴ�ӣ�ϴ�Ӿ������õ��Լ�Ϊ���ѧʽ��CH3CH2OH��C2H5OH����C2H6O��
��7��Ϊ�����ƵõIJ�Ʒ�Ĵ��ȣ���ʵ��С���ȡ5.0�˵IJ�Ʒ���Ƴ�250mL��Һ�����ü�ӵ������궨����Һ��Ũ�ȣ�����ƿ�м���25mL0.01mol/LKIO3��Һ�������������KI�ữ���������з�Ӧ��5I-+IO3-+6H+=3I2+3H2O���ټ��뼸�ε�����Һ������������Na2S2O3��Һ�ζ���������Ӧ��I2+2S2O32-=2I-+S4O62-������ɫ��ȥ�Ұ���Ӳ���ɫʱ�ﵽ�ζ��յ㣮ʵ���������±���
| ʵ����� | 1 | 2 | 3 |
| Na2S2O3��Һ�����mL�� | 19.98 | 20.02 | 21.18 |
A���ζ��յ�ʱ���Ӷ���
B����ƿ������ˮ��ϴ
C���ζ���δ��Na2S2O3��Һ��ϴ
D���ζ��ܼ��촦�ζ�ǰ�����ݣ��ζ��յ㷢�����ݣ�
| A�� | D��E����Ԫ�ؽ�����ɻ�ѧʽΪE2D�Ļ����� | |
| B�� | ԭ�Ӱ뾶��E��F��C��D | |
| C�� | F��D�γɵĻ��������ʺܲ����ã������κ��ᷴӦ | |
| D�� | Ԫ�صķǽ����ԣ�D��C��F��B |
| A�� | ����β������ҵ�������ŷ����γɡ�����������Ҫԭ�� | |
| B�� | ����������ʢ��Ũ���ᣬ����Ϊ����Ũ�����Ӧ | |
| C�� | ����ֱ���ͨ�ֿ���ʴ����ǿ������Ϊ�������һ��� | |
| D�� | �������������ڽ��ػ���������������һ�����ָ��£������������ǽ������� |
| A�� | ���м���Ũ��ˮ�����ۣ����ȣ��ټ���AgNO3��Һ������������˵������Ũ��ˮ������ȡ����Ӧ | |
| B�� | ʵ�����Ʊ�����Ȳ����ͨ������һ���Ĵ̼�����ζ������ͨ��NaOH��Һ��Ũ����ϴ������ô�������Ȳ | |
| C�� | ��2%��AgNO3��Һ����εμ�2%�İ�ˮ��ֱ�������İ�ɫ����ǡ����ʧ�������Ƶõ�������Һ | |
| D�� | ��NaOH��Һ�м��������飬���ȣ��ټ���AgNO3��Һ������������˵�������鷢����ˮ�ⷴӦ |
| A�� | ��Ca��ClO��2��Һ��ͨ������SO2Ca2++3ClO-+SO2+H2O�TCaSO4��+Cl-+2HClO | |
| B�� | 1mol/L��NaAlO2��Һ��2.5mol/L�������������Ȼ�ϣ�2AlO2-+5H+�TAl��OH��3��+Al3++H2O | |
| C�� | ��11.2L��״���µ�����ͨ��200mL2mol/L��FeBr2��Һ�У����ӷ�Ӧ����ʽΪ��2Fe2++8Br-+5Cl2�T2Fe3++4Br2+10Cl- | |
| D�� | ��NH4HCO3��Һ�м�������NaAlO2��Һ��NH4++2AlO2-+HCO3--+2H2O�TNH3��+2Al��OH��3��+CO32-�� |
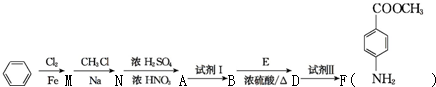
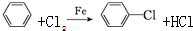
 �����������ԣ���������
�����������ԣ���������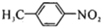 ��
��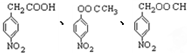 ����2�֣�
����2�֣�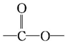 �ṹ��
�ṹ��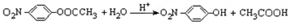 ��
��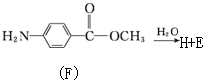 ������H��һ�������¾����۷�Ӧ���Ƶø߷�����ά���㷺����ͨѶ�����������������д�������۷�Ӧ�Ļ�ѧ����ʽ
������H��һ�������¾����۷�Ӧ���Ƶø߷�����ά���㷺����ͨѶ�����������������д�������۷�Ӧ�Ļ�ѧ����ʽ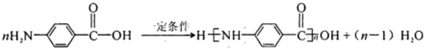 ��
��