题目内容
在标准状况下,物质①1gH2;②44.8L CH4;③3molH2O;④6.02×1023个O2.上述物质中,含分子数最多的是(选填编号,下同) ,含原子数最少的是 ,质量最大的是 .
考点:物质的量的相关计算
专题:
分析:根据n=
=
=
计算氢气、甲烷、氧气的物质的量,根据N=nNA可知,物质的量越大,含有的分子数越多,结合分子含有原子数目计算各物质含有原子总物质的量,根据N=nNA可知,物质的量越大,含有的分子数越多,原子数目越多,再根据m=nM计算甲烷、水、氧气的质量进行判断.
| m |
| M |
| V |
| Vm |
| N |
| NA |
解答:
解:①1gH2的物质的量为
=0.5mol,氢原子物质的量为0.5mol×2=1mol;
②标况下44.8L CH4的物质的量为
=2mol,含有原子物质的量为2mol×5=10mol,甲烷的质量为2mol×16g/mol=32g;
③3molH2O含有原子物质的量为3mol×3=9mol,水的质量为3mol×18g/mol=54g;
④6.02×1023个O2的物质的量为
=1mol,含有原子物质的量为1mol×2=2mol,氧气的质量为1mol×32g/mol=32g,
故3molH2O含有分子数目、质量最大,1gH2的含有原子数目最少,
故答案为:③;①;③.
| 1g |
| 2g/mol |
②标况下44.8L CH4的物质的量为
| 44.8L |
| 22.4L/mol |
③3molH2O含有原子物质的量为3mol×3=9mol,水的质量为3mol×18g/mol=54g;
④6.02×1023个O2的物质的量为
| 6.02×1023 |
| 6.02×1023mol-1 |
故3molH2O含有分子数目、质量最大,1gH2的含有原子数目最少,
故答案为:③;①;③.
点评:本题考查物质的量有关计算,侧重考查微粒数目的计算,比较基础,注意掌握以物质的量为中心的有关计算.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
日本福岛核电站泄漏物中含有放射性的
I.有关
I的说法正确是( )
131 53 |
131 53 |
| A、核外电子数为78 | ||
B、与
| ||
| C、中子数为131 | ||
D、与
|
在下列各组物质中,只有还原性的是( )
| A、Cl- CO Na+、 |
| B、Na Cl- S2- |
| C、Fe3+ SO42- NO3- |
| D、Fe2+ O2 H2S |
“摩尔”是表示( )
| A、物质的质量单位 |
| B、物质微粒的个数单位 |
| C、6.02×1023个微粒的集体 |
| D、物质“物质的量”的单位 |
下列实验方法正确的是( )
| A、从溴水中提取溴可用酒精作为萃取剂 |
| B、检验碘化钾溶液可用淀粉 |
| C、分离碘和食盐可用加热的方法 |
| D、用加热的方法除去铜中混有的氧化铜 |
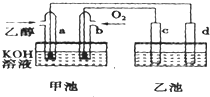 如图甲池和乙池中的四个电极都是惰性材料,溶液体积均为200mL,请根据图示回答下列问题
如图甲池和乙池中的四个电极都是惰性材料,溶液体积均为200mL,请根据图示回答下列问题