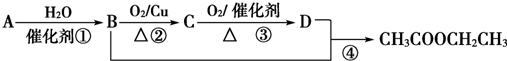
题目内容
5.六种短周期元素在周期表中的相对位置如下所示,其中E元素原子核外电子总数是其最外层电子数的3倍.关于元素周期表及这六种元素性质,请回答:| A | B | C |
| D | E | F |
(2)AC2的电子式为
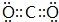 .
.(3)在一定条件下,由B单质与H2反应生成1molG时,放出的热量为46.2kJ,写出该反应的热化学方程式:N2(g)+3H2(g)?2NH3(g)△H=-92.4 kJ/mol.
(4)工业上用G检验输送氯气的管道是否漏气,可观察到大量白烟,同时有单质B生成,写出化学方程式8NH3+3Cl2═6NH4Cl+N2.该反应中被氧化的G与参与反应的G的质量之比1:4.
(5)F的单质可由其氧化物与氢化物反应生成,写出该反应的化学方程式:2H2S+SO2=3S↓+2H2O.
分析 由短周期元素相对位置,可知A、B、C处于第二周,D、E、F处于第三周期,E元素原子核外电子总数是其最外层电子数的3倍,设核外最外层电子数为x,则有(2+8+x)=3x,解得x=5,则E为P元素,可知A为碳元素,B为N元素,C为O元素,D为Si,F为S元素.
解答 解:由短周期元素相对位置,可知A、B、C处于第二周,D、E、F处于第三周期,E元素原子核外电子总数是其最外层电子数的3倍,设核外最外层电子数为x,则有(2+8+x)=3x,解得x=5,则E为P元素,可知A为碳元素,B为N元素,C为O元素,D为Si,F为S元素.
(1)这六种元素中O元素非金属性最强,故氢化物中,最稳定的是H2O,故答案为:H2O;
(2)CO2的电子式为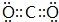 ,故答案为:
,故答案为: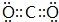 ;
;
(3)在一定条件下,由氮气与H2反应生成1molG(氨气)时,放出的热量为46.2kJ,该反应的热化学方程式:N2(g)+3H2(g)?2NH3(g)△H=-92.4 kJ/mol,
故答案为:N2(g)+3H2(g)?2NH3(g)△H=-92.4 kJ/mol;
(4)工业上用G(氨气)检验输送氯气的管道是否漏气,可观察到大量白烟,同时有单质B生成,反应生成氯化铵与氮气,反应方程式为:8NH3+3Cl2═6NH4Cl+N2,反应中被氧化的氨气与参与反应的氨气的质量之比为2:8=1:4,
故答案为:8NH3+3Cl2═6NH4Cl+N2;1:4;
(5)F(硫)的单质可由其氧化物与氢化物反应生成,该反应的化学方程式:2H2S+SO2=3S↓+2H2O,
故答案为:2H2S+SO2=3S↓+2H2O.
点评 本题考查结构性质位置关系应用,熟练掌握元素周期表的结构,注意对基础知识的理解掌握.

练习册系列答案
相关题目
15.在水电离出的c(H+)=1×10-14 mol•L-1的溶液中,一定能大量共存的离子组是( )
| A. | K+、Na+、HCO3-、Cl- | B. | K+、AlO2-、Br-、Cl- | ||
| C. | Na+、Cl-、NO3-、SO42- | D. | Al3+、NH4+、Cl-、SO42- |
16.下列说法正确的是( )
| A. | 原子最外层电子数等于或大于4的元素一定是非金属元素 | |
| B. | 原子最外层只有2个电子的元素一定是金属元素 | |
| C. | 最外层电子数比次外层电子数多的元素一定位于第二周期 | |
| D. | 某元素的离子最外层电子数与次外层电子数相同,该元素一定位于第三周期 |
13.关于化学键的下列叙述中,正确的是( )
| A. | 离子化合物可能含共价键 | B. | 共价化合物可能含离子键 | ||
| C. | 离子化合物中只含离子键 | D. | 共价化合物中可能含共价键 |
20.下列递变规律不正确的是( )
| A. | Na、Mg、Al还原性依次减弱 | B. | Cl2、Br2、I2氧化性依次增强 | ||
| C. | Be、Mg、Ca与盐酸反应越来越剧烈 | D. | P、S、Cl最高正价依次升高 |
10.甲醇是重要的化工原料,又是一种可再生能源,具有广泛的开发和应用前景.
(1)已知反应CO(g)+2H2(g)?CH3OH(g)△H=-99kJ.mol-1中的相关化学键键能如下:
则x=1076.
(2)在一容积可变的密闭容器中,1molCO与2molH2发生反应:CO(g)+2H2(g)$\stackrel{催化剂}{?}$ CH3OH(g)
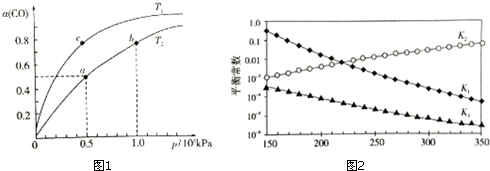
△H1<0,CO在不同温度下的平衡转化率(α)与压强的关系如图1所示.
①a、b两点的反应速率:v(a)<v(b)(填“>”、“<”、“=”)
②T1<T2 (填“>”、“<”、“=”),原因是而正反应是放热反应,温度升高,平衡逆向移动,CO的平衡转化率减小,故Tl<T2.
③在c点条件下,下列叙述能说明上述反应能达到化学平衡状态的是bc(填代号)
a.H2的消耗速率是CH3OH生成速率的2倍
b.CH3OH的体积分数不再改变
c.混合气体的密度不再改变
d.CO和CH3OH的物质的量之和保持不变
④计算图1中a点的平衡常数KP=1.6×10-7(kPa)-2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数).
(3)利用合成气(主要成分为CO、CO2和H2)合成甲醇,发生的主要反应如下:
I:CO(g)+2H2(g)$\stackrel{催化剂}{?}$ CH3OH(g)△H1
Ⅱ:CO2(g)+H2(g)$\stackrel{催化剂}{?}$ CO(g)+H2O(g)△H2
Ⅲ:CO2(g)+3H2(g)$\stackrel{催化剂}{?}$ CH3OH(g)+H2O(g)△H3
上述反应对应的平衡常数分别为K1、K2、K3,它们随温度变化的曲线如图2所示.则△H1>△H3(填“>”、“<”、“=”),理由是曲图l可知,随着温度升高,K1减小,则△H1<0,根据盖斯定律又得△H3=△H1+△H2,所以△H2>△H3.
(1)已知反应CO(g)+2H2(g)?CH3OH(g)△H=-99kJ.mol-1中的相关化学键键能如下:
| 化学键 | H-H | C-O | C≡C | H-O | C-H |
| E/(KJ.mol-1) | 436 | 343 | x | 465 | 413 |
(2)在一容积可变的密闭容器中,1molCO与2molH2发生反应:CO(g)+2H2(g)$\stackrel{催化剂}{?}$ CH3OH(g)
△H1<0,CO在不同温度下的平衡转化率(α)与压强的关系如图1所示.
①a、b两点的反应速率:v(a)<v(b)(填“>”、“<”、“=”)
②T1<T2 (填“>”、“<”、“=”),原因是而正反应是放热反应,温度升高,平衡逆向移动,CO的平衡转化率减小,故Tl<T2.
③在c点条件下,下列叙述能说明上述反应能达到化学平衡状态的是bc(填代号)
a.H2的消耗速率是CH3OH生成速率的2倍
b.CH3OH的体积分数不再改变
c.混合气体的密度不再改变
d.CO和CH3OH的物质的量之和保持不变
④计算图1中a点的平衡常数KP=1.6×10-7(kPa)-2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数).

(3)利用合成气(主要成分为CO、CO2和H2)合成甲醇,发生的主要反应如下:
I:CO(g)+2H2(g)$\stackrel{催化剂}{?}$ CH3OH(g)△H1
Ⅱ:CO2(g)+H2(g)$\stackrel{催化剂}{?}$ CO(g)+H2O(g)△H2
Ⅲ:CO2(g)+3H2(g)$\stackrel{催化剂}{?}$ CH3OH(g)+H2O(g)△H3
上述反应对应的平衡常数分别为K1、K2、K3,它们随温度变化的曲线如图2所示.则△H1>△H3(填“>”、“<”、“=”),理由是曲图l可知,随着温度升高,K1减小,则△H1<0,根据盖斯定律又得△H3=△H1+△H2,所以△H2>△H3.
17.表是元素周期表的一部分,回答下列问题:
(1)写出①、②两种元素的名称:碳、氮.
(2)写出⑧、⑨两种元素的符号:Si、P.
(3)在这些元素中,最活泼的金属的离子结构示意图是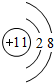 ,最活泼的非金属元素是F (填元素符号,下同),Ar是最不活泼的元素.
,最活泼的非金属元素是F (填元素符号,下同),Ar是最不活泼的元素.
(4)这些元素的最高价氧化物对应水化物中,HClO4(填化学式,下同)酸性最强,NaOH的碱性最强;能形成两性氢氧化物的元素是Al(填元素符号).
(5)在⑤到⑪的元素中,Cl(填元素符号)原子半径最小.
(6)比较⑤和⑥的化学性质,Na(填元素符号)更活泼,试用实验证明之(简述操作、现象和结论)金属钠与金属镁单质分别与冷水反应,反应剧烈程度大的是钠,反之是镁.
| 族 周期 | IA | IIA | IIIA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑪ | ⑫ |
(2)写出⑧、⑨两种元素的符号:Si、P.
(3)在这些元素中,最活泼的金属的离子结构示意图是
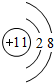 ,最活泼的非金属元素是F (填元素符号,下同),Ar是最不活泼的元素.
,最活泼的非金属元素是F (填元素符号,下同),Ar是最不活泼的元素.(4)这些元素的最高价氧化物对应水化物中,HClO4(填化学式,下同)酸性最强,NaOH的碱性最强;能形成两性氢氧化物的元素是Al(填元素符号).
(5)在⑤到⑪的元素中,Cl(填元素符号)原子半径最小.
(6)比较⑤和⑥的化学性质,Na(填元素符号)更活泼,试用实验证明之(简述操作、现象和结论)金属钠与金属镁单质分别与冷水反应,反应剧烈程度大的是钠,反之是镁.