题目内容
某含C、H、O三种元素的有机物4.6g完全燃烧,若将生成的气体全部通过浓硫酸,则浓硫酸质量增加5.4g;若将生成的气体全部通过足量的过氧化钠,过氧化钠的质量增加6.2g(假定气体全部吸收).
(1)试通过计算推断该有机物的分子式.
(2)该有机物有多种同分异构体,其中一种能和Na反应生成H2,请试写出该有机物的结构简式: .
(1)试通过计算推断该有机物的分子式.
(2)该有机物有多种同分异构体,其中一种能和Na反应生成H2,请试写出该有机物的结构简式:
考点:有关有机物分子式确定的计算
专题:烃及其衍生物的燃烧规律
分析:浓硫酸质量增加5.4g为燃烧生成水的质量;若将生成的气体全部通过足量的过氧化钠,水、二氧化碳都与过氧化钠反应,根据差量法计算水反应导致固体增重,再计算二氧化碳与过氧化钠发生导致固体增重,进而计算二氧化碳的质量,根据n=
计算水、二氧化碳的物质的量,再根据质量守恒定律确定是否含有O元素及其质量,确定有机物的最简式,据此确定分子式,该有机物能与Na反应生成氢气,则有机物含有羟基、羧基中的至少一种,结合分子式确定其结构简式.
| m |
| M |
解答:
解:(1)浓硫酸质量增加5.4g为燃烧生成水的质量,其物质的量=
=0.3mol,n(H)=0.3mol×2=0.6 mol,
Na2O2+2H2O=4NaOH+O2 △(m)
36 32 4
5.4 g m(H)
m(H)=
=0.6 g
Na2O2+2CO2=2Na2CO3+O2 △(m)
88 32 56
m(CO2) 6.2 g-m(H)=6.2g-0.6g=5.6g
m(CO2)=
=8.8 g
n(C)=
=0.2 mol
m(C)+m(H)=0.2mol×12g/mol+0.6mol×1g/mol=3g<4.6g,故有机物还含有O元素,则n(O)=
=0.1 mol
故该有机物分子中C、H、O原子数目之比=n(C):n(H):n(O)=0.2:0.6:0.1=2:6:1,有机物的最简式为C2H6O,H原子已经饱和C的四价结构,故有机物分子式为C2H6O,
答:该有机物分子式为C2H6O.
(2)该有机物分子式为C2H6O,能与Na反应生成氢气,则有机物含有羟基,其结构简式为CH3CH2OH,
故答案为:CH3CH2OH.
| 5.4g |
| 18g/mol |
Na2O2+2H2O=4NaOH+O2 △(m)
36 32 4
5.4 g m(H)
m(H)=
| 5.4g×4 |
| 36 |
Na2O2+2CO2=2Na2CO3+O2 △(m)
88 32 56
m(CO2) 6.2 g-m(H)=6.2g-0.6g=5.6g
m(CO2)=
| 5.6g×88 |
| 56 |
n(C)=
| 8.8g |
| 44g/mol |
m(C)+m(H)=0.2mol×12g/mol+0.6mol×1g/mol=3g<4.6g,故有机物还含有O元素,则n(O)=
| 4.6g-3g |
| 16g/mol |
故该有机物分子中C、H、O原子数目之比=n(C):n(H):n(O)=0.2:0.6:0.1=2:6:1,有机物的最简式为C2H6O,H原子已经饱和C的四价结构,故有机物分子式为C2H6O,
答:该有机物分子式为C2H6O.
(2)该有机物分子式为C2H6O,能与Na反应生成氢气,则有机物含有羟基,其结构简式为CH3CH2OH,
故答案为:CH3CH2OH.
点评:本题考查有机物分子式确定,难度中等,关键是利用差量法确定二氧化碳的质量.

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目
甲基环己烷可由甲苯与氢气加成制得,其环上一氯代物的同分异构体数目是( )
| A、4 | B、3 | C、2 | D、1 |
在由水电离出的c(H+)=1×10-13mol/L的溶液中,一定可以大量共存的是( )
| A、Ba2+Na+ NO3-Cl- |
| B、Fe2+ Na+ NO3- Cl- |
| C、SO42-SO32- NH4+Na+ |
| D、Mg2+Na+Br-AlO2- |
设NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、46g有机物C2H6O中含有的H-O键的数目为NA |
| B、常温下,2L 1mol?L-1的乙酸溶液中,所含分子总数小于2NA |
| C、标准状况下,5.6L NO和5.6L O2组成的混合气体中所含原子数为NA |
| D、18g D2O含有的电子总数为10NA |
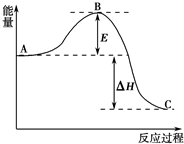 2SO2(g)+O2(g)?2SO3(g),反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ?mol-1.
2SO2(g)+O2(g)?2SO3(g),反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ?mol-1.