题目内容
在由水电离出的c(H+)=1×10-13mol/L的溶液中,一定可以大量共存的是( )
| A、Ba2+Na+ NO3-Cl- |
| B、Fe2+ Na+ NO3- Cl- |
| C、SO42-SO32- NH4+Na+ |
| D、Mg2+Na+Br-AlO2- |
考点:离子共存问题
专题:离子反应专题
分析:由水电离产生的c(H+)=1×10-13mol/L,为酸或碱溶液,根据离子之间不能结合生成水、气体、沉淀,不能发生氧化还原反应等,则离子大量共存,以此来解答.
解答:
解:A.无论溶液呈酸性还是碱性,离子之间都不发生任何反应,可大量共存,故A正确;
B.酸性条件下,NO3-与Fe2+发生氧化还原反应,碱性条件下Fe2+不能大量共存,故B错误;
C.酸性条件下SO32-不能大量共存,碱性条件下NH4+不能大量共存,故C错误;
D.AlO2-与Mg2+发生互促水解反应,碱性条件下Mg2+不能大量共存,酸性条件下AlO2-不能大量共存,故D错误.
故选A.
B.酸性条件下,NO3-与Fe2+发生氧化还原反应,碱性条件下Fe2+不能大量共存,故B错误;
C.酸性条件下SO32-不能大量共存,碱性条件下NH4+不能大量共存,故C错误;
D.AlO2-与Mg2+发生互促水解反应,碱性条件下Mg2+不能大量共存,酸性条件下AlO2-不能大量共存,故D错误.
故选A.
点评:本题考查离子的共存,为高考常见题型,注重信息的抽取和氧化还原反应的考查,对学生思维严密性有较好的训练,具有坚实的基础知识即可解答,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
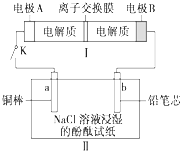 如图所示装置Ⅰ是一种可充电电池,装置Ⅱ为电解池.离子交换膜只允许Na+通过,充放电的化学方程式为Na2S4+3NaBr
如图所示装置Ⅰ是一种可充电电池,装置Ⅱ为电解池.离子交换膜只允许Na+通过,充放电的化学方程式为Na2S4+3NaBr
| ||
| 放电 |
| A、负极反应为4Na-4e-═4Na+ |
| B、闭合K后,b电极附近的pH变小 |
| C、闭合K后,a电极上有气体产生 |
| D、当有0.01mol Na+通过离子交换膜时,b电极上析出标准状况下的气体112mL |
化学与科学、技术、社会、环境密切相关.下列叙述正确的是:①NO2、CO2和SO2都是大气污染物;②为了防止食品受潮变质,常在食品包装袋中放入活性铁粉;③单质硅是将太阳能转变为电能的常用材料;④维生素C易失电子,在人体内起抗氧化作用( )
| A、①② | B、②③ | C、③④ | D、①④ |
对于常温下0.01mol/L的氨水,下列叙述正确的是( )
| A、c(H+)+c(NH4+)=2c(OH-) |
| B、由H2O电离出的c(H+)=1.0×10-12mol?L-1 |
| C、与等体积等浓度的氯化铵溶液混合c(NH4+)+c(NH3?H2O)+c(NH3)=0.02mol?L-1 |
| D、与等体积等浓度的盐酸混合后所得溶液c(OH-)+c(NH3?H2O)+c(NH3)=c(H+) |
有等体积的NaCl、CaCl2、AlCl3溶液,完全沉淀其中的Cl-消耗同浓度的AgNO3溶液体积相等,则三种溶质的浓度之比为( )
| A、1:1:1 |
| B、1:2:3 |
| C、6:3:2 |
| D、3:2:1 |
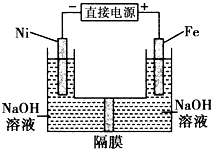 高铁酸盐在能源环保领域有广泛用途.用镍(Ni)、铁做电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的装置如图所示.下列推断合理的是( )
高铁酸盐在能源环保领域有广泛用途.用镍(Ni)、铁做电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的装置如图所示.下列推断合理的是( )| A、铁是阳极,电极反应为Fe-6e-+4H2O═FeO42-+8H+ |
| B、镍电极上的电极反应为2H2O+2e-═H2↑+2OH- |
| C、若隔膜为阴离子交换膜,则OH-自右向左移动 |
| D、电解时阳极区pH降低、阴极区pH升高,最终溶液pH不变 |
在密闭容器中,加热等物质的量的NaHCO3和Na2O2的固体混合物,充分反应后,容器中固体剩余物是( )
| A、Na2CO3和Na2O2 |
| B、Na2CO3和NaOH |
| C、NaOH和Na2O2 |
| D、NaOH、Na2O2和Na2CO3 |