题目内容
设NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、46g有机物C2H6O中含有的H-O键的数目为NA |
| B、常温下,2L 1mol?L-1的乙酸溶液中,所含分子总数小于2NA |
| C、标准状况下,5.6L NO和5.6L O2组成的混合气体中所含原子数为NA |
| D、18g D2O含有的电子总数为10NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.C2H6O可能为二甲醚,二甲醚分子中不存在氧氢键;
B.乙酸溶液中,含有乙酸分子和水分子;
C.根据化学反应中遵循质量守恒定律计算出含有的原子数目;
D.重水中含有10个电子,重水的摩尔质量为20g/mol,18g重水的物质的量为0.9mol,含有9mol电子.
B.乙酸溶液中,含有乙酸分子和水分子;
C.根据化学反应中遵循质量守恒定律计算出含有的原子数目;
D.重水中含有10个电子,重水的摩尔质量为20g/mol,18g重水的物质的量为0.9mol,含有9mol电子.
解答:
解:A.46g有机物C2H6O的物质的量为1mol,C2H6O可能为二甲醚,二甲醚分子中不存在C-H键,故A错误;
B.2L 1mol?L-1的乙酸溶液中含有溶质乙酸2mol,由于溶液中含有水分子,醋酸只是部分电离,所以溶液中含有的分子大于2mol,所含分子总数大于2NA,故B错误;
C.标况下,5.6L NO的物质的量为0.25mol,含有0.5mol原子,5.6L O2的物质的量为0.25mol,含有0.5mol氧原子,根据质量守恒,混合气体中总共含有1mol原子,所含原子数为NA,故C正确;
D.18g重水的物质的量为0.9mol,0.9mol重水中含有9mol电子,有的电子总数为9NA,故D错误;
故选C.
B.2L 1mol?L-1的乙酸溶液中含有溶质乙酸2mol,由于溶液中含有水分子,醋酸只是部分电离,所以溶液中含有的分子大于2mol,所含分子总数大于2NA,故B错误;
C.标况下,5.6L NO的物质的量为0.25mol,含有0.5mol原子,5.6L O2的物质的量为0.25mol,含有0.5mol氧原子,根据质量守恒,混合气体中总共含有1mol原子,所含原子数为NA,故C正确;
D.18g重水的物质的量为0.9mol,0.9mol重水中含有9mol电子,有的电子总数为9NA,故D错误;
故选C.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系,选项A、B为易错点,注意分子式C2H6O可能为乙醇或二甲醚、乙酸溶液中存在水分子.

练习册系列答案
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案
相关题目
下列有关电极和电解质溶液构成的装置叙述不正确的是( )
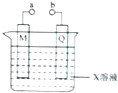

| A、若X、M、Q分别是H2SO4、Pb和PbO2,a、b连接后两极都有PbSO4生成 |
| B、若X、M、Q分别是CuSO4、Ag和Fe无论a、b是否连接Fe都被腐蚀 |
| C、若X、M、Q分别CuSO4、Cu和Fe,a、b是分别连接电源的正负极,则可对铁镀铜 |
| D、若X、M、Q分别是NaCl、C和Fe,则a、b连接后,M电极上有气体产生 |
对于常温下0.01mol/L的氨水,下列叙述正确的是( )
| A、c(H+)+c(NH4+)=2c(OH-) |
| B、由H2O电离出的c(H+)=1.0×10-12mol?L-1 |
| C、与等体积等浓度的氯化铵溶液混合c(NH4+)+c(NH3?H2O)+c(NH3)=0.02mol?L-1 |
| D、与等体积等浓度的盐酸混合后所得溶液c(OH-)+c(NH3?H2O)+c(NH3)=c(H+) |
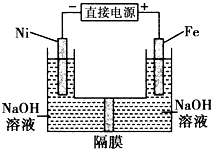 高铁酸盐在能源环保领域有广泛用途.用镍(Ni)、铁做电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的装置如图所示.下列推断合理的是( )
高铁酸盐在能源环保领域有广泛用途.用镍(Ni)、铁做电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的装置如图所示.下列推断合理的是( )| A、铁是阳极,电极反应为Fe-6e-+4H2O═FeO42-+8H+ |
| B、镍电极上的电极反应为2H2O+2e-═H2↑+2OH- |
| C、若隔膜为阴离子交换膜,则OH-自右向左移动 |
| D、电解时阳极区pH降低、阴极区pH升高,最终溶液pH不变 |
在密闭容器中,加热等物质的量的NaHCO3和Na2O2的固体混合物,充分反应后,容器中固体剩余物是( )
| A、Na2CO3和Na2O2 |
| B、Na2CO3和NaOH |
| C、NaOH和Na2O2 |
| D、NaOH、Na2O2和Na2CO3 |
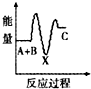
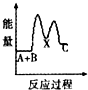
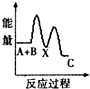
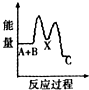
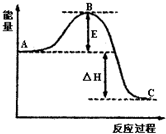 H2O2是重要的氧化剂,它的水溶液常用来消毒、杀菌、漂白等.请回答下列有关问题.
H2O2是重要的氧化剂,它的水溶液常用来消毒、杀菌、漂白等.请回答下列有关问题.