题目内容
甲基环己烷可由甲苯与氢气加成制得,其环上一氯代物的同分异构体数目是( )
| A、4 | B、3 | C、2 | D、1 |
考点:有机化合物的异构现象
专题:同分异构体的类型及其判定
分析:甲基环己烷比甲苯多一种氢原子(与甲基相连的碳上的氢原子),根据环上一氯代物的同分异构体等于环上氢原子的种类来解答.
解答:
解:甲基环己烷中与甲基相连的碳上有一个氢原子,还能够被取代,甲基环己烷中环上含有4种氢原子,环上一氯取代物有4种,
故选A.
故选A.
点评:本题考查同分异构体的书写,难度不大,注意根据题意解题.

练习册系列答案
相关题目
常温时,下列各组离子在指定溶液中一定不能大量共存的是( )
| A、含有大量NO3-的溶液中:Na+、OH-、I-、SO32- |
| B、pH<7的溶液中:Cu2+、Fe3+、NO3-、Cl- |
| C、使石蕊试液变蓝的溶液中:K+、SO32-、S2-、CO32- |
D、c( )=0.1mol/L的溶液中:Na+、Fe3+、SO42-、NO3- )=0.1mol/L的溶液中:Na+、Fe3+、SO42-、NO3- |
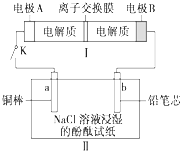 如图所示装置Ⅰ是一种可充电电池,装置Ⅱ为电解池.离子交换膜只允许Na+通过,充放电的化学方程式为Na2S4+3NaBr
如图所示装置Ⅰ是一种可充电电池,装置Ⅱ为电解池.离子交换膜只允许Na+通过,充放电的化学方程式为Na2S4+3NaBr
| ||
| 放电 |
| A、负极反应为4Na-4e-═4Na+ |
| B、闭合K后,b电极附近的pH变小 |
| C、闭合K后,a电极上有气体产生 |
| D、当有0.01mol Na+通过离子交换膜时,b电极上析出标准状况下的气体112mL |
下列有关电极和电解质溶液构成的装置叙述不正确的是( )
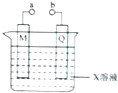

| A、若X、M、Q分别是H2SO4、Pb和PbO2,a、b连接后两极都有PbSO4生成 |
| B、若X、M、Q分别是CuSO4、Ag和Fe无论a、b是否连接Fe都被腐蚀 |
| C、若X、M、Q分别CuSO4、Cu和Fe,a、b是分别连接电源的正负极,则可对铁镀铜 |
| D、若X、M、Q分别是NaCl、C和Fe,则a、b连接后,M电极上有气体产生 |
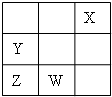 W、X、Y、Z为短周期元素,在周期表中位置如图所示,有关元素W、X、Y、Z的叙述,不正确的是( )
W、X、Y、Z为短周期元素,在周期表中位置如图所示,有关元素W、X、Y、Z的叙述,不正确的是( )| A、通常情况下四种元素的单质中,X化学性质最稳定 |
| B、四种元素都能与氢元素形成稳定的化合物 |
| C、Y、Z离子最外层电子数相同 |
| D、四种元素中Z元素最高价氧化物对应的水化物酸性最强 |
下列有机物中,常温下呈气态的是( )
| A、CH3Cl |
| B、CH2Cl2 |
| C、CCl4 |
| D、CH3COOH |
化学与科学、技术、社会、环境密切相关.下列叙述正确的是:①NO2、CO2和SO2都是大气污染物;②为了防止食品受潮变质,常在食品包装袋中放入活性铁粉;③单质硅是将太阳能转变为电能的常用材料;④维生素C易失电子,在人体内起抗氧化作用( )
| A、①② | B、②③ | C、③④ | D、①④ |
对于常温下0.01mol/L的氨水,下列叙述正确的是( )
| A、c(H+)+c(NH4+)=2c(OH-) |
| B、由H2O电离出的c(H+)=1.0×10-12mol?L-1 |
| C、与等体积等浓度的氯化铵溶液混合c(NH4+)+c(NH3?H2O)+c(NH3)=0.02mol?L-1 |
| D、与等体积等浓度的盐酸混合后所得溶液c(OH-)+c(NH3?H2O)+c(NH3)=c(H+) |