题目内容
9.能证明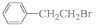 与过量NaOH醇溶液共热时发生了消去反应的是( )
与过量NaOH醇溶液共热时发生了消去反应的是( )| A. | 混合体系$\stackrel{溴水}{→}$Br2的颜色褪去 | |
| B. | 混合体系$\stackrel{足量稀HNO_{3}}{→}$ $\stackrel{AgNO_{3}溶液}{→}$淡黄色沉淀 | |
| C. | 混合体系$\stackrel{提取}{→}$有机物$\stackrel{酸性KMnO_{4}溶液}{→}$紫色褪去 | |
| D. | 混合体系$\stackrel{提取}{→}$有机物$\stackrel{Br_{2}的CCl_{4}溶液}{→}$Br2的颜色褪去 |
分析 根据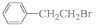 与过量NaOH醇溶液共热时发生了消去反应生成苯乙烯,苯乙烯、乙醇都能使酸性高锰酸钾溶液褪色,苯乙烯能使溴水褪色,乙醇不能使溴水褪色来解答;
与过量NaOH醇溶液共热时发生了消去反应生成苯乙烯,苯乙烯、乙醇都能使酸性高锰酸钾溶液褪色,苯乙烯能使溴水褪色,乙醇不能使溴水褪色来解答;
解答 解:A.混合体系$\stackrel{溴水}{→}$Br2的颜色褪去,可能是单质溴与碱反应,也可能单质溴与烯烃发生加成反应,无法证明发生消去反应,故A错误;
B.混合体系$\stackrel{足量稀HNO_{3}}{→}$ $\stackrel{AgNO_{3}溶液}{→}$淡黄色沉淀,说明生成了溴离子,而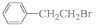 发生水解反应和消去反应都能生成溴离子,无法证明发生消去反应,故B正确;
发生水解反应和消去反应都能生成溴离子,无法证明发生消去反应,故B正确;
C.合体系$\stackrel{提取}{→}$有机物$\stackrel{酸性KMnO_{4}溶液}{→}$紫色褪去,乙醇也能使酸性高锰酸钾溶液褪色,无法证明发生消去反应,故C错误;
D.混合体系$\stackrel{提取}{→}$有机物$\stackrel{Br_{2}的CCl_{4}溶液}{→}$Br2的颜色褪去,说明有苯乙烯生成,能证明发生消去反应,故D正确.
故选D.
点评 本题考查有机物的结构与性质,把握卤代烃消去反应和水解反应产物及性质为解答的关键,注意涉及实验方案的严密性,题目难度不大.

练习册系列答案
相关题目
19. Mn、Fe均为第四周期过渡元素,部分电离能数据如表所示,请回答下列问题:
Mn、Fe均为第四周期过渡元素,部分电离能数据如表所示,请回答下列问题:
(1)Mn元素基态原子的电子排布式为[Ar]3d54s2,比较两元素的I2、I3可知,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难.其原因是由Mn2+转化为Mn3+时,3d能级由较稳定的3d5半充满状态转为不稳定的3d4状态需要的能量较多,而Fe2+到Fe3+时,3d能级由不稳定的3d6到稳定的3d5半充满状态,需要的能量相对要少.
(2)氯化铁常温下为固体,熔点282℃,沸点315℃,在300℃以上易升华.易溶于水,也易溶于乙醚、丙酮等有机溶剂.则氯化铁的晶体类型为分子晶体.
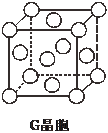
(3)金属铁的晶体在不同的温度下有两种堆积方式,如图所示.则体心立方晶胞和面心立方晶胞中实际含有的Fe原子个数之比为1:2.
(4)下列分子或离子中,能提供孤电对与Cu2+形成配位键的是D.(填字母,下同)
①H2O ②NH3 ③F- ④CN-
A.仅①②B.仅①②③C.仅①②④D.①②③④
(5)向盛有硫酸铜溶液的试管中加入氨水,首先形成难溶物,继续加入氨水,难溶物溶解并得到深蓝色的透明溶液.下列叙述正确的是B.
A.反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变
B.沉淀溶解后生成深蓝色的[Cu(NH3)4]2+
C.若硫酸铜溶液中混有少量硫酸,则可用氨水除去硫酸铜溶液中的硫酸
D.[Cu(NH3)4]2+的空间构型为平面正方形.
 Mn、Fe均为第四周期过渡元素,部分电离能数据如表所示,请回答下列问题:
Mn、Fe均为第四周期过渡元素,部分电离能数据如表所示,请回答下列问题:| 元素 | Mn | Fe | |
| 电离能(kJ•mol-1) | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
(2)氯化铁常温下为固体,熔点282℃,沸点315℃,在300℃以上易升华.易溶于水,也易溶于乙醚、丙酮等有机溶剂.则氯化铁的晶体类型为分子晶体.
(3)金属铁的晶体在不同的温度下有两种堆积方式,如图所示.则体心立方晶胞和面心立方晶胞中实际含有的Fe原子个数之比为1:2.
(4)下列分子或离子中,能提供孤电对与Cu2+形成配位键的是D.(填字母,下同)
①H2O ②NH3 ③F- ④CN-
A.仅①②B.仅①②③C.仅①②④D.①②③④
(5)向盛有硫酸铜溶液的试管中加入氨水,首先形成难溶物,继续加入氨水,难溶物溶解并得到深蓝色的透明溶液.下列叙述正确的是B.
A.反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变
B.沉淀溶解后生成深蓝色的[Cu(NH3)4]2+
C.若硫酸铜溶液中混有少量硫酸,则可用氨水除去硫酸铜溶液中的硫酸
D.[Cu(NH3)4]2+的空间构型为平面正方形.
17.下列试剂不会因为空气中的二氧化碳和水蒸气而变质的是( )
| A. | Na2CO3 | B. | Na2O2 | C. | CaO | D. | Ca(ClO)2 |
4.向等物质的量浓度的Ba(OH)2与BaCl2的混合溶液中加入NaHCO3溶液,下列离子方程式与事实相符的是( )
| A. | HCO3-+OH-→CO32-+H2O | |
| B. | Ba2++OH-+HCO3-→BaCO3↓+H2O | |
| C. | Ba2++2OH-+2HCO3-→BaCO3↓+CO32-+H2O | |
| D. | 2Ba2++3OH-+3HCO3-→2BaCO3↓+CO32-+3H2O |
18.高铁酸钾(K2FeO4)是一种兼具净水和消毒功能的可溶性盐,可发生如下反应:2K2FeO4+16HCl→4KCl+2FeCl3+8H2O+3Q↑,下列说法不正确的是( )
| A. | 可用湿润的淀粉碘化钾试纸检验产物Q | |
| B. | K2FeO4在水中的电离方程式为K2FeO4→2K++Fe6++4O2一 | |
| C. | 反应中氧化剂与还原剂的物质的量之比为1:3 | |
| D. | 反应中涉及的物质中有5种为电解质 |
19.常温下,下列各组离子一定能在指定溶液中大量共存的是( )
| A. | 0.1 mol/L NH4HCO3溶液中:K+、Na+、NO3-、Cl- | |
| B. | $\frac{{k}_{W}}{c({H}^{+})}$=1×10-13 mol/L的溶液中:NH4+、Na+、SiO32-、Cl- | |
| C. | 与Al反应能放出H2的溶液中:Fe2+、K+、NO3-、SO42- | |
| D. | 水电离的c(H+)=1×10-13mol/L的溶液中:K+、Na+、AlO2-、CO32- |
 现有前四周期六种元素X、Y、Z、E、F、G,它们的原子序数依次增大,除G外,其它五种元素都是短周期元素.X、Y、E三种元素组成的化合物是实验室常用燃料.取F的化合物做焰色反应实验,其焰色呈黄色,G的单质是生活中常见的一种金属,GE是黑色固体.请回答下列问题:
现有前四周期六种元素X、Y、Z、E、F、G,它们的原子序数依次增大,除G外,其它五种元素都是短周期元素.X、Y、E三种元素组成的化合物是实验室常用燃料.取F的化合物做焰色反应实验,其焰色呈黄色,G的单质是生活中常见的一种金属,GE是黑色固体.请回答下列问题: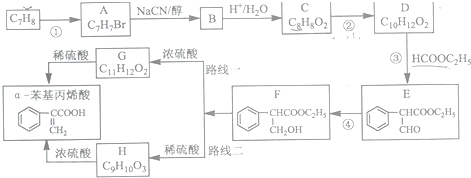


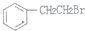 制备
制备 的合成路线.
的合成路线.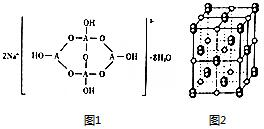 已知A、B、C、D、E五种元素是周期表中前四周期元素.且原子序数依次增大. 其中A、B、C为同周期的非金属元素,且B、C原子中均有两个未成对电子. D、E 为同周期元素且分别位于s区和d区.五种元素所有的s能均为全充满.E的d能级电子数等于A、B、C最高能层的p能级电子数之和.
已知A、B、C、D、E五种元素是周期表中前四周期元素.且原子序数依次增大. 其中A、B、C为同周期的非金属元素,且B、C原子中均有两个未成对电子. D、E 为同周期元素且分别位于s区和d区.五种元素所有的s能均为全充满.E的d能级电子数等于A、B、C最高能层的p能级电子数之和. .
.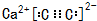 ,若细胞的长宽高分別为520pm、520pm和690pm,该晶体密度为2.28 g•cn-2(保留到小数点后两位).
,若细胞的长宽高分別为520pm、520pm和690pm,该晶体密度为2.28 g•cn-2(保留到小数点后两位).