题目内容
17.下列试剂不会因为空气中的二氧化碳和水蒸气而变质的是( )| A. | Na2CO3 | B. | Na2O2 | C. | CaO | D. | Ca(ClO)2 |
分析 不会因为空气中的二氧化碳和水蒸气而变质的是物质和二氧化碳、水蒸气不发生反应的物质,据此分析判断选项.
解答 解:A.碳酸钠是盐和二氧化碳、水蒸气都不发生反应,不会因为空气中的二氧化碳和水蒸气而变质,故A正确;
B.过氧化钠和空气中的二氧化碳、水蒸气都发生反应,会因为空气中的二氧化碳和水蒸气而变质,故B错误;
C.氧化钙是碱性氧化物和空气中的水反应生成氢氧化钙,会因为空气中的二氧化碳和水蒸气而变质,故C错误;
D.次氯酸钙会吸收空气中的二氧化碳和水蒸气发生反应生成次氯酸和碳酸钙,会因为空气中的二氧化碳和水蒸气而变质,故D错误;
故选A.
点评 本题考查了一些常见物质在空气中发生反应的问题,是对学生进行物质性质的训练与提高,难度不大.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
7.在以离子键为主的化学键中常含有共价键的成分,两种元素的电负性差异越小,其共价键成分越大.下列各对原子形成的化学键中共价键成分最多的是( )
| A. | K与F | B. | Na与Cl | C. | Al与S | D. | Mg与Cl |
8.离子化合物是离子通过离子键结合成的化合物.下列物质属于离子化合物的是( )
| A. | H2O | B. | HCl | C. | NH4Cl | D. | CO2 |
5.合成氨反应为:N2(g)+3H2(g)?2NH3(g).图1表示在一定的温度下此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线.图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响.下列说法正确的是( )
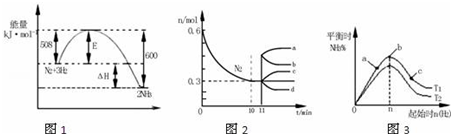

| A. | 由图1可知2NH3(g)?N2(g)+3H2(g)△H=-92kJ•mol-1 | |
| B. | 图2中0~10min内该反应的平均速率v(H2)=0.045mol•L-1•min-1,从11min起其它条件不变,压缩容器的体积为1L,则n(N2)的变化曲线为d | |
| C. | 图3中a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是b点 | |
| D. | 图3中T1和T2表示温度,对应温度下的平衡常数为K1、K2,则:T1>T2,K1>K2 |
12.下列物质的分子中,共用电子对数目最多的是( )
| A. | H2 | B. | NH3 | C. | H2O | D. | CH4 |
2.一种香豆素的衍生物结构如图所示,关于该有机物说法正确的是( )


| A. | 该有机物分子式为 C10H10O4 | |
| B. | 1mol该有机物与 H2发生加成时最多消耗H2 5 mol | |
| C. | 1mol该有机物与足量溴水反应时最多消耗Br23 mol | |
| D. | 1mol该有机物与 NaOH 溶液反应是最多消耗NaOH 3 mol |
9.能证明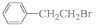 与过量NaOH醇溶液共热时发生了消去反应的是( )
与过量NaOH醇溶液共热时发生了消去反应的是( )
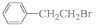 与过量NaOH醇溶液共热时发生了消去反应的是( )
与过量NaOH醇溶液共热时发生了消去反应的是( )| A. | 混合体系$\stackrel{溴水}{→}$Br2的颜色褪去 | |
| B. | 混合体系$\stackrel{足量稀HNO_{3}}{→}$ $\stackrel{AgNO_{3}溶液}{→}$淡黄色沉淀 | |
| C. | 混合体系$\stackrel{提取}{→}$有机物$\stackrel{酸性KMnO_{4}溶液}{→}$紫色褪去 | |
| D. | 混合体系$\stackrel{提取}{→}$有机物$\stackrel{Br_{2}的CCl_{4}溶液}{→}$Br2的颜色褪去 |
6.下列不能用于判断F和Cl的非金属性强弱的事实是( )
| A. | 气态氢化物的稳定性 | B. | 最高价氧化物对应水化物的酸性 | ||
| C. | 单质与氢气反应的难易 | D. | 单质与氢气反应放出热量的多少 |
7.NA代表阿伏伽德罗常数的值,下列说法不正确的是( )
| A. | 过氧化钠与水反应生成2.24 L O2时转移的电子数为0.2NA | |
| B. | 1 L 14 mol/L硝酸与足量铜反应生成气体分子数小于7NA | |
| C. | 1 L1 mol/L NaHS溶液中H2S、HS-和S2-粒子数之和为NA | |
| D. | 1 mol OH-的电子总数比1 mol-OH的电子总数多NA |