题目内容
14.如图所示,甲、乙为相互串联的两个电解池.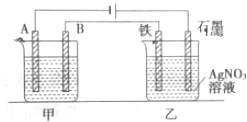
(1)甲池若为用电解原理精炼铜的装置,则A电极名称为阴极,电极材料是纯铜,电极反应式为Cu2++2e-═Cu,电解质溶液可以是含铜离子的盐溶液.
分析 依据电解精炼的原理是粗铜做阳极,精铜做阴极,含铜离子的电解质溶液进行电解反应,在阴极是溶液中铜离子得到电子生成铜.
解答 解:电解精炼的原理是粗铜做阳极,精铜做阴极,含铜离子的电解质溶液进行电解反应,在阴极是溶液中铜离子得到电子生成铜,电极反应是Cu2++2e-═Cu;
故答案为:阴;纯铜;Cu2++2e-═Cu;含铜离子的盐溶液.
点评 本题考查了电解原理的分析判断,装置分析判断电极名称是基础,掌握电化学基本知识是解题关键,题目难度不大.

练习册系列答案
 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
4.下列反应属于放热反应的是( )
| A. | 氢氧化钡晶体和氯化铵晶体的反应 | |
| B. |  能量变化如图所示的反应 | |
| C. | 燃烧反应和中和反应 | |
| D. | 化学键断裂吸收的热量比化学键生成放出的热量多的反应 |
5.下列说法正确的是( )
| A. | NO和NO2的排放能引起酸雨,还可能引起光化学烟雾 | |
| B. | 太阳能电池与普通电池相同,都可以把化学能转化为电能 | |
| C. | 含有重金属盐的皮革废料经水解制成的粉状物可掺入奶粉中 | |
| D. | 普通玻璃可以制钢化玻璃,也可以制光导纤维 |
2.某有机物a的分子式和己烷相同,且主链上有4个碳原子,则下列关于a的观点正确的是( )
| A. | a的一氯代物可能有三种 | |
| B. | a分子中可能有三个甲基 | |
| C. | a能与溴的四氯化碳溶液发生取代反应 | |
| D. | a的分子式为C6H10 |
6.将200mL 0.1mol•L-1 Na2CO3溶液与含1.71gBa(OH)2的溶液混合后,为使混合液呈中性,需再加入1mol•L-1盐酸的体积为( )
| A. | 30mL | B. | 40mL | C. | 50mL | D. | 60mL |
12.研究硫元素及其化合物的性质具有重要意义

(1)25℃,在0.10mol•L-1HA溶液中,通入HCl气体或加入Na〇H固体以调节 溶液PH,溶液pH与c(S2-)关系如图1(忽略溶液体积的变化、H2S的挥发).
①pH=11 时,溶液中的 c(H2S)+c(HS-)=0.0987 mol•L-1.(保留3位有效数字)
②某溶液含0.010mol•L-1 Fe2+、未知浓度的Mn2+和0.10mol•L-1H2S,当溶液pH=2 时,Fe2+开始沉淀;当Mn2+开始沉淀时,溶液中$\frac{c(M{n}^{2+})}{c(F{e}^{2+})}$=2.0×106.
[已知:Ksp(FeS)=1.4X10-19,Ksp(MnS)=2.8×10-13]
(2)硫化氢的转化是资源利用和环境保护的重要研究课题.由硫化氢获得硫单质有多种方法.其中一种是将烧碱吸收H2S后的溶液加入到如图2所示的电解池 的阳极区进行电解.请写出阳极的电极反应式S2--2e-═S,同时阳极区还发生(n-1)S+S2-═Sn2-.电解后阳极区的溶液用稀硫酸酸化,产生淡黄色浑浊,其离子方程式为Sn2-+2H+=(n-1)S↓+H2S↑.
(3)25℃,两种酸的电离平衡常数如表.
实验室常用饱和NaHC03溶液除去C02中少量的S02,请写出S02和NaHC03溶液反应的主要离子方程式SO2+HCO3-=HSO3-+CO2↑.

(1)25℃,在0.10mol•L-1HA溶液中,通入HCl气体或加入Na〇H固体以调节 溶液PH,溶液pH与c(S2-)关系如图1(忽略溶液体积的变化、H2S的挥发).
①pH=11 时,溶液中的 c(H2S)+c(HS-)=0.0987 mol•L-1.(保留3位有效数字)
②某溶液含0.010mol•L-1 Fe2+、未知浓度的Mn2+和0.10mol•L-1H2S,当溶液pH=2 时,Fe2+开始沉淀;当Mn2+开始沉淀时,溶液中$\frac{c(M{n}^{2+})}{c(F{e}^{2+})}$=2.0×106.
[已知:Ksp(FeS)=1.4X10-19,Ksp(MnS)=2.8×10-13]
(2)硫化氢的转化是资源利用和环境保护的重要研究课题.由硫化氢获得硫单质有多种方法.其中一种是将烧碱吸收H2S后的溶液加入到如图2所示的电解池 的阳极区进行电解.请写出阳极的电极反应式S2--2e-═S,同时阳极区还发生(n-1)S+S2-═Sn2-.电解后阳极区的溶液用稀硫酸酸化,产生淡黄色浑浊,其离子方程式为Sn2-+2H+=(n-1)S↓+H2S↑.
(3)25℃,两种酸的电离平衡常数如表.
| Ka | Ka2 | |
| H2S03 | 1.3×10-2 | 6.3×10-8 |
| H2C03 | 4.2×10-7 | 5.6×10-11 |
13.下列关于物质或离子检验的叙述正确的是( )
| A. | 向某溶液中滴加氯水,再滴加KSCN溶液,若溶液变成血红色,则原溶液中一定有Fe2+ | |
| B. | 钾元素焰色反应的操作是:将铂丝放在稀盐酸中洗涤后灼烧至无色,然后再用铂丝蘸取固体氯化钾,进行灼烧,直接观察火焰颜色 | |
| C. | 向某溶液中滴加氯化钡溶液,产生白色沉淀,再滴加足量稀硝酸,依然有白色固体,说明原溶液含有SO42- | |
| D. | 向某黄色溶液中加入淀粉溶液,若溶液变蓝色,则原溶液中含有I2 |